Clear Sky Science · de
Die Zielsteuerung der UFL1-AKT-Kaskade unterdrückt das Fortschreiten des triple-negativen Mammakarzinoms
Warum diese Forschung wichtig ist
Das triple-negative Mammakarzinom (TNBC) zählt zu den tödlichsten Formen von Brustkrebs, weil ihm die Hormon- und Wachstumsfaktor-Schaltstellen fehlen, auf die viele moderne Medikamente abzielen. Patientinnen erhalten oft nur konventionelle Chemotherapien, die im Verlauf unwirksam werden können, wenn Tumoren Resistenzen entwickeln. Diese Studie enthüllt einen bislang verborgenen molekularen „Motor“, der TNBC-Zellen beim Wachstum und bei der Umgehung von Chemotherapie unterstützt, und schlägt einen neuen Wirkstofftyp vor, der diesen Motor direkt blockiert.
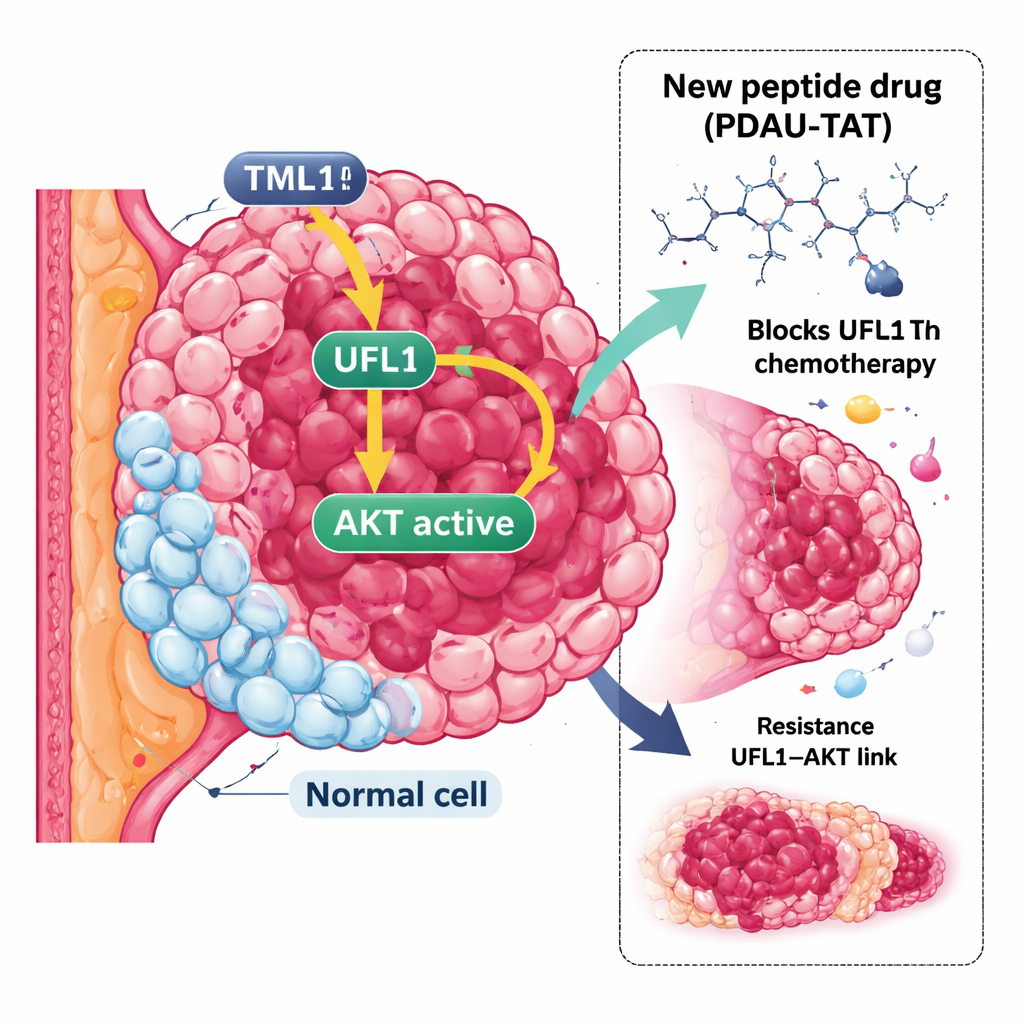
Eine hartnäckige Krebsform
TNBC ist definiert durch das Fehlen dreier häufiger Marker: des Östrogenrezeptors, des Progesteronrezeptors und des HER2-Wachstumsrezeptors. Mangels dieser Marker greifen viele erfolgreiche zielgerichtete Therapien nicht. Stattdessen werden Standardmedikamente wie Cisplatin und Doxorubicin eingesetzt, doch TNBC-Tumoren sind häufig resistent oder passen sich schnell an diese Behandlungen an und neigen stärker zur Metastasierung. Das schafft einen dringenden Bedarf an neuen Strategien, die über die üblichen Verdächtigen hinaus nach anderen Schwachstellen in den Kontrollsystemen des Tumors suchen.
Ein wenig bekanntes Protein mit großer Wirkung
Die Forschenden konzentrierten sich auf UFL1, ein Protein, das ein kleines Tag namens UFM1 an andere Proteine anhängt — ein Prozess, der als UFMylierung bekannt ist. Dieses Markierungssystem wurde erst vor Kurzem entdeckt, und seine Rolle beim Krebs war bislang unklar und teils widersprüchlich. Durch die Analyse von Patientendaten und Tumorproben zeigten die Autorinnen und Autoren, dass UFL1 in TNBC deutlich erhöht ist im Vergleich zu normalem Brustgewebe. Reduzierten sie UFL1 in TNBC-Zelllinien und Maus-Tumormodellen, teilten sich die Krebszellen langsamer und wurden deutlich empfindlicher gegenüber Chemotherapie, was nahelegt, dass UFL1 in diesem Kontext tumorfördernd wirkt.
UFL1 als Verbindung zu einem zentralen Wachstumsschalter
Bei tiefergehenden Untersuchungen entdeckten die Wissenschaftlerinnen und Wissenschaftler, dass UFL1 direkt an AKT bindet, ein zentrales Signalprotein, das Zellwachstum, Überleben und Stoffwechsel antreibt und in vielen Krebsarten überaktiv ist. Bei TNBC ist AKT häufig überaktiv, selbst wenn die üblichen upstream-Mutationen fehlen. Das Team fand heraus, dass UFL1 AKT an drei spezifischen Stellen chemisch markiert, wodurch AKT leichter von seinen aktivierenden Partnern eingeschaltet werden kann und gleichzeitig vor Enzymen geschützt wird, die es normalerweise ausschalten würden. Zellen ohne UFL1 oder mit einer so veränderten AKT-Variante, die diese Markierungen nicht annehmen kann, zeigten deutlich geringere AKT-Aktivität, langsameres Wachstum und größere Anfälligkeit für Chemotherapie sowohl in Zellkulturen als auch in Tiermodellen.
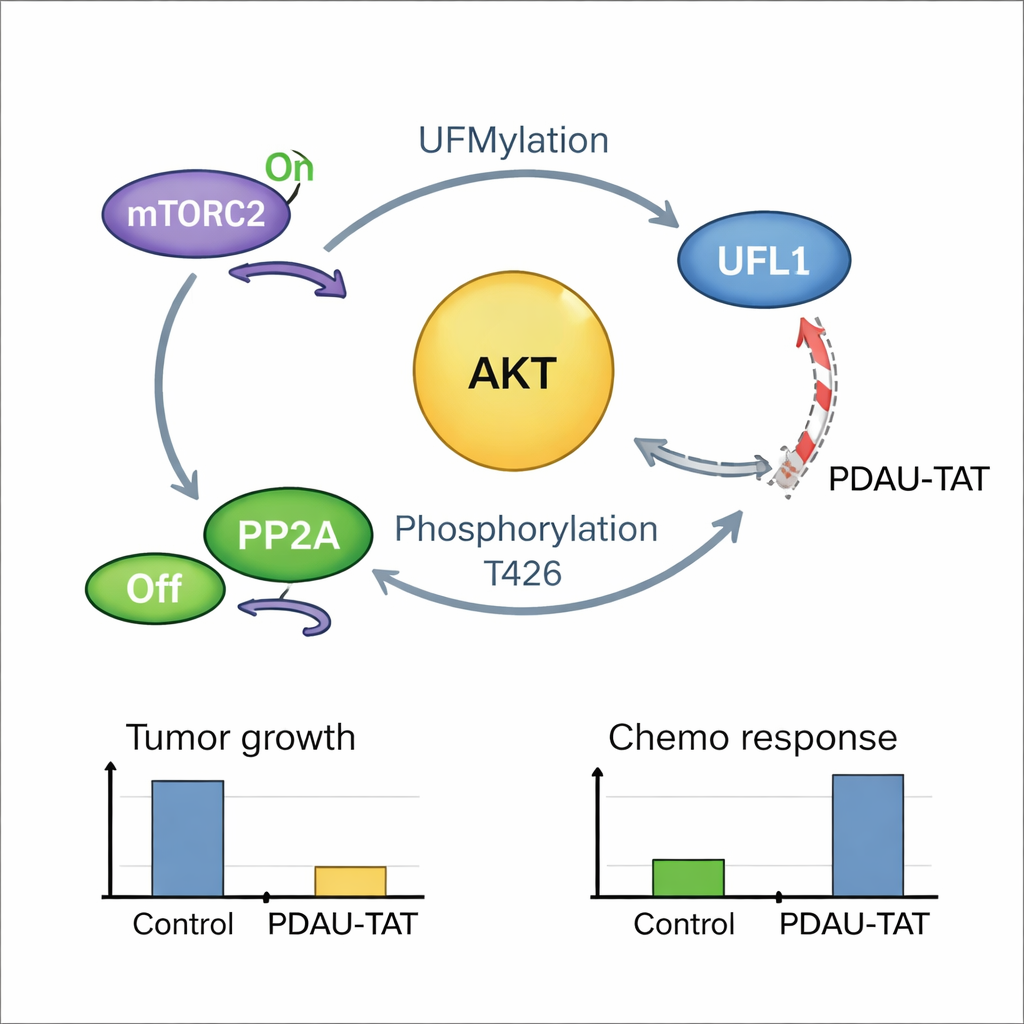
Eine sich selbst verstärkende Krebs-Schleife und ein Weg, sie zu durchbrechen
Die Verbindung erwies sich als noch enger: Ist AKT erst aktiviert, wirkt es rückkoppelnd auf UFL1 und modifiziert es an einer entscheidenden Stelle, wodurch UFL1s Markierungsaktivität gegenüber AKT und anderen Zielen verstärkt wird. So entsteht eine positive Rückkopplungsschleife, in der UFL1 AKT aktiviert und aktives AKT wiederum UFL1 weiter verstärkt. Patientenproben zeigten, dass hohe Spiegel modifizierten UFL1 stark mit hohen Spiegeln aktiven AKT korrelieren, was die Existenz dieser Schleife beim Menschen stützt. Um diese Verwundbarkeit auszunutzen, entwarf das Team ein kurzes, zellgängiges Peptid namens PDAU-TAT, das eine kleine Region von UFL1 nachahmt und sich zwischen UFL1 und AKT klemmt. Dieses Peptid stört ihre Interaktion, reduziert AKT-Aktivierung, verlangsamt das Tumorwachstum und macht TNBC-Zellen sowie aus Patientinnen gewonnene Tumoren empfindlicher gegenüber Chemotherapie, ohne in Mäusen offensichtliche Schäden an wichtigen Organen zu verursachen.
Was das für Patientinnen bedeuten könnte
Vereinfacht gesagt haben die Forschenden eine verborgene Verdrahtung in TNBC-Zellen aufgedeckt: UFL1 und AKT stecken in einer sich selbst verstärkenden Schleife, die Wachstumssignale dauerhaft „an“ hält und Tumoren hilft, Behandlungen zu widerstehen. Indem sie ein kleines Peptid entwickeln, das sich in diese Schleife einschleicht und UFL1 von AKT trennt, zeigen sie einen plausiblen neuen Weg, TNBC-Tumoren zu schwächen bei gleichzeitiger Schonung normaler Zellen, die in der Regel niedrigere UFL1-Spiegel aufweisen. Obwohl diese Arbeit noch präklinisch ist, weist sie auf eine neue Klasse zielgerichteter Therapien hin, die nicht die üblichen Rezeptoren adressieren, sondern die Protein‑Protein‑Verbindungen, die einige der aggressivsten Brustkrebse antreiben.
Zitation: Yang, X., Wen, Y., Ma, X. et al. Targeting the UFL1-AKT cascade suppresses triple-negative breast cancer progression. Nat Commun 17, 613 (2026). https://doi.org/10.1038/s41467-026-68493-2
Schlüsselwörter: triple-negatives Mammakarzinom, AKT-Signalgebung, UFMylierung, UFL1, Peptid-Krebstherapie