Clear Sky Science · de
Bradyzoiten-Subtypen bestimmen die Weggabelung in der Entwicklung von Toxoplasma
Verborgene Stadien eines verbreiteten Parasiten
Toxoplasma gondii ist ein winziger Parasit, der stillschweigend etwa jeden dritten Menschen weltweit infiziert, meist ohne dass die Betroffenen es bemerken. Bei Menschen mit geschwächtem Immunsystem – etwa Krebspatienten unter Chemotherapie oder Personen mit AIDS – kann der Parasit jedoch aus einem ruhenden Zustand erwachen und schwere, mitunter tödliche Hirnerkrankungen auslösen. Diese Studie untersucht genau diese ruhende Phase, um eine einfache, aber entscheidende Frage zu beantworten: Sind alle „schlafenden“ Parasiten gleich, oder gibt es verschiedene Typen mit unterschiedlichen Aufgaben?
Warum ruhende Parasiten wichtig sind
Während der Langzeitinfektion versteckt sich Toxoplasma in widerstandsfähigen, mikroskopisch kleinen Bläschen im Gehirn und in Muskeln, den sogenannten Gewebszysten. In jeder Zyste leben Hunderte von Bradyzoiten, der langsam wachsenden, ruhenden Form des Parasiten. Diese Bradyzoiten bilden das Reservoir für lebenslange Infektion und können plötzlich wieder in eine schnell wachsende Form, die Tachyzoiten, übergehen, welche Gewebe schädigen und sich im Körper ausbreiten. Da aktuelle Medikamente diese Zysten nicht beseitigen, ist ein genaues Verständnis dessen, was sich in ihnen abspielt, entscheidend, um Reaktivierungen bei gefährdeten Patienten zu verhindern.
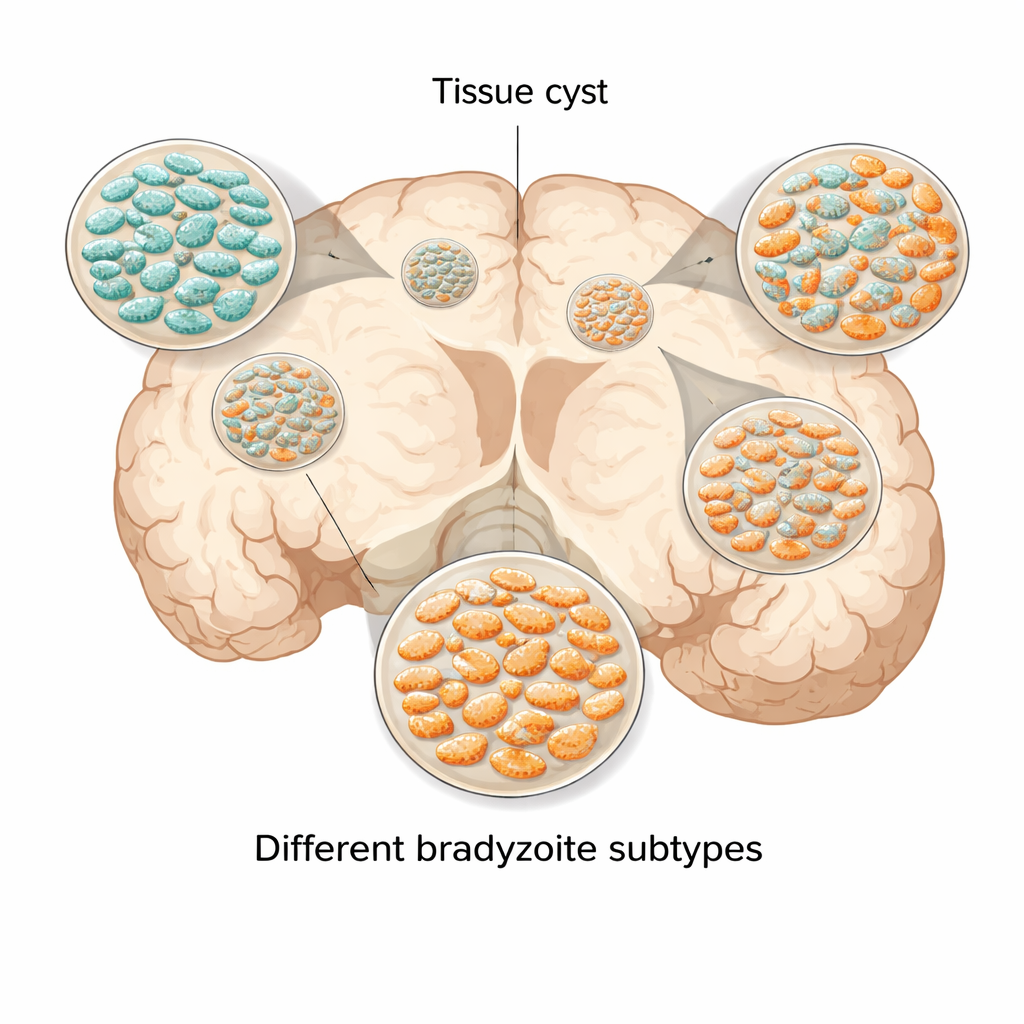
Unterschiedliche „Persönlichkeiten“ in Zysten entdecken
Die Forscher konzentrierten sich auf ein Oberflächenmolekül namens SRS22A, das bei einigen Bradyzoiten in Mäusen vorkommt, in Standard-Laborkulturen von Zysten aber auffällig fehlt. Mit speziell hergestellten Antikörpern als molekulare „Leuchtmarker“ zeigten sie, dass Gehirnzysten aus infizierten Mäusen nicht einheitlich sind. Manche Zysten sind fast vollständig mit SRS22A-positiven Parasiten gefüllt, manche fehlen diesen Marker völlig, und viele enthalten eine Mischung aus beiden. Diese Muster verändern sich im Verlauf der Infektion und zeigen, dass Zysten wachsen, aufreißen und sich neu bilden, dabei aber eine reiche interne Vielfalt bewahren, anstatt in einem einzigen, ausgereiften Endzustand zu enden.
Zwei Hauptwege: Ausbreiten versus Verweilen
Um zu prüfen, was diese Unterschiede bedeuten, trennten die Wissenschaftler SRS22A-positive und SRS22A-negative Bradyzoiten aus Mausgehirnen und verfolgten, was geschah, wenn jede Gruppe Hirnzellen in Kultur und lebende Mäuse infizierte. SRS22A-positive Parasiten verwandelten sich rasch in schnell replizierende Tachyzoiten, die sich durch Zellschichten und Organe der Maus ausbreiteten. Infizierte Mäuse trugen in der frühen Phase der Infektion mehr Parasiten und entwickelten später deutlich mehr Hirnzysten. Im Gegensatz dazu blieben SRS22A-negative Parasiten tendenziell in der Bradyzoiten-Form, vermehrten sich langsam und bauten neue Zystwände auf. Anstatt eine explosive Ausbreitung voranzutreiben, schien diese Gruppe darauf ausgerichtet zu sein, das langfristige Reservoir leise zu erhalten.
Fünf Subtypen durch Einzelzell-Profilierung aufgedeckt
Noch genauer untersuchten die Wissenschaftler die Parasiten mit Einzelzell-RNA-Sequenzierung, einer Technik, die abliest, welche Gene in Tausenden einzelner Parasiten aktiv sind. Dabei wurden mindestens fünf Hauptsubtypen von Bradyzoiten innerhalb chronischer Gehirnzysten entdeckt, jeder mit einer eigenen Genaktivitäts-„Signatur“. Eine Gruppe, die für SRS22A und andere Marker angereichert war, die sonst typischerweise in der Katzen-Phase des Parasiten vorkommen, könnte darauf vorbereitet sein, die sexuelle Vermehrung wieder aufzunehmen, wenn eine Katze infizierte Beutetiere frisst. Andere Gruppen schalteten Gene an, die mit Invasionswerkzeugen oder dem Aufbau der Zystwand verknüpft sind, was darauf hindeutet, dass einige Parasiten sich darauf vorbereiten, auszubrechen und neue Zellen zu infizieren, während andere die Schutzhülle um die Gemeinschaft verstärken.
Neues Nachdenken über einen einfachen Lebenszyklus
In der Summe stellen diese Befunde das einfache Lehrbuchbild in Frage, wonach Toxoplasma langsam vom schnellen Tachyzoiten in eine einzige, stabile „ruhende“ Bradyzoiten-Form übergeht. Vielmehr ähnelt jede Zyste eher einem kleinen, gemischten Dorf von Spezialisten: Einige Parasiten stehen bereit, auszubrechen und sich zu verbreiten, einige vertiefen die chronische Infektion durch den Aufbau neuer Zysten, und andere sind möglicherweise für den Sprung in einen Katzenwirt vorbereitet. Diese Komplexität erklärt, warum Labor‑Modelle, die nur eine Teilmenge dieser Typen erzeugen, wichtige Verhaltensweisen realer Infektionen übersehen können und warum Medikamente, die nur eine Phase angreifen, oft nicht zur Heilung führen.
Was das für Patienten bedeutet
Für Menschen mit einer Toxoplasma-Infektion ist die Botschaft der Studie: Die „schlafenden“ Parasiten in ihrem Gewebe sind nicht alle gleich. Bestimmte Subtypen erscheinen als die treibenden Kräfte hinter gefährlichen Aufflackern, während andere eine stille, chronische Infektion aufrechterhalten oder den Parasiten auf die Übertragung zu neuen Wirten vorbereiten. Durch die Identifizierung von Oberflächenmarkern wie SRS22A und von Genmustern, die diese Subtypen unterscheiden, haben Forscher jetzt einen Fahrplan, um bessere Labor‑Modelle, Impfstoffe und Medikamente zu entwickeln, die gezielt die Formen angreifen, die am ehesten schwere Erkrankungen verursachen. Langfristig könnten daraus Therapien entstehen, die nicht nur Symptome kontrollieren, sondern verhindern, dass der Parasit jemals wieder erwacht.
Zitation: Ulu, A., Srivastava, S., Kachour, N. et al. Bradyzoite subtypes rule the crossroads of Toxoplasma development. Nat Commun 17, 1783 (2026). https://doi.org/10.1038/s41467-026-68489-y
Schlüsselwörter: Toxoplasma gondii, Bradyzoit, Gewebszyste, Reaktivierung des Parasiten, Einzelzell-RNA-Sequenzierung