Clear Sky Science · de
Kontinuierlich einstellbare Multistabilität in DNA‑Replikationsnetzwerken
Von einfachen Schaltern zu vielen möglichen Zuständen
Biologische Systeme, von sich teilenden Zellen bis zu sich entwickelnden Embryonen, funktionieren selten wie einfache Lichtschalter, die nur an oder aus sind. Stattdessen halten sie oft viele langlebige Zustände, ähnlich einem Dimmer, der in unzähligen Positionen stehen bleiben kann. Dieser Artikel berichtet über ein DNA‑basiertes chemisches Netzwerk, das eher wie jener Dimmer arbeitet: Es kann stabil nicht nur einige wenige Zustände, sondern im Wesentlichen beliebige Zusammensetzungen entlang eines kontinuierlichen Spektrums aufrechterhalten. Diese Fähigkeit könnte eine leistungsfähige Grundlage für künftige intelligente Materialien, molekulare Speicher und biochemische Computer sein, die analoge und nicht nur digitale Informationen verarbeiten.
Warum mehrere stabile Zustände wichtig sind
Viele zelluläre Entscheidungen — ob eine Stammzelle reift, eine Zelle sich selbst zerstört oder ein Genetzwerk ein vergangenes Signal speichert — hängen von „Multistabilität“ ab, also der Fähigkeit, unter gleichen Bedingungen in mehr als einem stabilen Aktivitätsmuster zu verharren. Traditionelle synthetische Varianten solcher Systeme wurden aus Genkreisen, Enzymen oder DNA‑Strängen aufgebaut, die einander ein‑ oder ausschalten. Diese Entwürfe liefern typischerweise eine Handvoll diskreter Ausgänge, wie klassische bistabile Schalter mit zwei langlebigen Zuständen. Die Skalierung dieser Idee ist schwierig: Ein N‑Zustands‑System kann ungefähr N×(N−1) sorgfältig abgestimmte Hemmverbindungen erfordern, und das System springt dennoch nur zwischen wenigen festen Punkten statt entlang eines glatten Kontinuums von Möglichkeiten.
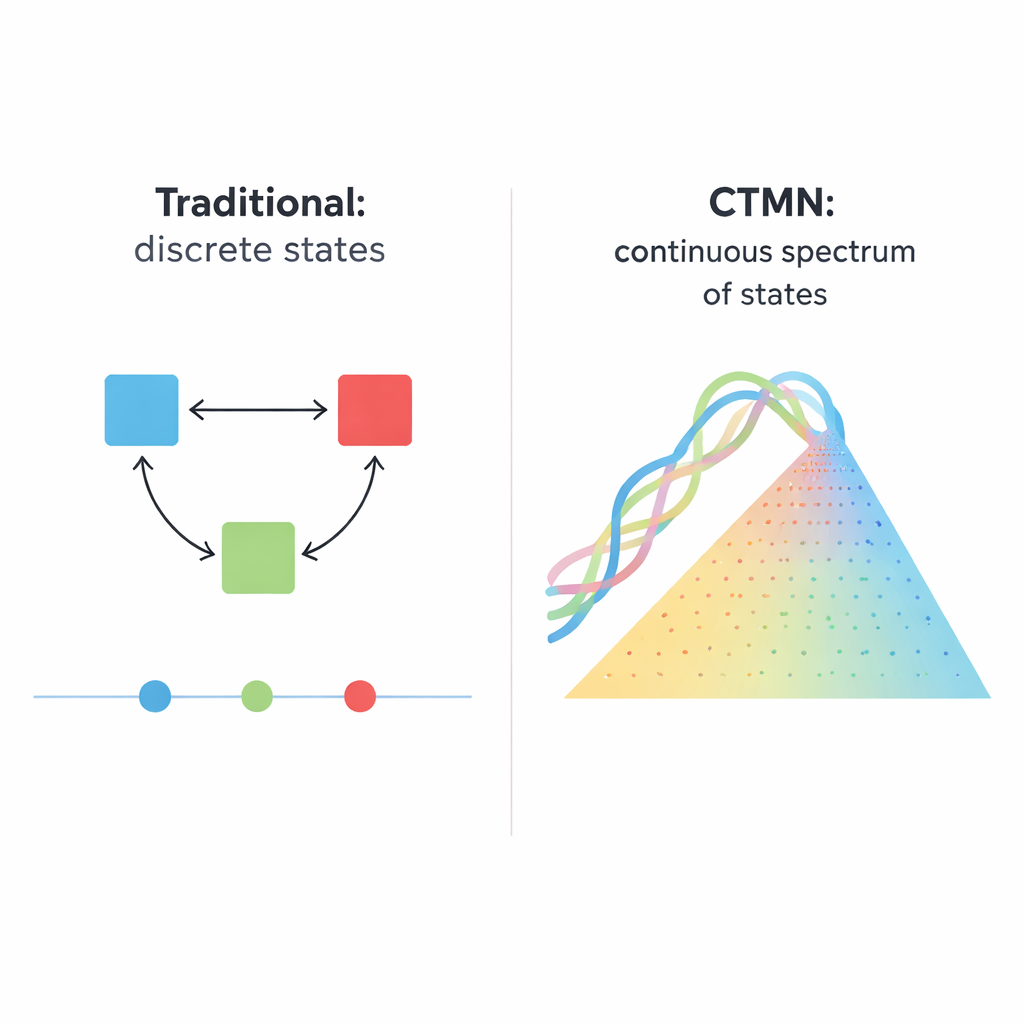
Ein neues DNA‑Netzwerk: kontinuierlich einstellbar
Die Autoren stellen ein anderes Gestaltungsprinzip vor, umgesetzt in den so genannten kontinuierlich einstellbaren Multistabilitätsnetzwerken (CTMNs). Anstatt auf viele separate inhibitory Signale zu setzen, nutzen sie direkte Konkurrenz zwischen DNA‑Replikationsmodulen, die durch reversible Strang‑Austausch‑Reaktionen verbunden sind. Jedes Modul besteht aus konstruierten DNA‑Doppelsträngen, die sowohl an Strangverdrängungsreaktionen teilnehmen als auch als Vorlage für eine DNA‑Polymerase dienen können, unterstützt von einer Nicking‑Enzymaktivität, die wichtige Segmente schneidet und regeneriert. Der chemische Treibstoff — Nukleotidbausteine, dNTPs genannt — treibt andauernde Polymerisation und Nicking an und hält das System weit vom Gleichgewicht entfernt. Unter diesen Bedingungen „frieren“ die konkurrierenden Module effektiv in den relativen Anteilen ein, mit denen sie gestartet sind, und erzeugen nicht nur zwei oder drei Ergebnisse, sondern eine ganze kontinuierliche Linie (oder bei mehreren Modulen eine Ebene) langlebiger Zustände.
Wie die molekulare Maschinerie das Gedächtnis festschreibt
In ihrem einfachsten Zwei‑Modul‑Netzwerk, CTMN‑1, zeigen die Forscher experimentell und durch detaillierte kinetische Modellierung, dass sich das System in eine Familie stabiler Mischungen einpendeln kann, die nahezu den gesamten Bereich von „überwiegend Modul A“ bis „überwiegend Modul B“ abdecken. Die Polymerisation wandelt aktive Doppelstränge in verlängerte Formen um, die vorübergehend aus dem Strangaustausch konkurrierenden Kreislauf entfernt sind; Nicking stellt sie dann wieder her und schließt damit eine autoregulatorische Schleife. Wenn beide Module diese Schleife teilen, unterdrücken sie die wechselseitige Umwandlung so stark, dass das System nahe seiner Anfangszusammensetzung für viele Stunden gesperrt bleibt, solange Treibstoff vorhanden ist. Die lineare Stabilitätsanalyse der zugrunde liegenden Gleichungen zeigt eine ganze Mannigfaltigkeit — effektiv ein Kontinuum — von stationären Zuständen, im Gegensatz zu dem einzelnen Fixpunkt, der zu sehen ist, wenn Enzyme oder Treibstoff entfernt werden.
Programmierbare Reaktionen und molekulares Gedächtnis
Da der Zustand des Netzwerks in DNA‑Zusammensetzungen gespeichert ist, lässt er sich auf programmierbare Weise steuern und auslesen. Die Autoren entwerfen kurze RNA‑„Trigger“, die vorübergehend spezifische DNA‑Stränge binden, die Konkurrenz zugunsten eines Moduls verschieben und das Netzwerk in eine neue Zusammensetzung lenken. Selbst nachdem die RNA von einem Enzym abgebaut wurde, bleibt der neue Zustand erhalten und fungiert als eine Form von molekularem Gedächtnis. Wiederholte oder stärkere Stimuli treiben das System glatt entlang des Kontinuums von Zuständen, statt es zwischen einfachen Ein/Aus‑Positionen umzuschalten. Zudem können die DNA‑Replikationsprodukte selbst so gestaltet werden, dass sie als Signale für nachgelagerte Prozesse dienen: In Demonstrationen aktivierten verschiedene Zustände von CTMN‑1 selektiv einen von zwei DNA‑basierten Katalysatoren oder lenkten die RNA‑Transkription zugunsten eines von zwei Botensträngen, ohne die zugrundeliegende Multistabilität zu stören.
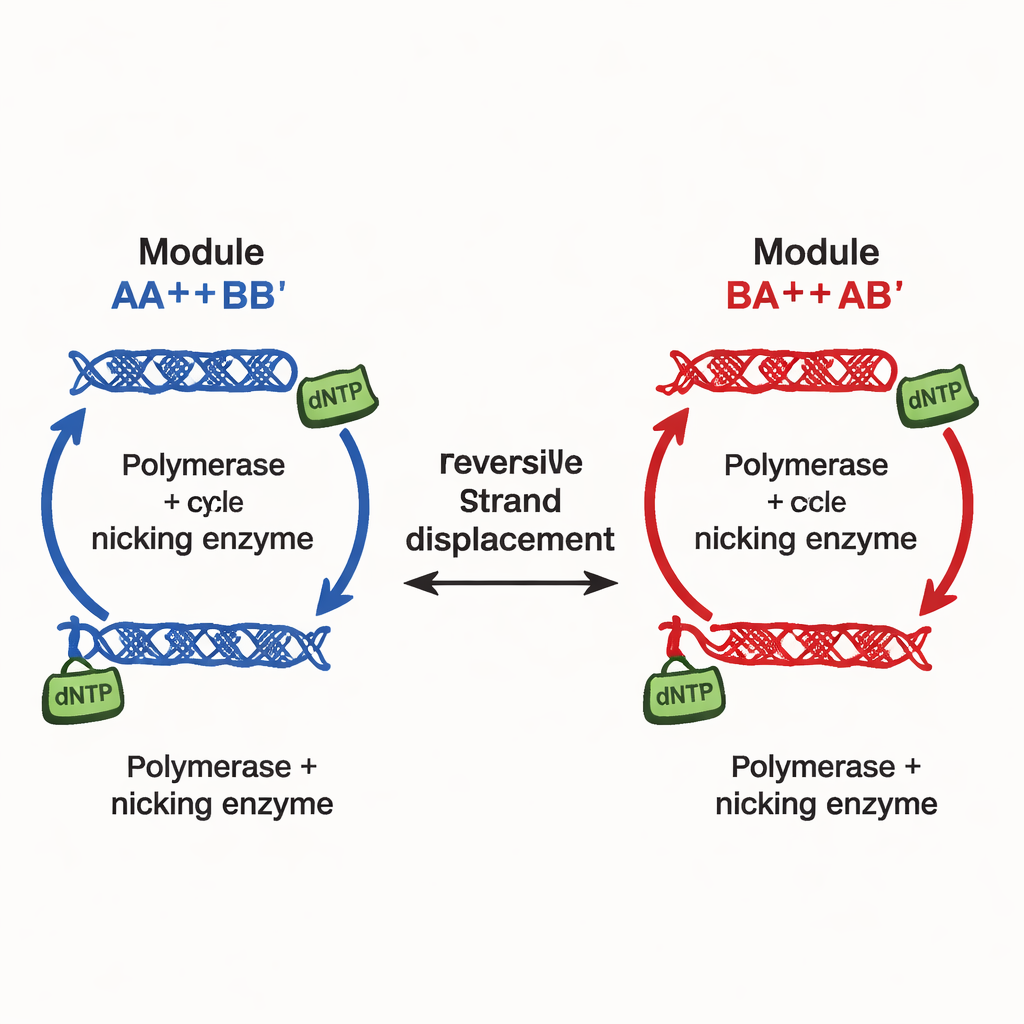
Hochskalierung zu komplexen molekularen „Dimmern”
Um zu zeigen, dass die Strategie skalierbar ist, bauen die Forscher ein Drei‑Modul‑Netzwerk, CTMN‑2, indem sie weitere entworfene DNA‑Doppelstränge hinzufügen, die eine gemeinsame Austauschdomäne teilen, aber unterschiedliche Replikationsvorlagen kodieren. Nun füllen die möglichen stationären Zustände eine zweidimensionale Region aus, wie Punkte in einem dreieckigen Phasendiagramm, statt entlang einer einfachen Linie. Erneut bestätigen Experimente, dass viele verschiedene Zusammensetzungen stabil sind, solange Treibstoff und Enzyme vorhanden sind, und dass alle zu einem einzigen Gleichgewichtspunkt kollabieren, wenn die Energiezufuhr wegfällt. Da das Hinzufügen neuer Module lediglich neue DNA‑Konstrukte erfordert, die in denselben Verdrängungsrahmen eingesteckt werden, wächst die Gesamtverdrahtung nicht in der Komplexität wie bei traditionellen Entwürfen.
Was das für künftige molekulare Technologien bedeutet
Für Nicht‑Spezialisten ist die Kernbotschaft, dass die Autoren ein DNA‑Replikationsnetzwerk in ein hochflexibles, analoges Speichersystem verwandelt haben. Statt zwischen wenigen voreingestellten Optionen zu wählen, kann ihr System zuverlässig einen von Dutzenden experimentell unterscheidbarer Zustände halten, jeder definiert durch die Menge jedes DNA‑Moduls, und transiente chemische Pulse in langlebige Verschiebungen entlang dieses Kontinuums umwandeln. Da die Ausgangs‑DNA‑Stränge programmierbar und von dem stabilisierenden Mechanismus entkoppelt sind, könnte derselbe Rahmen prinzipiell eine breite Palette nachgeschalteter biochemischer Reaktionen oder Materialeigenschaften mit feiner, abgestufter Kontrolle regulieren. Diese Arbeit weist somit auf molekulare Geräte hin, die eher wie neuronale oder mechanische analoge Systeme rechnen, erinnern und sich anpassen als wie einfache digitale Schalter.
Zitation: Zhong, R., Fu, Y., Jiang, S. et al. Continuously tunable multistability in DNA replication networks. Nat Commun 17, 1782 (2026). https://doi.org/10.1038/s41467-026-68488-z
Schlüsselwörter: DNA‑Multistabilität, molekulares Gedächtnis, synthetische biochemische Netzwerke, DNA‑Strangverdrängung, analoge molekulare Berechnung