Clear Sky Science · de
Robuste und interpretierbare Vorhersage von Genmarkern und Zelltypen aus Spatial-Transcriptomics-Daten
Routine-Gewebeschnitte in molekulare Karten verwandeln
Wenn eine Biopsie entnommen wird, sehen Ärzte normalerweise nur das, was das Mikroskop zeigt: die Formen und Muster von Zellen in rosa-violetten Färbungen. Unter diesen Farben verbirgt sich jedoch eine Welt von Genen, die an- und abgeschaltet werden und beeinflussen, wie ein Krebs wächst und auf Behandlung reagiert. Diese Studie stellt STimage vor, ein neues System der künstlichen Intelligenz (KI), das darauf abzielt, dieses molekulare Skript direkt aus standardmäßigen Pathologiebildern zu lesen und so potenziell schnellere, kostengünstigere Einblicke ohne zusätzliche Labortests zu liefern.
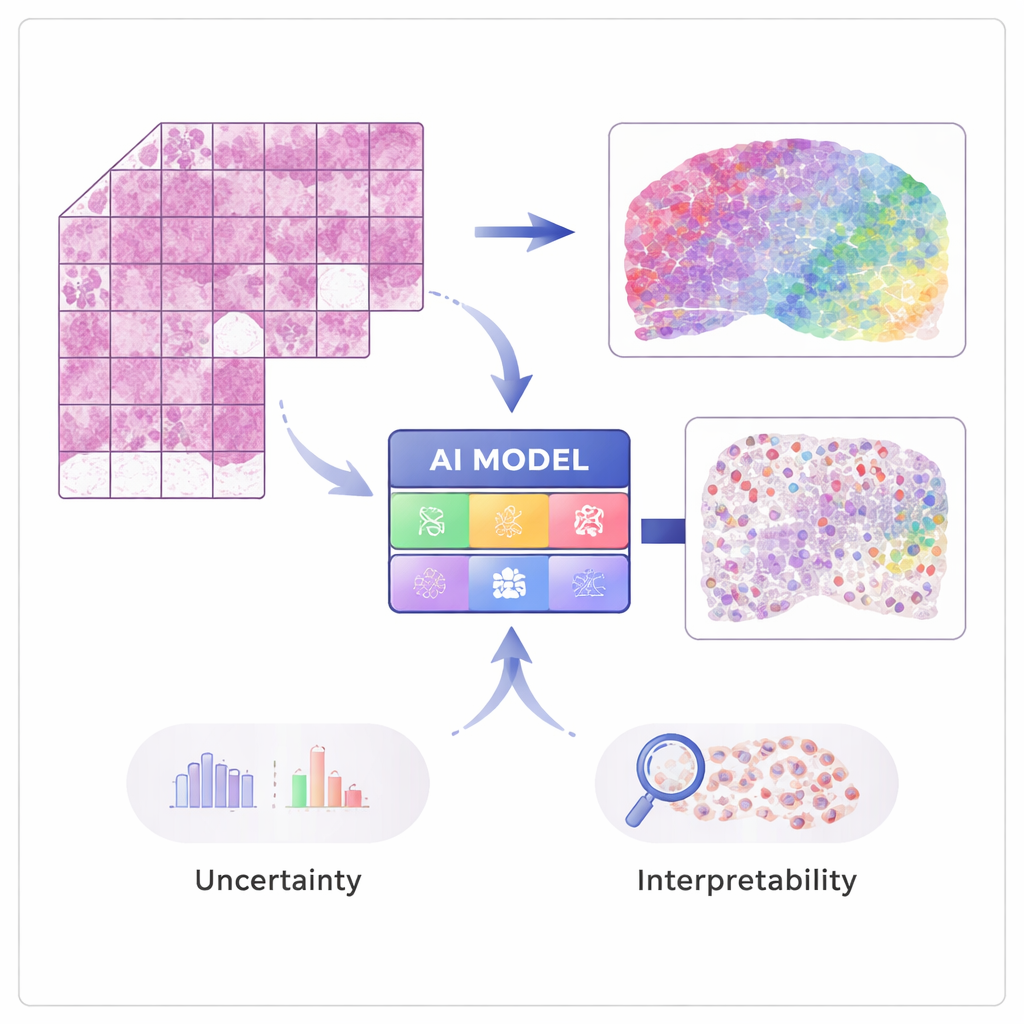
Von Bildern zur Genaktivität
Moderne Techniken der „spatialen Transkriptomik“ können die Aktivität zehntausender Gene messen und zugleich bewahren, wo im Gewebe jedes Signal herkommt. Diese Methoden sind leistungsfähig, aber teuer und noch nicht routinemäßig in Kliniken verfügbar. STimage wird an einer überschaubaren Anzahl solcher spatialer Datensätze trainiert, in denen jedem Gewebebild detaillierte Genmessungen an vielen kleinen Punkten zugeordnet sind. Die KI lernt, lokale visuelle Muster auf der Hämatoxylin‑und‑Eosin-(H&E-)Färbung — etwa die Dichte oder Unregelmäßigkeit der Zellkerne — mit der zugrunde liegenden Genaktivität zu verknüpfen, sodass sie später Genexpression und Zelltypen allein aus gewöhnlichen Bildern vorhersagen kann.
Aufbau eines vertrauenswürdigeren KI-Pathologen
Ein zentrales Ziel der Arbeit ist nicht nur Genauigkeit, sondern Zuverlässigkeit und Erklärbarkeit. Statt für jedes Gen nur eine einzelne Zahl auszugeben, sagt STimage eine vollständige Wahrscheinlichkeitsverteilung voraus, die einen wahrscheinlichen Bereich der Genaktivität an jedem Ort beschreibt. Es trennt außerdem zwei Arten von Unsicherheit: eine, die durch verrauschte oder variable Daten bedingt ist, und eine andere, die das fehlende Wissen des Modells widerspiegelt. Durch das Trainieren vieler leicht unterschiedlicher Modellversionen und deren Mittelung — ein sogenannter Ensemble-Ansatz — verbessern die Forschenden sowohl die Leistung als auch das Verständnis dafür, wo das System zuversichtlich ist und wo nicht, was für klinische Entscheidungen entscheidend ist.
Testen über Krebsarten, Technologien und Krankenhäuser hinweg
Das Team evaluierte STimage an vielfältigen Datensätzen aus Brust-, Haut- und Nierenkrebs sowie an einer immunologisch bedingten Lebererkrankung. Es lernte, wichtige Krebs- und Immunmarker vorherzusagen und stimmte oft mit den tatsächlichen räumlichen Mustern überein, die unabhängige Experimente zeigten. Das Modell hielt sich auch bei Daten aus verschiedenen Laboren, unterschiedlichen Probenvorbereitungen und sogar unterschiedlichen Basistechnologien — einschließlich Plattformen mit Einzelzellauflösung und älteren, niedrigauflösenderen Systemen — robust. In direkten Vergleichen mit mehreren bestehenden KI-Werkzeugen lagen STimage und seine Ensemble-Varianten meist vorn, besonders wenn beurteilt wurde, wie gut die vorhergesagten Muster der realen Verteilung der Genaktivität im Gewebe entsprachen.
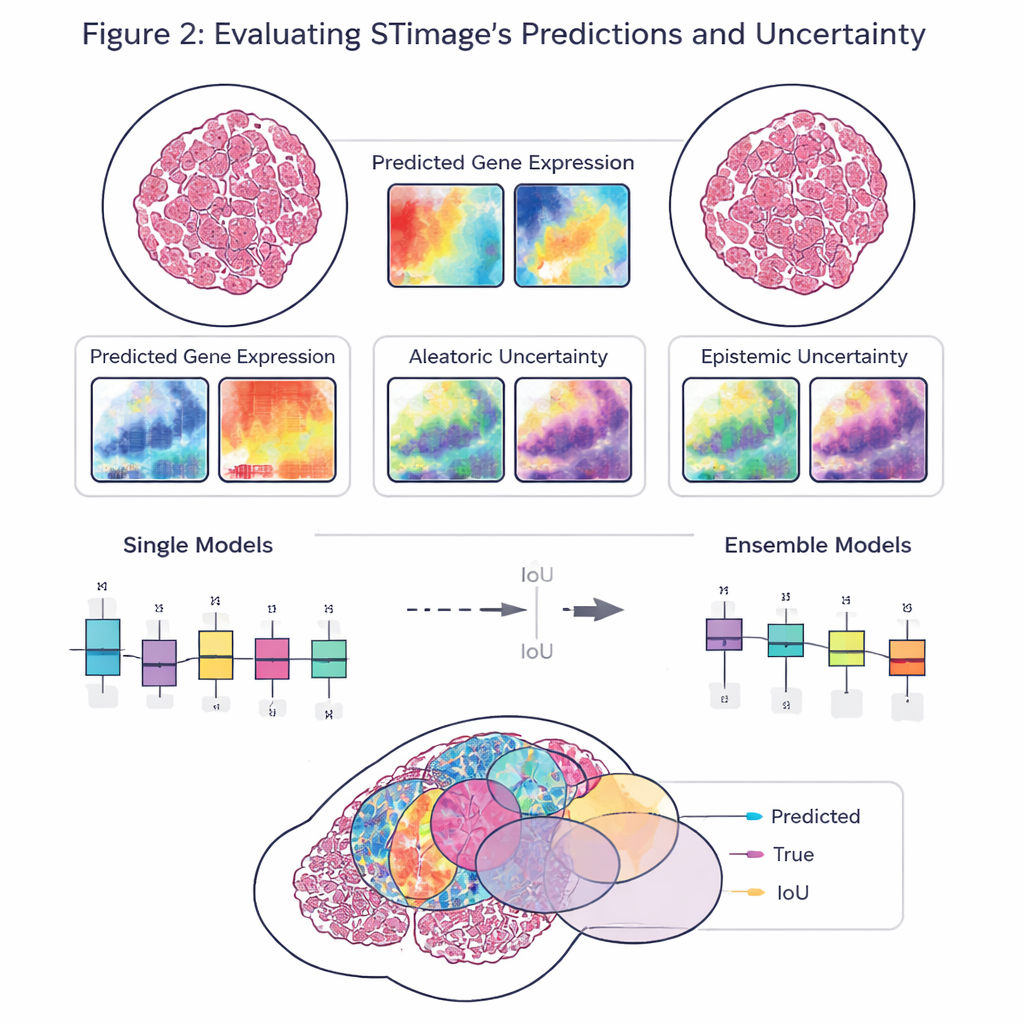
Einblick in Tumore: Zellen, Überleben und Wirkstoffantwort
STimage geht über Genvorhersagen hinaus und leitet ab, welche Zelltypen jede Region besetzen, indem es hochauflösende Datensätze nutzt, in denen die Identität jeder Zelle bekannt ist. Das Modell konnte Krebszellen von Immun- und Stützzellen unterscheiden und ihre Anordnung über einen Schnitt hinweg abbilden. Die Autoren wandten STimage anschließend auf große Sammlungen routinemäßiger Krebsbilder aus The Cancer Genome Atlas an. Selbst ohne räumliche Messungen waren die vom KI-System vorhergesagten Genprofile eng mit den realen Bulk‑Gen‑Daten korreliert. Diese Vorhersagen reichten aus, um Patienten in höhere und niedrigere Risikogruppen zu unterteilen und dabei zu helfen, solche zu identifizieren, die mit höherer Wahrscheinlichkeit vollständig auf bestimmte Brustkrebstherapien ansprechen.
Warum das für zukünftige Patientinnen und Patienten wichtig ist
Für Patientinnen, Patienten und Kliniker ist das Versprechen von STimage eine Art „molekularer Überzug“ auf dem vertrauten Pathologieschnitt. Statt mehrere teure Tests zu veranlassen, könnte eines Tages ein einziges eingescanntes Bild offenbaren, wo aggressive Genprogramme aktiv sind, wie Immunzellen verteilt sind und welche Marker auf bessere oder schlechtere Verläufe beziehungsweise auf unterschiedliche Wirkstoffantworten hinweisen. Obwohl die Methode noch verfeinert wird und die Korrelation mit tatsächlichen Messungen nicht perfekt ist, macht ihre Fähigkeit, räumliche Muster zu erfassen, ihre eigene Unsicherheit abzuschätzen und hervorzuheben, welche Zellen ihre Vorhersagen antreiben, sie zu einem praktischen Schritt in Richtung informativerer, transparenterer digitaler Pathologie.
Zitation: Tan, X., Mulay, O., Xie, J. et al. Robust and interpretable prediction of gene markers and cell types from spatial transcriptomics data. Nat Commun 17, 1781 (2026). https://doi.org/10.1038/s41467-026-68487-0
Schlüsselwörter: digitale Pathologie, spatiale Transkriptomik, Krebs-Biomarker, Deep Learning, Tumormikroumgebung