Clear Sky Science · de
PTRAMP, CSS und Ripr bilden einen konservierten Komplex, der für die Invasion von Merozoiten verschiedener Plasmodium‑Arten in Erythrozyten erforderlich ist
Warum das für den Kampf gegen Malaria wichtig ist
Malaria‑Parasiten müssen in unsere roten Blutkörperchen eindringen, um Krankheit zu verursachen. Diese Studie deckt eine kleine Gruppe von Proteinen auf, die eine gemeinsame „Einstiegsbrücke“ bilden, die von mehreren wichtigen Malaria‑Arten genutzt wird, einschließlich solcher, die den Menschen befallen. Indem sie zeigt, wie diese Brücke gebaut wird und wie Antikörper sie zum Teil blockieren können, weist die Arbeit auf neue Ansätze zur Entwicklung von Impfstoffen hin, die gegen mehr als eine Malaria‑Art gleichzeitig schützen könnten. 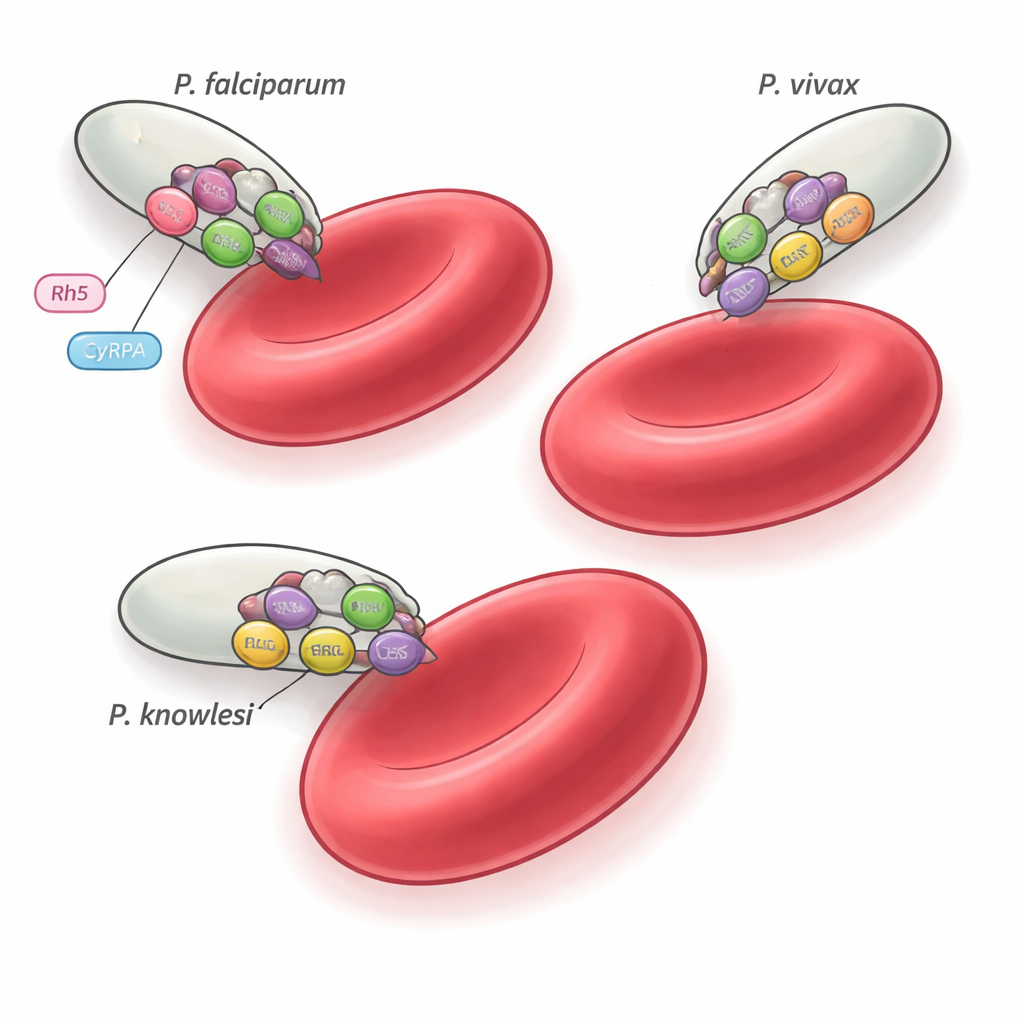
Ein gemeinsames Werkzeugset bei vielen Malaria‑Parasiten
Es gibt mehr als 200 Plasmodium‑Arten, doch nur einige wenige, etwa P. falciparum, P. vivax und P. knowlesi, infizieren Menschen. Diese Arten liegen auf unterschiedlichen Zweigen des Parasiten‑Stammbaums und bevorzugen unterschiedliche Typen von roten Blutkörperchen, müssen aber alle Erythrozyten mit großer Präzision invasieren. Frühere Arbeiten an P. falciparum identifizierten einen fünfteiligen Verbund, den PCRCR‑Komplex, der für die Invasion essentiell ist und an einen menschlichen Erythrozyten‑Rezeptor namens Basigin bindet. Ein Baustein dieses Komplexes, ein Protein namens Rh5, ist nur in P. falciparum und seinen nahen Verwandten vorhanden, was die Frage aufwirft: Was verwenden andere Malaria‑Arten stattdessen? Die vorliegende Studie konzentriert sich auf drei Begleitproteine — PTRAMP, CSS und Ripr — die im gesamten Genus konserviert sind, und prüft, ob sie eine universelle Invasionsmaschine bilden.
Aufbau einer dreiteiligen Invasionsbrücke
Mithilfe von Sequenzsuchen über viele Parasiten‑Genome zeigen die Autor:innen, dass PTRAMP, CSS und Ripr in allen wichtigen Plasmodium‑Linien vorhanden sind, im Gegensatz zu Rh5, das auf eine Untergruppe beschränkt ist. Strukturvorhersagen mit AlphaFold, kombiniert mit detaillierten biochemischen Messungen, zeigen, dass PTRAMP und CSS ein stabiles Paar bilden, das durch eine spezifische Disulfidbindung zwischen zwei konservierten Cysteinresten zusammengehalten wird. Diese Zwei‑Protein‑Plattform klemmt dann an das C‑Terminus von Ripr und bildet so einen dreiteiligen PTRAMP–CSS–Ripr (PCR)‑Komplex. Experimente mit Proteinen aus P. falciparum, P. vivax und P. knowlesi zeigen, dass sich dieser Komplex in allen drei Arten mit hoher Affinität bildet und dass nur eine kleine Region am C‑terminalen Ende von Ripr für die enge Bindung nötig ist. 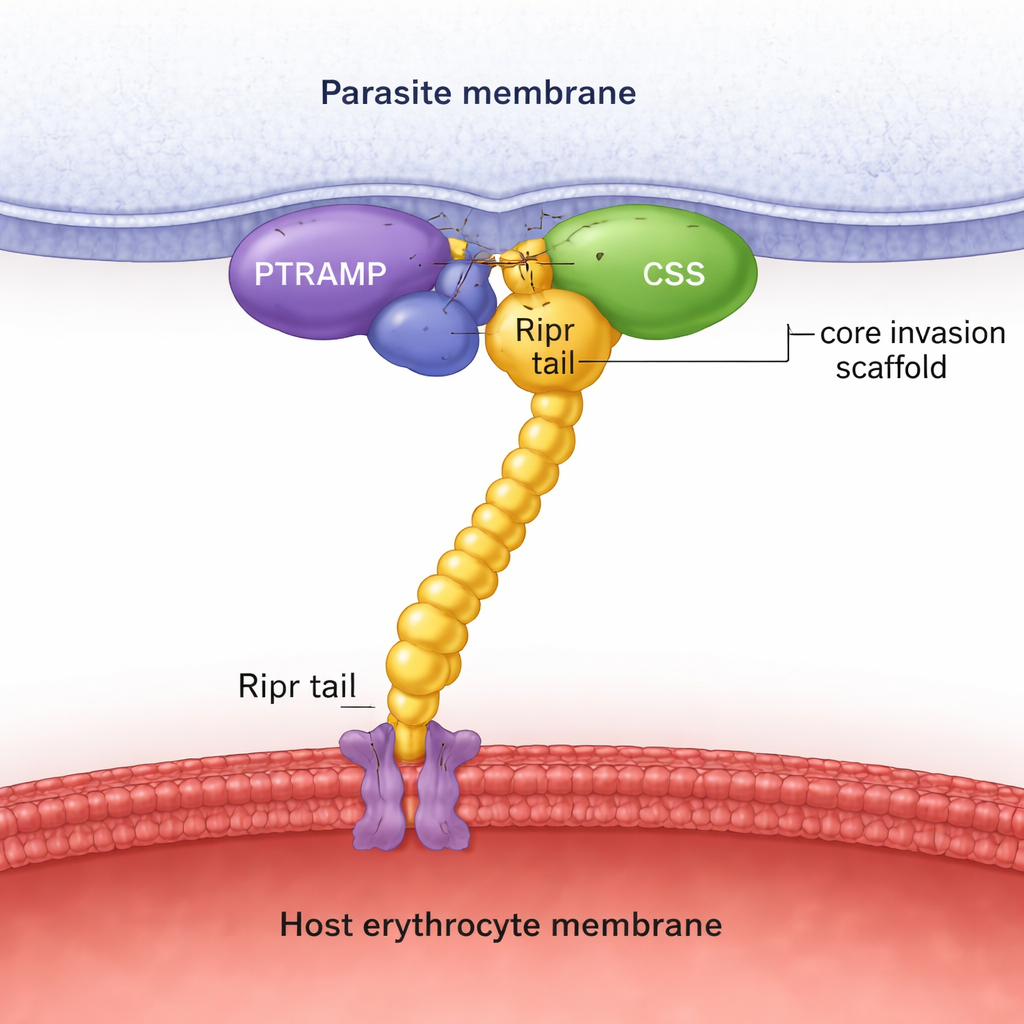
Die Struktur in atomarer Detailliertheit sehen
Um über Vorhersagen hinauszugehen, löste das Team Kristallstrukturen und sammelte Kryo‑Elektronenmikroskopie‑Bilder. Die Kristallstruktur des P. vivax PTRAMP–CSS‑Paars zeigt genau, wie ein kurzer Abschnitt von PTRAMP über CSS verläuft und die entscheidende Disulfidverbindung bildet. Eine andere Struktur fängt einen wirksamen Antikörper gebunden an zwei von Riprs wachstumsfaktorähnlichen Domänen ein und kartiert ein inhibitorisches Epitop am Ripr‑Ende. Die Kryo‑EM‑Analyse des P. knowlesi PCR‑Komplexes bestätigt die von AlphaFold vorhergesagte Gesamtgestalt: PTRAMP und CSS liegen nahe an der Parasitenmembran und umgreifen Ripr, dessen länglicher Körper sich in Richtung Wirtszelle erstreckt. Zusammen stützen diese strukturellen Momentaufnahmen die Idee, dass das PCR‑Trio ein starres Gerüst bildet, das während der Invasion physikalisch die Lücke zwischen Parasit und Erythrozyt überspannt.
Antikörper, die mehr als eine Art erkennen
Weil diese Proteine konserviert sind, untersuchten die Autor:innen, ob menschliche Infektionen natürlicherweise Antikörper hervorrufen, die zwischen Arten kreuzreagieren. Plasma von Patient:innen, die mit P. falciparum, P. vivax oder P. knowlesi infiziert waren, zeigte starke Antikörperreaktionen gegen CSS und Ripr aus mehreren Arten, was darauf hindeutet, dass Menschen Antikörper gegen gemeinsame Regionen des PCR‑Komplexes entwickeln. Das Team erzeugte dann monoklonale Antikörper und Nanobodies gegen P. vivax PTRAMP, CSS und Ripr und prüfte, ob diese das Parasitenwachstum in Kultur hemmen können. Einige Antikörper, insbesondere einer mit der Bezeichnung 5B3, die an Riprs Schwanz bindet, konnten die Invasion durch P. knowlesi und in höheren Konzentrationen durch P. falciparum hemmen. Überraschenderweise stoppten dieselben Antikörper P. vivax oder den eng verwandten Affenparasiten P. cynomolgi nicht, obwohl sie die Proteine dieser Arten binden konnten.
Ein geteiltes Gerüst mit artspezifischen Aufsätzen
Funktionelle Tests zeigen, dass der PCR‑Komplex selbst nicht direkt rote Blutkörperchen ergreift; vielmehr dient er wahrscheinlich als konserviertes strukturelles Gerüst, an das jede Art ihre eigenen rezeptorbindenden Partner ankoppelt. In P. falciparum beispielsweise arbeitet das PCR‑Trio mit CyRPA und Rh5 zusammen, um Basigin auf menschlichen Erythrozyten anzusprechen. Bei P. vivax und P. knowlesi sind die entsprechenden rezeptorbindenden Proteine und Wirtsziele noch unbekannt, doch derselbe PTRAMP–CSS–Ripr‑Kern scheint die Invasionsmaschinerie zu organisieren. Dass einige Antikörper kreuzreagieren, aber nur bestimmte Arten hemmen, unterstreicht, wie subtile Unterschiede in der Komplexassemblierung und im Timing die Anfälligkeit für die Immunabwehr verändern können.
Was das für künftige Malaria‑Impfstoffe bedeutet
Für Nicht‑Spezialist:innen lautet die Kernbotschaft: Malaria‑Parasiten sehr unterschiedlicher Arten teilen einen gemeinsamen „Stecker“, den sie zum Eindringen in rote Blutkörperchen verwenden — bestehend aus den Proteinen PTRAMP, CSS und Ripr — auch wenn sie diesen Stecker an unterschiedliche Rezeptoren auf der Zelloberfläche anschließen. Dieser konservierte Stecker ist nun strukturell kartiert und kann in einigen Fällen durch Antikörper getroffen werden, die artsübergreifend wirken. Zwar sind weitere Arbeiten nötig, um das vollständige Set an Partnerproteinen zu identifizieren und inhibitorische Antikörper zu verbessern, doch die Entdeckung eines universellen Invasionsgerüsts eröffnet Wege für Impfdesigns, die gegen mehrere Malaria‑Formen zugleich schützen könnten, statt nur gegen eine einzige.
Zitation: Seager, B.A., Lim, P.S., Xiao, X. et al. PTRAMP, CSS and Ripr form a conserved complex required for merozoite invasion of Plasmodium species into erythrocytes. Nat Commun 17, 1780 (2026). https://doi.org/10.1038/s41467-026-68486-1
Schlüsselwörter: Malaria‑Invasion, Plasmodium‑Proteine, Merozoiten‑Einstieg, artenübergreifender Impfstoff, Erythrozyteninfektion