Clear Sky Science · de
Cryo-Elektronen-Tomographie zeigt gekoppelte Flavivirus-Replikation, Abschnürung und Reifung
Wie gehirninfizierende Viren Zellmembranen kapern
Flaviviren, eine große Gruppe von Viren, zu der unter anderem die Erreger von Dengue-Fieber und der Frühsommer-Meningoenzephalitis gehören, können ins Gehirn eindringen und schwere Erkrankungen verursachen. Wie genau sich diese winzigen Krankheitserreger jedoch in unseren Zellen kopieren und neue Viruspartikel zusammenbauen, blieb weitgehend verborgen. In dieser Studie werden hochauflösende 3D-Elektronenaufnahmen bei kryogenen Temperaturen eingesetzt, um tickenübertragene Flaviviren in menschlichen Zellen und in Mausgewebe des Gehirns bei der Arbeit zu beobachten. Die Aufnahmen zeigen eine unerwartet enge Kopplung zwischen Genomkopie, Virusassemblierung und Virusreifung.
Versteckte Virusfabriken in Zellmembranen
Flaviviren schwimmen bei der Replikation nicht einfach frei in der Zelle. Stattdessen remodeln sie ein zelluläres Membransystem, das endoplasmatische Retikulum (ER), und bilden dort spezialisierte Taschen, die als Replikationsorganellen bezeichnet werden. Diese sehen aus wie winzige einwärts gerichtete Knospen auf der ER-Oberfläche und dienen als geschützte Kammern, in denen virale RNA-Genome kopiert werden. Mithilfe der Kryo-Elektronen-Tomographie, einer Technik, die 3D-Schnappschüsse von blitzgefrorenen Zellen in nahezu nativen Zustand erzeugt, visualisierten die Forscher diese Knospen in menschlichen Lungenzellen, die mit einem tickenübertragenen Flavivirus verwandt mit dem FSME-Virus infiziert waren. Sie stellten fest, dass das ER in infizierten Bereichen anschwillt und mit Clustern dieser Replikationsorganellen gefüllt ist, von denen einige leer sind, andere jedoch dichte, fadenförmige RNA enthalten.
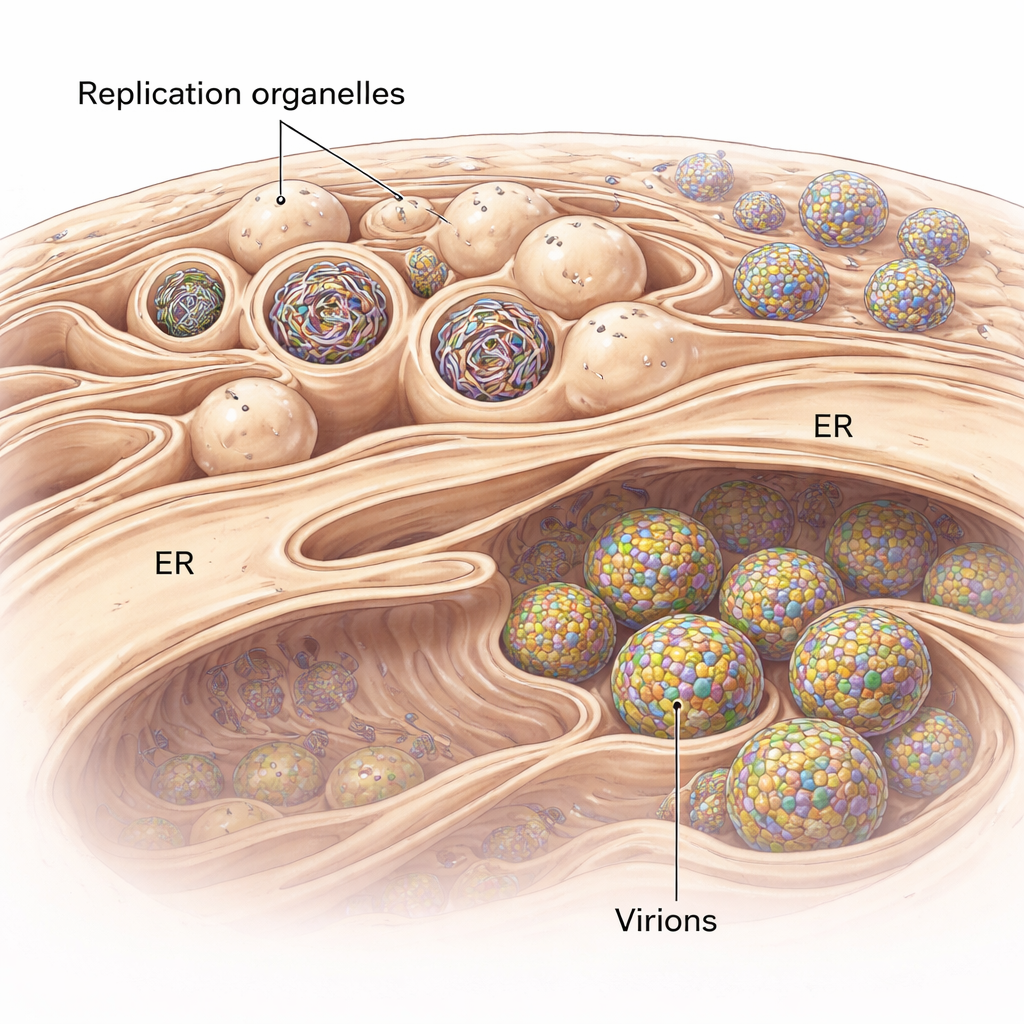
Aufbau der perfekten viralen Blase
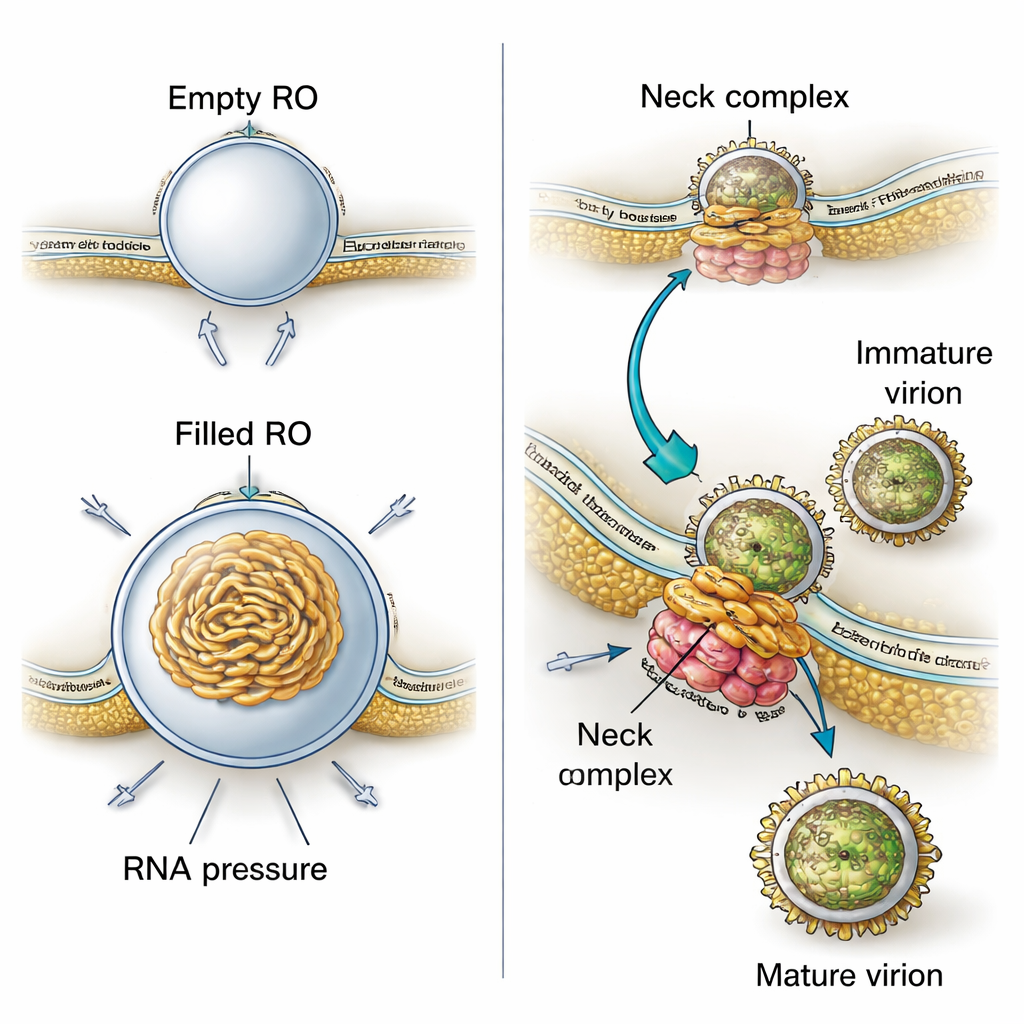
Warum haben diese Membrantaschen eine so präzise, knospenartige Form? Durch die Kombination ihrer 3D-Bilder mit physikalischer Modellierung zeigen die Autoren, dass zwei Kräfte zusammenwirken. Erstens ist die Membran der Replikationsorganellen durchgängig dicker als normales ER, was darauf hindeutet, dass virale Proteine oder veränderte Lipide die Membran versteifen und krümmen, sodass schon vor dem Einströmen von RNA eine stabile Knospe entsteht. Zweitens wickelt sich die virale RNA, wenn sie vorhanden ist, im Inneren der Tasche auf und drückt nach außen, wodurch die Knospe größer wird. Berechnungen auf Grundlage der gemessenen Größen deuten darauf hin, dass jede gefüllte Organelle wahrscheinlich einen Druck enthält, der von ungefähr einer Kopie des viralen Genoms in doppelsträngiger Form herrührt. Das bedeutet, dass das Virus sowohl eine vorgeformte Membran als auch den physikalischen Druck seines eigenen genetischen Materials nutzt, um seine winzigen Fabriken zu bauen und zu stabilisieren.
Fließband: Von der Genomkopie zu neuen Viren
Die Studie enthüllt außerdem, wie eng die Virusproduktion an diese Replikationsorte gekoppelt ist. In ihren 3D-Aufnahmen beobachteten die Forscher häufig, dass neue Viruspartikel direkt neben Replikationsorganellen entstehen und in benachbarte ER-ähnliche Räume abschnüren. Unreife Partikel zeigten eine stachelige Oberfläche, während reifere glatt erschienen. Messungen in den Tomogrammen ergaben, dass unreife Partikel näher an den Replikationsorganellen liegen als reife, was darauf hindeutet, dass die Partikel beim kurzen Durchgang durch verflochtene Membrankompartimente die strukturellen Veränderungen durchlaufen, die nötig sind, um infektiös zu werden. Eine große Proteinanordnung an der engen „Halsstelle“, wo jede Replikationsknospe mit dem Zytoplasma verbunden ist, scheint das Replikationsorganell an einer benachbarten Membran zu verankern, an der das Abschnüren stattfindet. Dieser Komplex wirkt wahrscheinlich wie ein molekularer Reißverschluss, der die RNA-Produktion mit der Verpackung dieser RNA in neue Viruspartikel koordiniert.
Maturation feinjustiert durch eine einzelne Aminosäure
Um zu untersuchen, wie die Virusreifung gesteuert wird, verglich das Team zwei Versionen eines chimären Virus, die sich nur durch eine Aminosäure an einer Stelle unterscheiden, die von einem Wirtsenzym namens Furin erkannt wird. Dieses Enzym schneidet ein virales Oberflächenprotein und hilft so, unreife stachelige Partikel in glatte reife zu verwandeln. In Test-Rohr-Spaltungsassays und in infizierten Zellen wurde die Variante mit Arginin an dieser Position schneller geschnitten als die Variante mit Glutamin. Bei der Beobachtung in Zellen mittels Kryo-Elektronen-Tomographie produzierte das schneller geschnittene Virus einen höheren Anteil reifer Partikel in der Nähe der Replikationsorganellen. Trotz dieser mikroskopischen Unterschiede zeigten beide Varianten im Mausmodell ähnliche Wachstums- und Krankheitsverläufe, was darauf hindeutet, dass das Virus eine Bandbreite an Reifungseffizienzen tolerieren kann und dennoch infektiös bleibt.
Infektion direkt im Gehirn beobachten
Die meisten Strukturstudien von Viren basieren auf Zelllinien, doch diese Arbeit geht weiter und umfasst lebendes Gewebe. Die Forscher isolierten aus infizierten Mäusen eine Hirnstruktur, das Plexus choroideus, und bereiteten es für die Kryo-Elektronen-Tomographie mittels Hochdruckgefrierens und fokussierter Ionenstrahl-Bearbeitung vor. Selbst in dieser komplexen Umgebung beobachteten sie die gleichen charakteristischen Merkmale: Cluster von Replikationsorganellen, verdickte Membranen und nahegelegene Vesikel, die mit reifen Viruspartikeln gefüllt sind. Das zeigt, dass das Membran-Remodelling und die eng gekoppelte Abfolge von Replikation–Assemblierung–Reifung, wie sie in kultivierten Zellen beobachtet wurden, auch im Gehirn stattfinden, wo diese Viren Krankheit verursachen.
Warum diese verborgenen Abläufe wichtig sind
Für Nicht-Fachleute ist die zentrale Botschaft, dass diese gehirninfizierenden Viren in unseren Zellen eine hochorganisierte Produktionslinie betreiben. Sie formen Zellmembranen zu winzigen, unter Druck stehenden Blasen, in denen Genome kopiert werden, verbinden diese Blasen direkt mit den Stellen, an denen neue Partikel abschnüren, und beginnen sogar die letzten Reifungsschritte in unmittelbarer Nähe des ursprünglichen Replikationsorts. Die Identifizierung der verdickten Replikationsmembranen, des halsüberspannenden Proteinkomplexes und der eng verflochtenen Reifungskompartimente erklärt nicht nur, wie Flaviviren so effizient replizieren, sondern weist auch auf neue Ziele für antivirale Wirkstoffe hin, die die verborgenen Fabriken und Montagewege des Virus stören sollen.
Zitation: Dahmane, S., Schexnaydre, E., Zhang, J. et al. Cryo-electron tomography reveals coupled flavivirus replication, budding and maturation. Nat Commun 17, 828 (2026). https://doi.org/10.1038/s41467-026-68483-4
Schlüsselwörter: Flavivirus, Cryo-Elektronen-Tomographie, Replikationsorganellen, Virusreifung, Frühsommer-Meningoenzephalitis