Clear Sky Science · de
Spektroelektrochemische Einblicke in Kupfer-Kobalt-Katalysatoren für die gemeinsame Elektroreduzierung von CO2 und Nitrit zu Harnstoff
Abfallgase in Dünger verwandeln
Harnstoffdünger ist eine Grundlage der modernen Landwirtschaft, aber seine konventionelle Herstellung ist energieintensiv und CO2-lastig. Diese Studie untersucht einen ganz anderen Ansatz: Elektrizität zu nutzen, um Kohlendioxid (CO2) und stickstoffhaltige Abfälle (etwa Nitrit aus Abgasen oder Abwasser) direkt in Harnstoff umzuwandeln. Für eine breite Leserschaft ist der Reiz offensichtlich: ein Weg zu lebenswichtigem Dünger, der Emissionen senken, Abfallströme als Rohstoffe nutzen und eines Tages mit erneuerbarem Strom betrieben werden könnte.
Warum die Harnstoffproduktion neu denken?
Heute wird Harnstoff überwiegend hergestellt, indem zuerst Ammoniak aus Stickstoff und fossilem Wasserstoff (Haber–Bosch-Verfahren) erzeugt wird und dieses Ammoniak dann bei hohen Temperaturen und Drücken mit CO2 umgesetzt wird. Diese Prozesskette ist zentralisiert, kapitalintensiv und setzt pro Tonne Harnstoff nahezu eine Tonne CO2 frei. Mit wachsender globaler Düngemittelnachfrage steigen auch die Umweltkosten. Eine Alternative besteht darin, fossile Brennstoffe ganz zu umgehen, die Schlüsselreaktionen elektrisch—idealerweise mit erneuerbarem Strom—anzutreiben und CO2 sowie Stickstoffoxide (NOx), die derzeit als Abfall gelten, als Ausgangsstoffe zu nutzen.
Eine neue Rolle für Kupfer und Kobalt
Die Autoren entwickeln Dünnschichtkatalysatoren, die durch Co-Sputtern von Kupfer (Cu) und Kobalt (Co) auf Kohlepapier hergestellt werden, und stimmen das Cu:Co-Verhältnis sorgfältig ab. Sie konzentrieren sich auf die gleichzeitige elektrochemische Reduktion von CO2 und Nitrit (NO2⁻) in Wasser bei neutralem pH-Wert—ein Umfeld, das die feine Bildung von Kohlenstoff–Stickstoff-(C–N)-Bindungen fördern kann, die für Harnstoff nötig sind. Die herausragende Zusammensetzung ist ein 1:1-Gemisch aus Cu und Co, das bei moderater angelegter Spannung eine Harnstoffproduktionsrate von etwa 61 Millimol pro Stunde und Gramm Katalysator erreicht. Mikroskopie- und Röntgenmessungen zeigen, dass sich die Metalle auf atomarer Skala eng mischen und während des Betriebs größtenteils metallisch bleiben, wodurch eine robuste Plattform entsteht, auf der sowohl CO2 als auch Nitrit effizient reagieren können. 
Wie der Katalysator Arbeit aufteilt
Harnstoff auf diesem Weg herzustellen ist schwierig, weil einfachere Reaktionen—etwa die Wasserstoffentwicklung oder die alleinige Reduktion von CO2 bzw. Nitrit—stark konkurrieren. Die Schlüsselidee, so die Forschenden, ist eine Arbeitsteilung zwischen Kupfer- und Kobaltatomen, die zusammenwirken. Elektrochemische Tests zeigen, dass Kupfer allein hauptsächlich CO2 in kohlenstoffbasierte Brennstoffe und Chemikalien umwandelt, während Kobalt allein Nitrit überwiegend zu Ammoniak reduziert, ohne Harnstoff zu bilden. Erst wenn Cu- und Co-Atome eng vermischt sind, tritt nennenswerter Harnstoff auf. Spektrale „Schnappschüsse“, die während der Reaktion aufgenommen wurden, detektieren charakteristische oberflächengebundene Fragmente: Kohlenstoffspezies aus CO2 (*CO und *COOH), die Kupfer bevorzugen, und Stickstoffspezies aus Nitrit (*NH2 und verwandte Gruppen), die Kobalt bevorzugen. An den Grenzflächen zwischen Cu und Co können diese Fragmente zusammentreffen und koppeln, um das C–N-Rückgrat des Harnstoffs zu bilden.
Die richtigen Bedingungen für die Bindungsbildung finden
Die Studie zeigt, dass die Zusammensetzung allein nicht ausreicht; auch das umgebende Lösungsmittel und die Membran müssen abgestimmt werden. Harnstoff erscheint nur in einem neutralen Bikarbonat-Elektrolyten, der genügend gelöstes CO2 verfügbar hält und genau die richtige Menge an Protonen (Wasserstoffionen) liefert, um „protongekoppelte Elektronentransfer“-Schritte zu ermöglichen, ohne die Oberfläche durch übermäßige Wasserstoffentwicklung zu überwältigen. Unter stark sauren oder stark alkalischen Bedingungen bildet sich Harnstoff entweder nicht oder zerfällt schnell zu einfacheren Produkten. Experimente mit verschiedenen Stickstoffquellen zeigen, dass Nitrit besonders effektiv für die Harnstoffbildung ist und Nitrat sowie Hydroxylamin übertrifft. Langzeittests über viele Stunden deuten darauf hin, dass die Cu–Co-Filme relativ stabil sind, mit nur mäßigem Metallverlust und anhaltender Harnstoffproduktion.
Mit Theorie unter die Haube schauen
Um zu verstehen, warum dieser Tandemkatalysator so gut funktioniert, wendet sich das Team Computersimulationen auf Basis der Dichtefunktionaltheorie zu. Diese Rechnungen stützen die Vorstellung, dass Kupfer die Anlagerung CO2-abgeleiteter Spezies begünstigt, während Kobalt Nitrit besser aktiviert und stickstoffhaltige Fragmente stabilisiert. Die Simulationen identifizieren einen bestimmten Schritt als energetischen Engpass: die Kopplung eines *NH2-Fragments (aus Nitrit) mit einem *COOH-Fragment (aus CO2) zur Bildung eines Intermediats, das manchmal als *NH2CO geschrieben wird. Ist dieses Stück einmal geschaffen, sind die verbleibenden Schritte zu Harnstoff vergleichsweise einfach. Die Cu–Co-Grenzfläche senkt die Energiekosten dieses entscheidenden Kopplungsschritts im Vergleich zu reinem Kupfer oder reinem Kobalt und erklärt damit den experimentell beobachteten Anstieg der Harnstoffausbeute beim bimetallischen System. 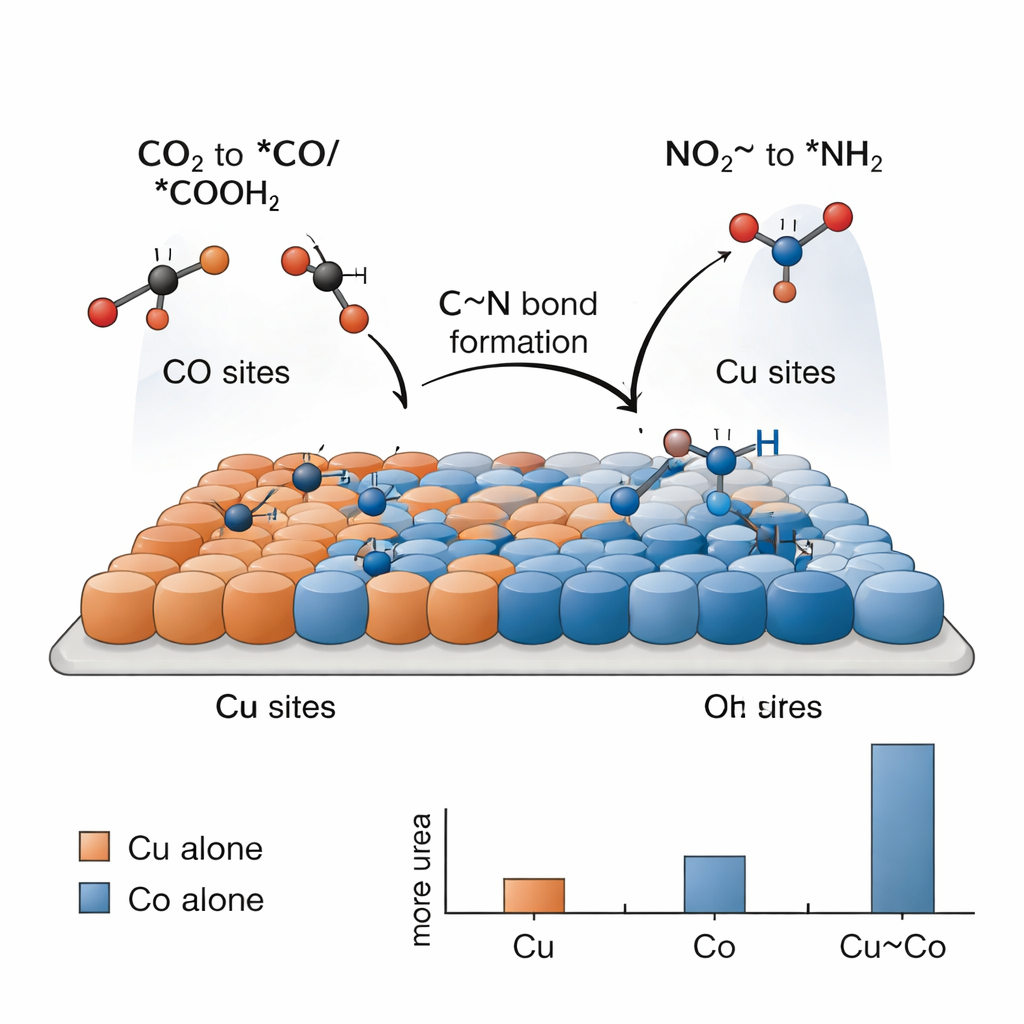
Vom Laborbefund zu nachhaltigerem Dünger
Praktisch betrachtet ersetzt diese Arbeit noch nicht die heutigen gigantischen Harnstoffwerke, aber sie macht deutlich, wie eine künftige elektrochemische Route gestaltet werden könnte. Indem gezeigt wird, dass Kupfer und Kobalt im Tandem arbeiten können—das eine liefert aktivierte Kohlenstoffspezies, das andere aktivierte Stickstoffspezies, beide unter sorgfältig kontrollierten Protonenbedingungen—zeichnet die Studie einen realistischen Pfad zu einer saubereren, potenziell dezentralen Harnstoffproduktion nach, die CO2 und Stickstoffabfälle als Ressourcen statt als Schadstoffe nutzt.
Zitation: Ramadhany, P., Trần-Phú, T., Yuwono, J.A. et al. Spectroelectrochemical insight into copper cobalt catalysts for CO2 and nitrite co-electroreduction to urea. Nat Commun 17, 1776 (2026). https://doi.org/10.1038/s41467-026-68481-6
Schlüsselwörter: elektrochemische Harnstoffsynthese, Kupfer-Kobalt-Katalysator, CO2-Nutzung, Nitritreduktion, C–N-Kupplung