Clear Sky Science · de
Strukturelle Grundlage für die selektive Hemmung des menschlichen GABA‑Transporters GAT3
Warum beruhigende Gehirnsignale wichtig sind
Unser Gehirn beruht auf einem empfindlichen Gleichgewicht zwischen Signalen, die erregen, und solchen, die beruhigen. Ein wichtiger beruhigender Botenstoff ist GABA, ein Molekül, das hilft, außer Kontrolle geratene Aktivität zu verhindern, die mit Erkrankungen wie Epilepsie, Schlaganfallschäden und Alzheimer in Verbindung steht. Diese Studie konzentriert sich auf ein Protein namens GAT3, das GABA aus der Umgebung von Nervenzellen entfernt. Indem die Forschenden im atomaren Detail zeigen, wie ein neues Molekül an GAT3 bindet und es ausschaltet, liefern sie eine strukturelle Landkarte für die Entwicklung der nächsten Medikamentengeneration, die das natürliche Bremssystem des Gehirns schonend verstärken könnte.
Das eigene Bremspedal des Gehirns
GABA ist der Hauptinhibitor bzw. der hauptsächliche beruhigende Neurotransmitter im zentralen Nervensystem. Nachdem GABA aus Nervenendigungen freigesetzt wurde, muss es schnell entfernt werden, damit sich Hirnschaltkreise zurücksetzen können. Diese Säuberung übernehmen Transporterproteine, die GABA wieder in Zellen pumpen. Zwei dieser Transporter dominieren im Gehirn: GAT1, das überwiegend auf Neuronen vorkommt, und GAT3, das auf Stützzellen namens Astrozyten sitzt. Während ein GAT1‑blockierendes Medikament (Tiagabin) seit Jahrzehnten zur Behandlung von Epilepsie eingesetzt wird, hinken vergleichbare Wirkstoffe, die GAT3 anvisieren, hinterher. GAT3 ist jedoch besonders interessant, weil es GABA‑Spiegel außerhalb von Synapsen kontrolliert und lang anhaltende, background‑artige Hemmung formt, die die Gehirnaktivität fein abstimmen kann. 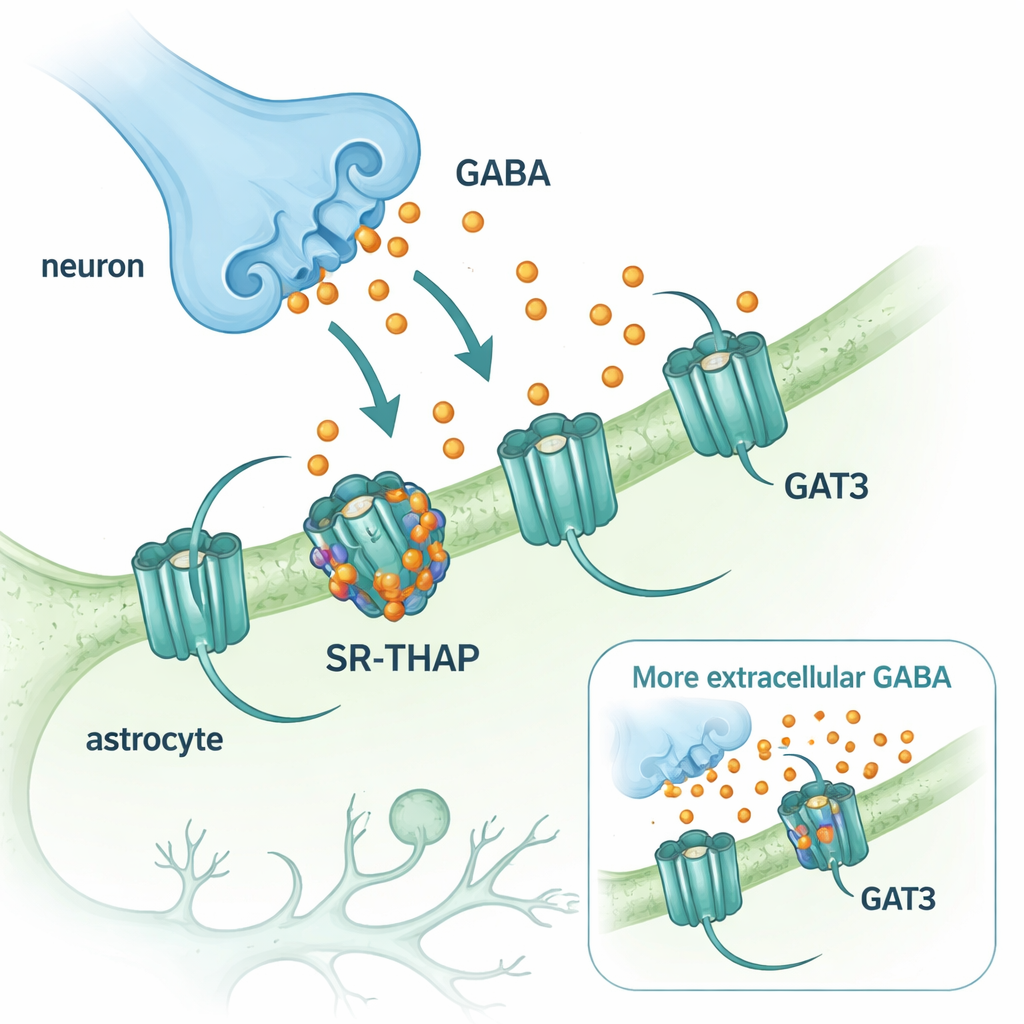
Entwurf eines präziseren molekularen Schlosses
Versuche, GAT3 zu hemmen, wurden durch das Fehlen detaillierter struktureller Informationen erschwert. Viele frühere Verbindungen entstanden durch Trial‑and‑Error, häufig durch das Anfügen sperriger Variationen bekannter GABA‑ähnlicher Moleküle. Eine der bekanntesten, (S)‑SNAP‑5114, erwies sich als chemisch instabil und schwierig in lebenden Tieren zu verwenden. Aufbauend auf einem stabileren Verwandten dieser Verbindung entwickelten die Autorinnen und Autoren SR‑THAP, ein neues kleines Molekül, das so gestaltet ist, dass es besser in GAT3 passt und widerstandsfähiger gegen Abbau ist. Experimente in humanen Zellkulturen zeigten, dass SR‑THAP GAT3 stark blockiert und dies auf nicht‑kompetitive Weise tut: Statt einfach mit GABA an der üblichen Bindestelle zu konkurrieren, verändert es die Funktionsweise des Transporters und reduziert dessen maximale Transportkapazität.
GAT3 in nahezu atomarer Auflösung sehen
Um genau zu verstehen, wie SR‑THAP wirkt, wandte sich das Team der Kryo‑Elektronenmikroskopie zu, einer Technik, die schockgefrorene Proteine mit Elektronen abbildet und ihre dreidimensionale Gestalt rekonstruiert. Sie lösten drei Varianten des menschlichen GAT3: gebunden an SR‑THAP, gebunden an GABA und in einem substratfreien Zustand. Alle drei zeigen die typische Architektur verwandter Neurotransporter: 12 dicht gepackte Helices, die die Membran durchspannen und einen zentralen Weg für GABA und die zugehörigen Ionen Natrium und Chlorid bilden. In der GABA‑gebundenen Struktur befindet sich der Transporter in einem „inward‑occluded“ Zustand – GABA und ein Natriumion sind in der Mitte eingespannt und sowohl von außen als auch von innen abgeriegelt. Eine wichtige aromatische Aminosäure bildet eine spezialisierte Wechselwirkung mit der Aminogruppe von GABA, was erklärt, wie GAT3 sein Substrat erkennt.
Wie SR‑THAP den Transporter aufschiebt
Im auffälligen Gegensatz dazu fängt die SR‑THAP‑gebundene Struktur GAT3 in einem „inward‑open“ Zustand ein, wobei die innere Seite des Proteins zur Zellinnenseite aufklafft. SR‑THAP liegt tief in dieser inneren Höhlung, verkeilt zwischen mehreren Helices, die normalerweise während des Transportzyklus bewegt werden. Es besetzt drei kleine Taschen mit unterschiedlichen chemischen Charakteren und geht ein Netzwerk von Wasserstoffbrücken und hydrophoben Kontakten ein. Diese Positionierung verklemmt den Transporter so, dass GABA und Ionen ihre Reise nicht mehr vollenden können. Die Autorinnen und Autoren zeigen, dass einige spezifische Aminosäuren, die diese Höhlung auskleiden, zwischen GAT3 und seinen nahen Verwandten variieren; der Austausch einer dieser Aminosäurereste verändert sowohl die Transportaktivität als auch die Wirksamkeit von SR‑THAP und erklärt, warum der Inhibitor deutlich selektiver für GAT3 ist als für GAT1 oder verwandte Transporter. 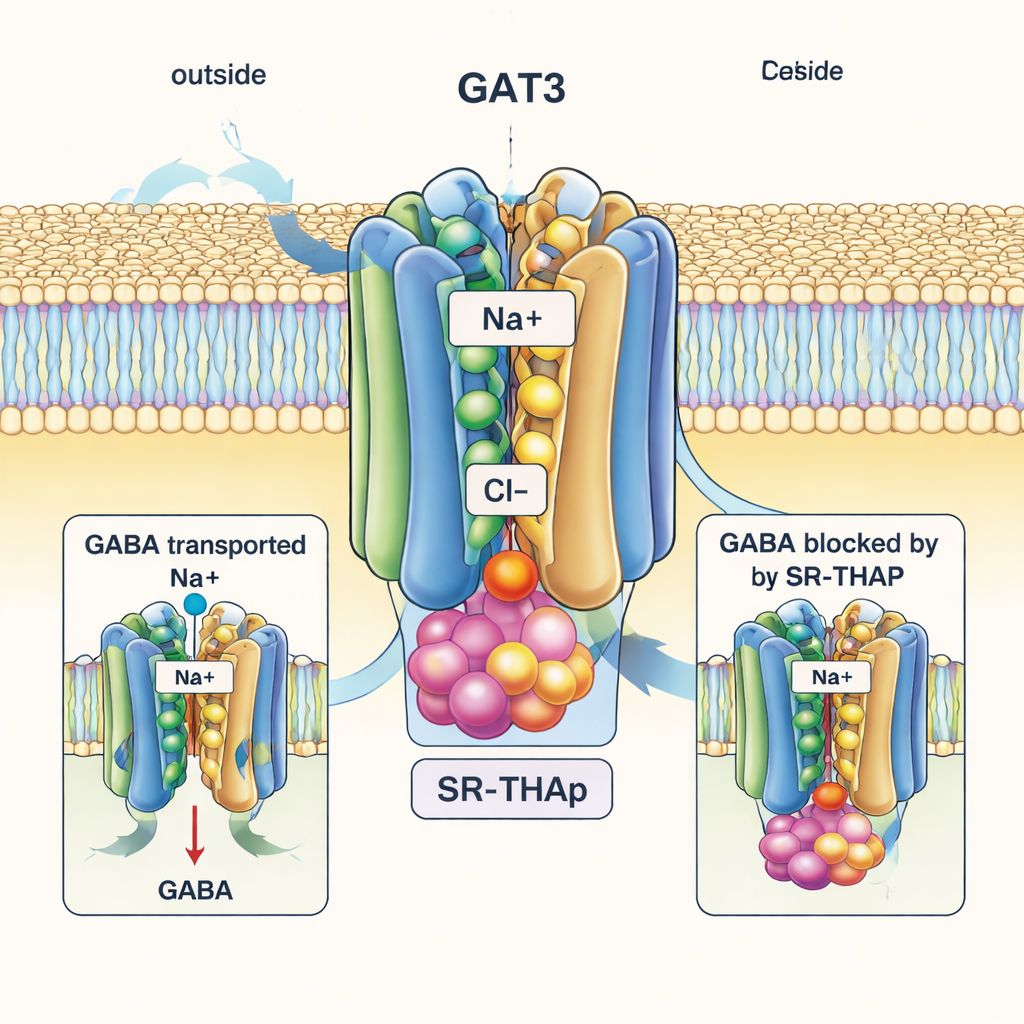
Türen öffnen sich für neue Epilepsie‑ und Gehirngesundheitsmedikamente
Zusammen zeigen diese Strukturen, wie GAT3 zwischen verschiedenen Formen wechselt, um GABA zu transportieren, und wie SR‑THAP eine weniger konservierte innere Tasche ausnutzt, um diesen Zyklus einzufrieren. Für Nicht‑Spezialisten lautet die zentrale Schlussfolgerung, dass die Studie einen detaillierten molekularen Plan liefert, um GAT3 auf hochselektive Weise auszuschalten. Solche Verbindungen könnten beruhigendes GABA feiner erhöhen als bestehende Arzneimittel und damit zu neuen Behandlungen oder Forschungstools für Epilepsie, Schlaganfall‑Erholung, Alzheimer‑Krankheit und andere Zustände führen, bei denen die inhibitorische Signalübertragung gestört ist.
Zitation: Mortensen, J.S., Bavo, F., Jensen, M.H. et al. Structural basis for selective inhibition of human GABA transporter GAT3. Nat Commun 17, 1774 (2026). https://doi.org/10.1038/s41467-026-68479-0
Schlüsselwörter: GABA‑Transporter, GAT3, Epilepsie, Cryo‑EM, Neurotransmitter‑Hemmung