Clear Sky Science · de
Ein stochastischer Mechanismus treibt die schnelle Substrattranslokation in der AAA+-Maschine ClpB
Wie zelluläre Maschinen Proteine in Bewegung halten
In jeder Zelle ziehen, schieben und formen winzige molekulare Maschinen ständig Proteine, um Zusammenlagerung zu verhindern und Schäden zu reparieren. Eine dieser Maschinen, ClpB, hilft, verhedderte Proteine zu retten – eine lebenswichtige Aufgabe unter Stressbedingungen. Diese Studie stellt eine einfache, aber grundlegende Frage: Wie wandelt ClpB den chemischen Brennstoff ATP in die mechanische Arbeit um, eine Proteinkette durch seine zentrale Pore zu ziehen, und geschieht das in wohlgeordneten, taktsynchronen Schritten oder auf eine zufälligere, diffusive Weise?
Ein Ring zur Proteinsanierung in Aktion
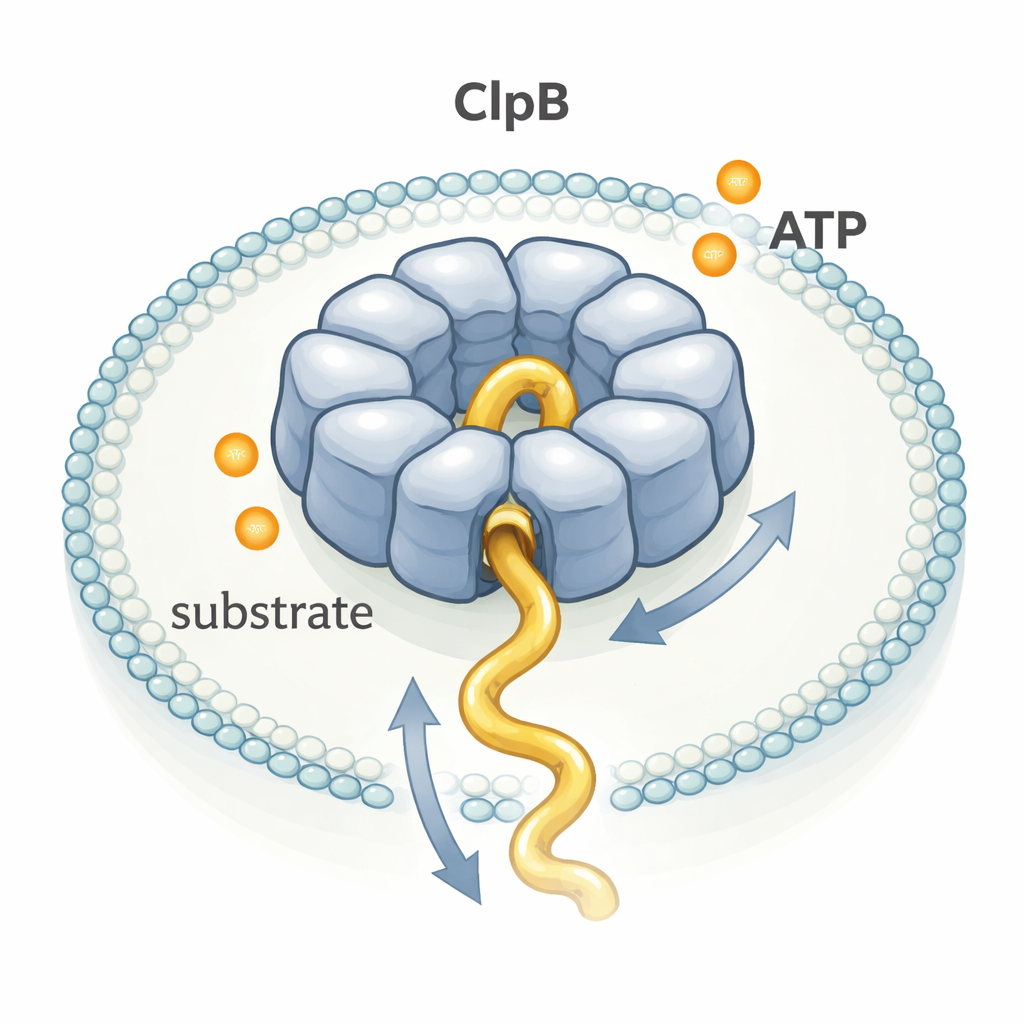
ClpB gehört zu einer großen Familie von Enzymen, den AAA+-Maschinen, die ringförmige Strukturen mit einem zentralen Tunnel bilden. Viele davon wurden mittels Kryo‑Elektronenmikroskopie in großer Detailtreue dargestellt, was ein populäres "Hand‑über‑Hand"‑Modell nahelegte: jedes verbrannte ATP würde einen kleinen, präzisen Schritt antreiben, wie ein Team, das ein Seil der Reihe nach zieht. Andere Experimente deuteten jedoch darauf hin, dass ClpB Proteine viel schneller bewegen könnte, als die langsame ATP‑Verbrauchsrate vermuten lässt. Um dieses Rätsel zu lösen, beobachteten die Autoren einzelne ClpB‑Moleküle in Echtzeit, während sie ein flexibles Testprotein, κ‑Kasein, durch ihre Pore bewegten.
Ein Molekül nach dem anderen beobachten
Die Forschenden fingen einzelne ClpB‑Ringe und einzelne κ‑Kasein‑Moleküle zusammen in winzigen Lipidbläschen ein, die auf einer Glasoberfläche befestigt waren. Sie befestigten Fluoreszenzfarbstoffe an bestimmten Punkten von ClpB und an der Proteinkette und nutzten dann Einzelmolekül‑FRET, eine Technik, die Distanzänderungen zwischen Farbstoffen auf Nanometerskala anzeigt. Wenn κ‑Kasein in die ClpB‑Pore glitt, rückten die Farbstoffe näher zusammen und der FRET‑Signal stieg als kurzer Ausschlag; wenn die Kette wieder austrat, fiel das Signal. Durch Messen der Dauer und Höhe Tausender solcher Ausschläge konnten sie ableiten, wie schnell und wie weit Segmente des Proteins durch die Pore geschoben wurden.
Schnell, schwach befeuert und nahezu temperaturunabhängig
Überraschenderweise waren die Translokationsereignisse extrem schnell: Das markierte Segment von κ‑Kasein durchquerte typischerweise mehrere Nanometer der Pore in etwa 1–2 Millisekunden – das ist etwa tausendmal schneller als die durchschnittliche Zeit zwischen ATP‑Hydrolyseereignissen in ClpB. Die meisten Ereignisse waren so kurz und folgten einer breiten Potenzgesetzverteilung statt einer einzelnen charakteristischen Zeitkonstante. Eine Temperaturänderung von 10 auf 32 °C verlangsamte diese Bewegungen kaum, was darauf hindeutet, dass die energetische Barriere für die Bewegung im Vergleich zu klassischen "Power‑Stroke"‑Motoren wie Kinesin winzig ist. Ebenso reduzierte eine Absenkung der ATP‑Konzentration die Häufigkeit der Ereignisse stark, hatte aber kaum Einfluss auf die Dauer einzelner Ereignisse. ATP steuerte demnach eher, wann ClpB sich einschaltete und wie oft es agierte, als die Geschwindigkeit einzelner Translokationsausbrüche.
Hin‑ und Herbewegung mit Vorwärtsbias
Um zu prüfen, ob Ketten immer in eine Richtung laufen, führten die Forscher komplexere Drei‑Farb‑FRET‑Experimente durch, bei denen beide Enden der Pore und das Substrat gefärbt wurden. So konnten sie unterscheiden, ob κ‑Kasein von oben oder unten in den Ring eintrat und ob es vollständig hindurchlief oder zurückzog. Sie entdeckten sechs unterschiedliche Muster: vollständiges Vorwärts‑ und Rückwärtsdurchfädeln, längere "partielle" Aufenthalte, bei denen die Kette beide Enden der Pore probte, bevor sie ging, und flüchtige Begegnungen in der Nähe nur eines Endes. Ungefähr drei Viertel der vollständigen Ereignisse liefen vorwärts, doch ein erheblicher Anteil verlief rückwärts, was zeigt, dass ClpB bidirektionale Diffusion des Substrats zulässt, allerdings mit nur moderatem Vorwärtsbias. Wenn ATP durch ein langsam hydrolysierbares Analogon ersetzt wurde, wurden die Ereignisse selten und deutlich langsamer, und die Vorzugsrichtung verschwand weitgehend.
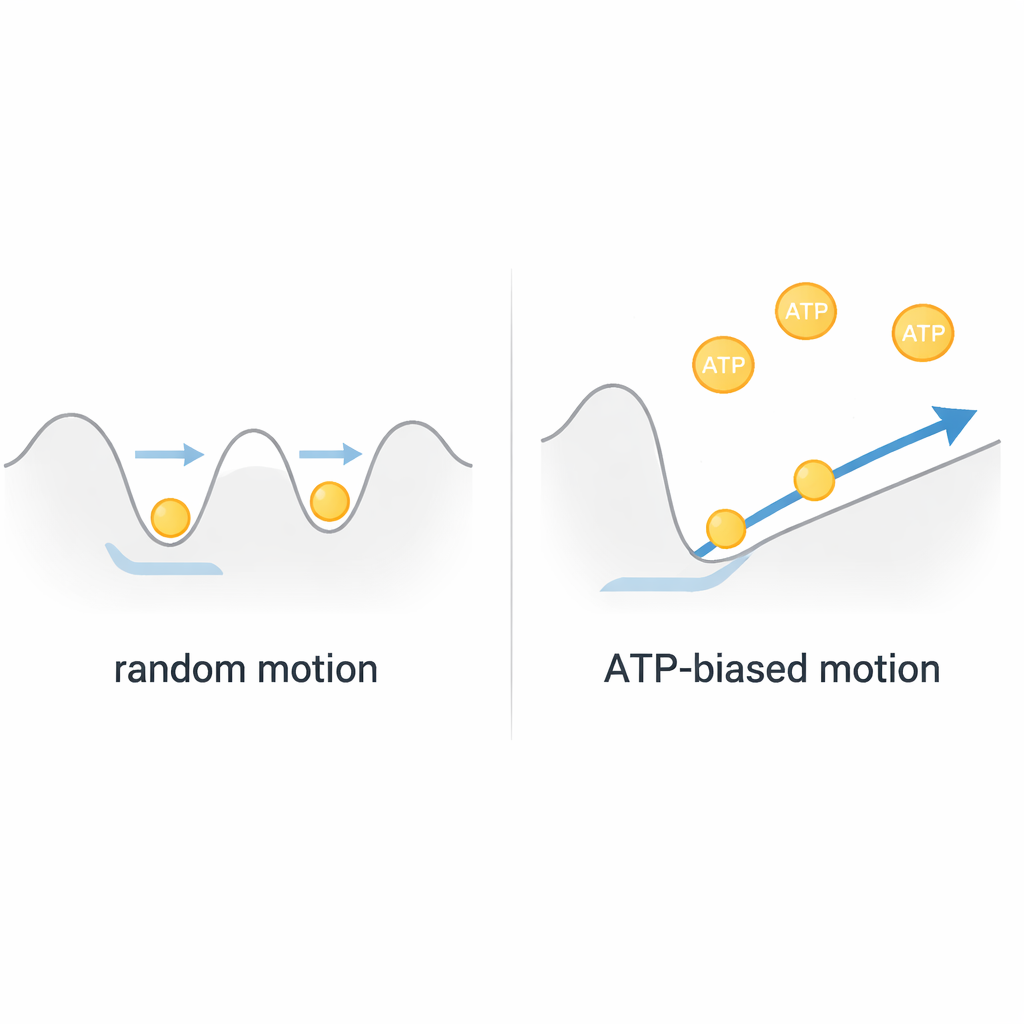
Ein Brownscher Motor, kein einfacher Flaschenzug
Setzt man diese Beobachtungen zusammen, schließen die Autoren, dass ClpB eher wie ein Brownscher Motor arbeitet als wie ein starrer, treibstoffgetriebener Flaschenzug. Die Proteinkette zappelt thermisch in einer flachen Energielandschaft innerhalb der Pore und bewegt sich schnell hin und her. ATP treibt nicht direkt große, diskrete Zugstöße an; stattdessen verändert es die Form dieser Landschaft durch schnelle Bewegungen interner "Porenschlaufen" und begünstigt so schwach die Bewegung in eine Richtung. Weil jedes vollständige Durchfädelungsereignis nur mit etwa ein bis zwei verbrauchten ATP‑Molekülen korreliert, erreicht ClpB bemerkenswert effizienten, schnellen Transport, indem es zufällige Bewegung gleichrichtet, anstatt gegen sie anzukämpfen. Diese Sichtweise verändert unser Verständnis vieler AAA+-Maschinen und legt nahe, dass biologische Nanomotoren oft Zufälligkeit nutzen, statt sie zu eliminieren.
Zitation: Casier, R., Levy, D., Riven, I. et al. A stochastic mechanism drives fast substrate translocation in the AAA+ machine ClpB. Nat Commun 17, 1773 (2026). https://doi.org/10.1038/s41467-026-68478-1
Schlüsselwörter: Proteintranslokation, AAA+-Maschine, Brownscher Motor, molekularer Chaperon, Einzelmolekül-FRET