Clear Sky Science · de
Struktur eines Brochothrix thermosphacta-Bakteriophagen enthüllt Mechanismus der Zellwandadsorption bei Gram-positiven infizierenden Siphophagen
Viren, die unsere Lebensmittel frisch halten
Bakterientötende Viren, sogenannte Bakteriophagen, prägen stillschweigend unsere Gesundheit und Lebensmittelversorgung. Manche verursachen tödliche Infektionen, andere lassen sich gezielt einsetzen, um lebensmittelübertragene Erreger und Verderb zu bekämpfen. Diese Studie zeigt in eindrücklichen atomaren Details, wie ein solcher Virus, NF5 genannt, an der robusten Außenhülle eines fleischverderbenden Bakteriums anhaftet und sie durchbohrt. Das Verständnis dieser mikroskopischen Auseinandersetzung könnte helfen, sicherere Wege zur Konservierung von Lebensmitteln und zur Bekämpfung antibiotikaresistenter Bakterien zu entwickeln.
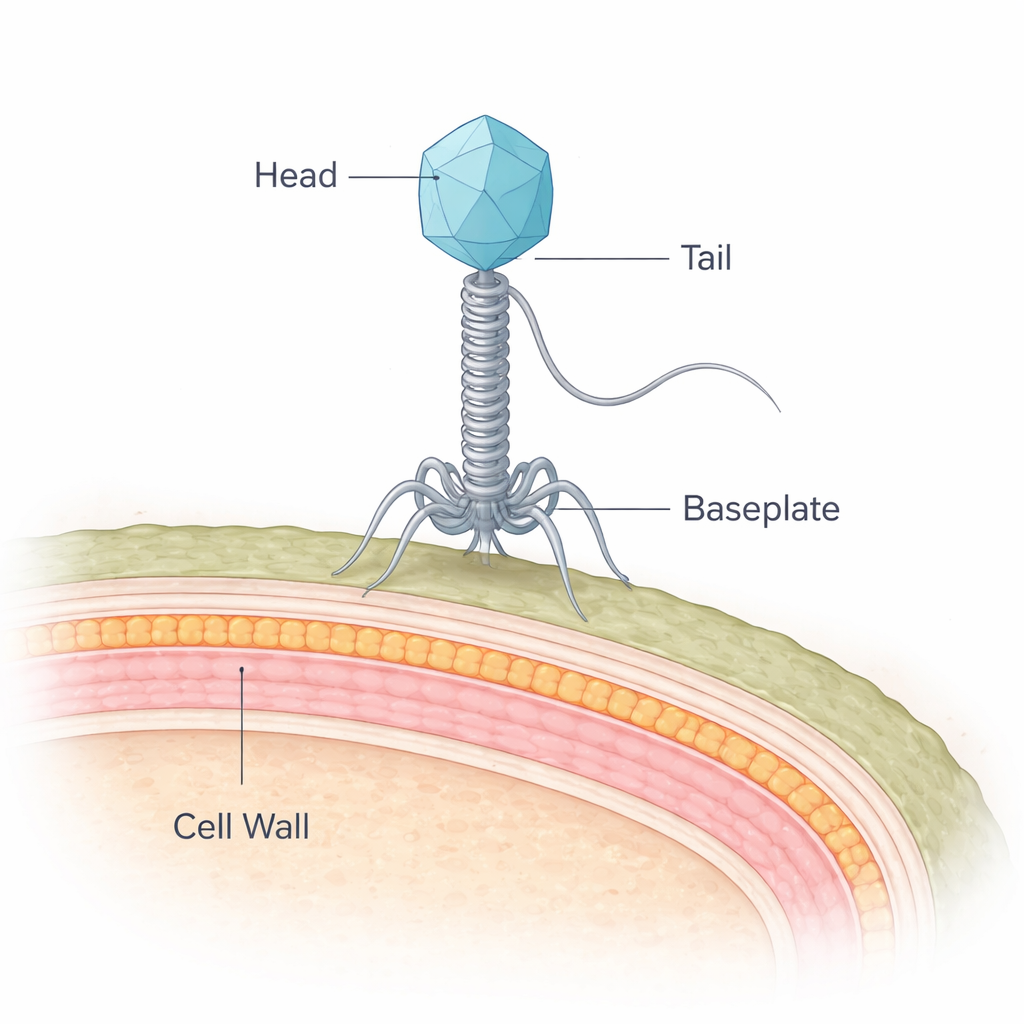
Ein Fleischverderber trifft auf seinen natürlichen Feind
Das Bakterium, um das sich diese Arbeit dreht, Brochothrix thermosphacta, ist ein häufiger Verursacher von unangenehmen Gerüchen und Schleimbildung bei gekühltem Fleisch. NF5 ist ein Virus, das dieses Bakterium befällt und zur Gruppe der Siphophagen gehört, die ihre DNA in einer Proteinhülle tragen und sie durch einen langen, flexiblen Schwanz einschleusen. Während Wissenschaftler die Strukturen vieler Viren, die sogenannte Gram-negative Bakterien infizieren, detailliert beschrieben haben, sind diejenigen, die Gram-positive Bakterien wie B. thermosphacta angreifen, weit weniger verstanden. Gram-positive Bakterien stellen ein besonderes Rätsel dar, weil sie von einer dicken, mehrschichtigen Zellwand geschützt sind, nicht von einer dünnen Wand und einer Außenmembran.
Eine molekulare Spritze, Atom für Atom aufgebaut
Mit modernster Kryo-Elektronenmikroskopie haben die Forschenden Millionen von NF5-Partikeln eingefroren und ihre dreidimensionale Struktur mit annähernd atomarer Auflösung rekonstruiert. Sie identifizierten 11 verschiedene Virusproteine, die gemeinsam Kopf, Hals, Schwanzrohr und eine aufwändige Basisplatte an der Schwanzspitze zusammenbauen — insgesamt 643 Proteinketten. Der Kopf bildet eine stabile ikosaedrische Hülle um die virale DNA, während ein 135 Nanometer langer Schwanz sich wie eine flexible Spritze nach unten erstreckt. Ringe wiederholter Proteine bilden ein hohles Schwanzrohr, dessen Innenseite stark negativ geladen ist — eine Anordnung, die vermutlich hilft, die DNA rasch in den Wirt abzuschießen.
Der intelligente Bohrer an der Schwanzspitze
Der komplizierteste Teil von NF5 ist die Basisplatte, eine mehrschichtige Struktur, die zugleich als Sensor, Bohrer und Anker fungiert. Nahe dem Zentrum sitzt ein „Maßbands“-Protein, das das Schwanzrohr füllt, sowie eine schwanzassoziierte Lysin, die das Rohr verschließt, bis die Infektion beginnt. Um diesen Kern herum befinden sich Proteine, die die bakterielle Oberfläche erkennen und greifen. Einige wirken wie federnde Arme, die sich stark biegen können und der Basisplatte helfen, zu kippen und dann in eine senkrechte Position zur Zellwand zu schnappen. Andere ähneln Fasern verwandter Viren und dürften spezifische Moleküle in der dicken Gram-positiven Wand binden und sogar Teile des zuckerreichen Netzwerks der Zellwand anknabbern. Auffallend ist, dass ein seitliches NF5-Faserprotein Funktionen kombiniert, die bei anderen Gram-positiven Viren auf mehrere Proteine verteilt sind — ein Hinweis auf ein effizientes, evolutionär gestrafftes Design.
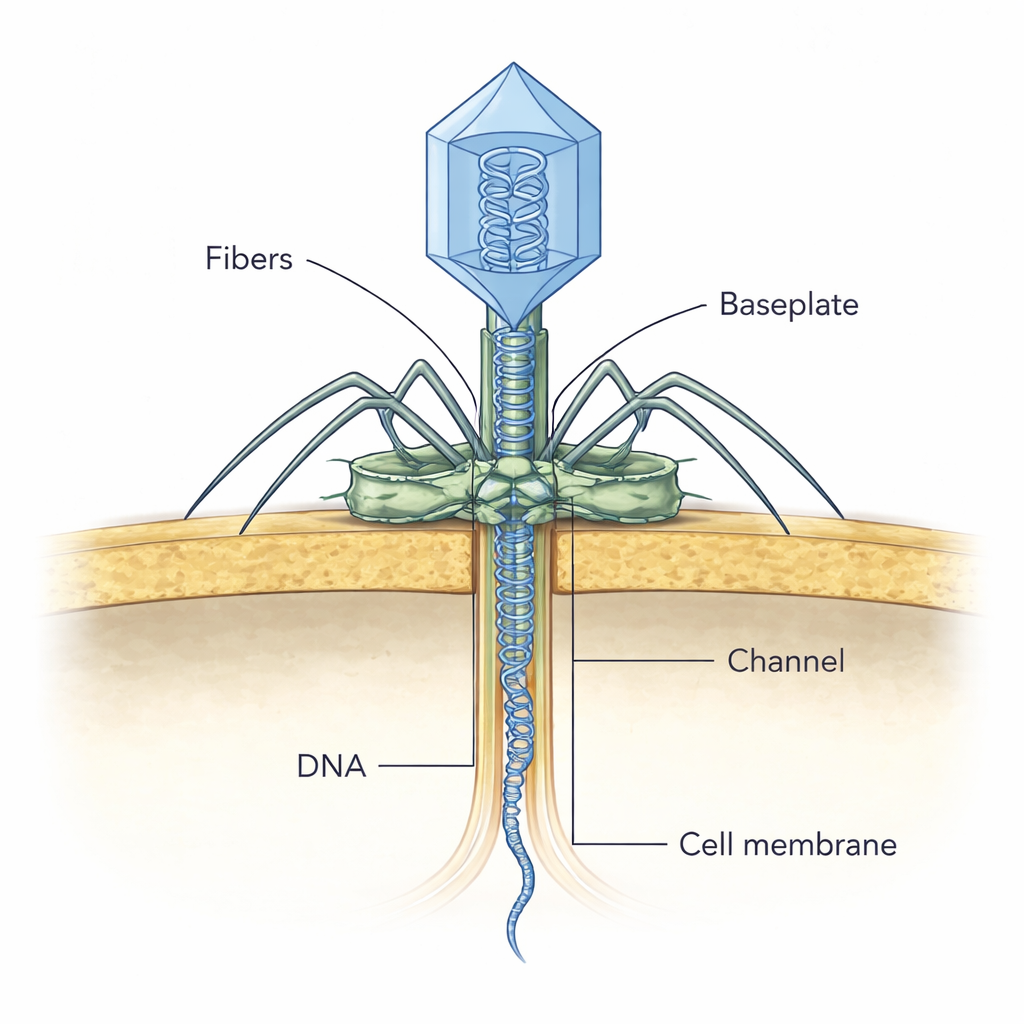
Ein Virus bei der Tat ertappt
Um zu sehen, wie diese Bauteile während der Infektion zusammenwirken, nutzte das Team Kryo-Elektronentomographie an dünnen Schnitten infizierter Bakterien. Sie fingen NF5-Partikel in unterschiedlichen scheinbaren Angriffsphasen ein. In frühen Aufnahmen haftet das Virus in einem Winkel an der Zellwand, wahrscheinlich indem es seine äußeren Fasern zur Auffindung geeigneter Rezeptoren einsetzt. Später richtet sich die Basisplatte senkrecht zur Zelloberfläche aus, und der noch angeheftete Viruskopf scheint weiterhin DNA zu enthalten. In nachfolgenden Stadien verliert der Kopf sein Innenleben, wenn die DNA freigesetzt wird, und eine dünne, kanalartige Dichte erscheint, die durch die bakterielle Wand in Richtung Zellmembran verläuft. Die Autorinnen und Autoren schlagen vor, dass sobald das Enzym an der Schwanzspitze die Zellwand kontaktiert und verdaut, es sich umordnet, den Verschluss öffnet und es dem Maßbandsprotein erlaubt, herauszugleiten und diesen temporären Tunnel zu bilden, durch den die virale DNA sicher in die Zelle gelangt.
Warum das über ein einzelnes Virus hinaus wichtig ist
Im Vergleich von NF5 mit Viren, die andere Bakterien infizieren, zeigen die Forschenden, dass sich zentrale Schwanz- und Basisplattenproteine bei Gram-positiven gegenüber Gram-negativen Phagen unterschiedlich entwickelt haben, um mit den sehr verschiedenen Oberflächenarchitekturen ihrer Wirte fertigzuwerden. Diese strukturellen Anpassungen — zusätzliche Domänen, längere Arme oder kombinierte Funktionen in einzelnen Proteinen — erscheinen als fein abgestimmte Reaktionen auf dickere, komplexere Zellwände. Die Arbeit liefert einen detaillierten Bauplan dafür, wie ein Virus eine harte bakterielle Barriere erkennen, anhaften und durchbrechen kann, und legt damit die Grundlage für das Engineering von Phagen oder phageninspirierten Werkzeugen zur besseren Kontrolle von Lebensmittelverderb und möglicherweise zur Bekämpfung schädlicher Gram-positiver Krankheitserreger.
Zitation: Peng, Y., Pang, H., Zheng, J. et al. Structure of a Brochothrix thermosphacta bacteriophage reveals cell wall adsorption mechanism in Gram-positive infecting siphophages. Nat Commun 17, 1772 (2026). https://doi.org/10.1038/s41467-026-68477-2
Schlüsselwörter: Struktur von Bakteriophagen, Gram-positive Bakterien, Cryo-Elektronenmikroskopie, Kontrolle von Lebensmittelverderb, Phagen-Infektionsmechanismus