Clear Sky Science · de
Identifizierung thermotoleranter nicht-kanonischer PAMs für zuverlässige One-Pot-CRISPR-Cas12a-Detektion
DNA-Tests auf Temperatur bringen
Schnelle, präzise Tests für Infektionen und genetische Veränderungen sind in der Medizin entscheidend, doch heutige DNA-Tests erfordern oft komplexe Laborgeräte und können seltene oder subtile Zielsequenzen übersehen. Diese Studie zeigt, dass das einfache Erhöhen der Temperatur eines CRISPR-basierten Tests viele zusätzliche nützliche DNA‑„Griffe“ freilegt und Ein-Röhrchen-Diagnostik schneller, empfindlicher und in der Lage macht, selbst Einzelbuchstabenunterschiede im genetischen Code zu unterscheiden. 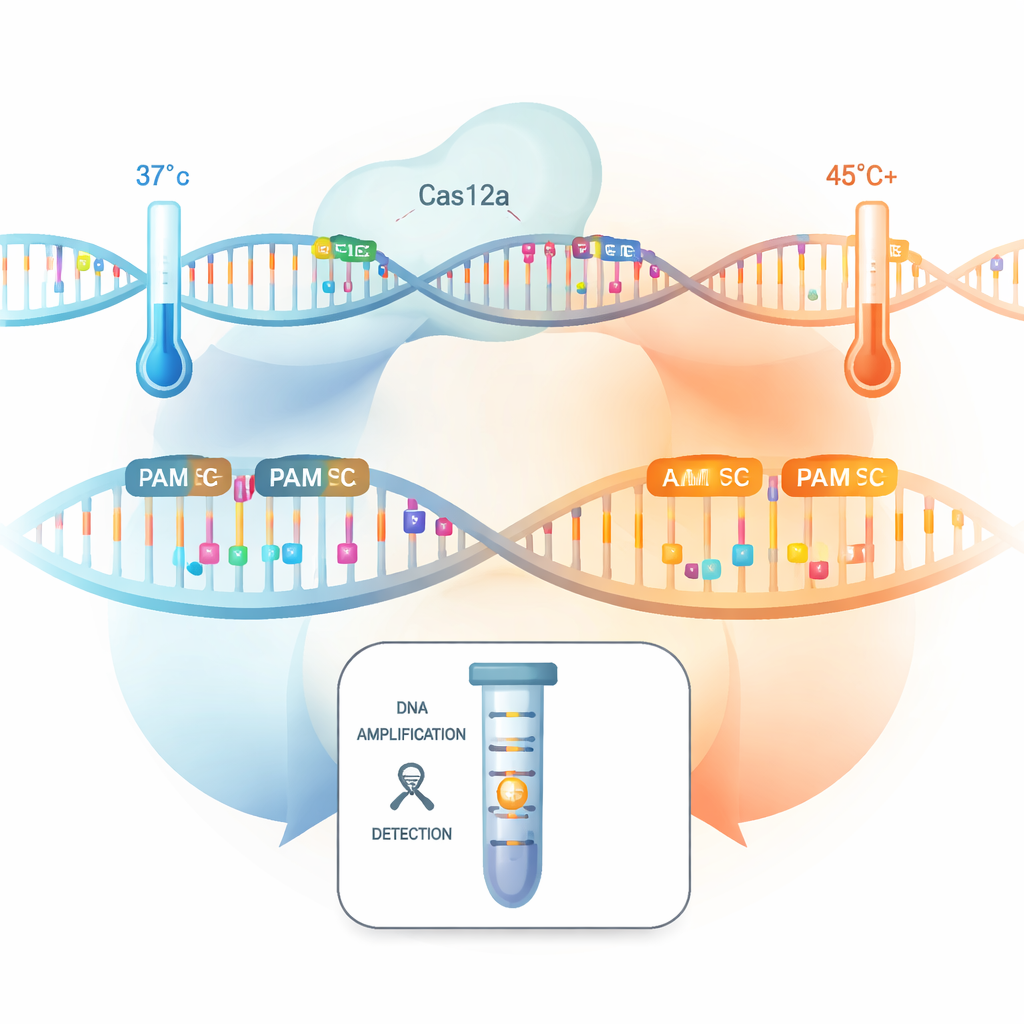
Warum CRISPR eine genaue Adresse braucht
CRISPR-Werkzeuge wie Cas12a finden spezifische DNA-Abschnitte, gesteuert von einer kurzen RNA, die wie eine Suchzeichenfolge wirkt. Sie können sich jedoch nur anlagern und aktiv werden, wenn in der Nähe ein vierbasiger Tag—ein sogenannter PAM—die richtige Sequenz aufweist; klassischerweise ist das ein enger Satz, der mit „TTT“ beginnt. Das ist wie das Bedürfnis nach einer Hausnummer, bevor ein Brief zugestellt werden kann: Fehlt die richtige Nummer, kommt die Nachricht nicht an. Diese PAM-Anforderung begrenzt die Stellen, an denen CRISPR suchen kann, ein ernstes Problem, wenn Ärzte bestimmte Mutationen, Resistenzmarker oder Virusvarianten nachweisen müssen, die nicht neben diesen klassischen Tags liegen.
Neue „Eingänge“ bei höheren Temperaturen entdecken
Die Forschenden testeten systematisch alle 256 möglichen vierbasigen PAM-Kombinationen, um zu untersuchen, wie gut sie Cas12as „kollaterale“ Schneideaktivität antreiben—also seine Fähigkeit, nach Zielerkennung viele benachbarte DNA-Stränge zu zerschneiden, was die Grundlage für CRISPR-Diagnosesignale ist. Bei normaler Körpertemperatur (37 °C) erzielten nur wenige nicht‑standardmäßige PAMs eine vergleichbare Leistung wie die klassischen. Als sie die Reaktion jedoch auf etwa 45 °C erhöhten, geschah etwas Auffälliges: 82 verschiedene nicht-kanonische PAMs erzeugten plötzlich starke Signal-Schneideaktivität und erreichten damit das Niveau der Standard‑Tags. Die Autor:innen vermuten, dass die erhöhte Wärme die lokale DNA-Struktur lockert und den Cas12a-Komplex flexibler macht, wodurch die Hürde sinkt, diese zuvor „schwachen“ PAMs zu erkennen.
Starke Signale, schonend zum Template
Cas12a besitzt zwei Schneidemodi. Im „cis“-Modus schneidet es das spezifische DNA-Stück, das es erkennen soll; im „trans“-Modus zerkleinert es nach Aktivierung rasch beliebige nahegelegene signalführende Stränge, was den Test aufleuchten lässt. Die Forschenden stellten fest, dass bei höheren Temperaturen nicht-kanonische PAMs sehr starke trans‑Schneideaktivität erzeugten—ideal für ein helles, schnelles Signal—während das cis‑Schneiden des Haupt-DNA-Templates relativ schwach blieb. Diese Kombination ist für One‑Pot-Tests optimal, bei denen die DNA zunächst vervielfältigt werden muss, ohne zerstört zu werden. Sie zeigten außerdem, dass Cas12a unter diesen wärmeren Bedingungen deutlich wählerischer gegenüber Fehlpaarungen zwischen Guide‑RNA und Ziel ist: Schon ein einzelner falscher Buchstabe kann das Signal abschalten, insbesondere bei Verwendung nicht‑kanonischer PAMs. 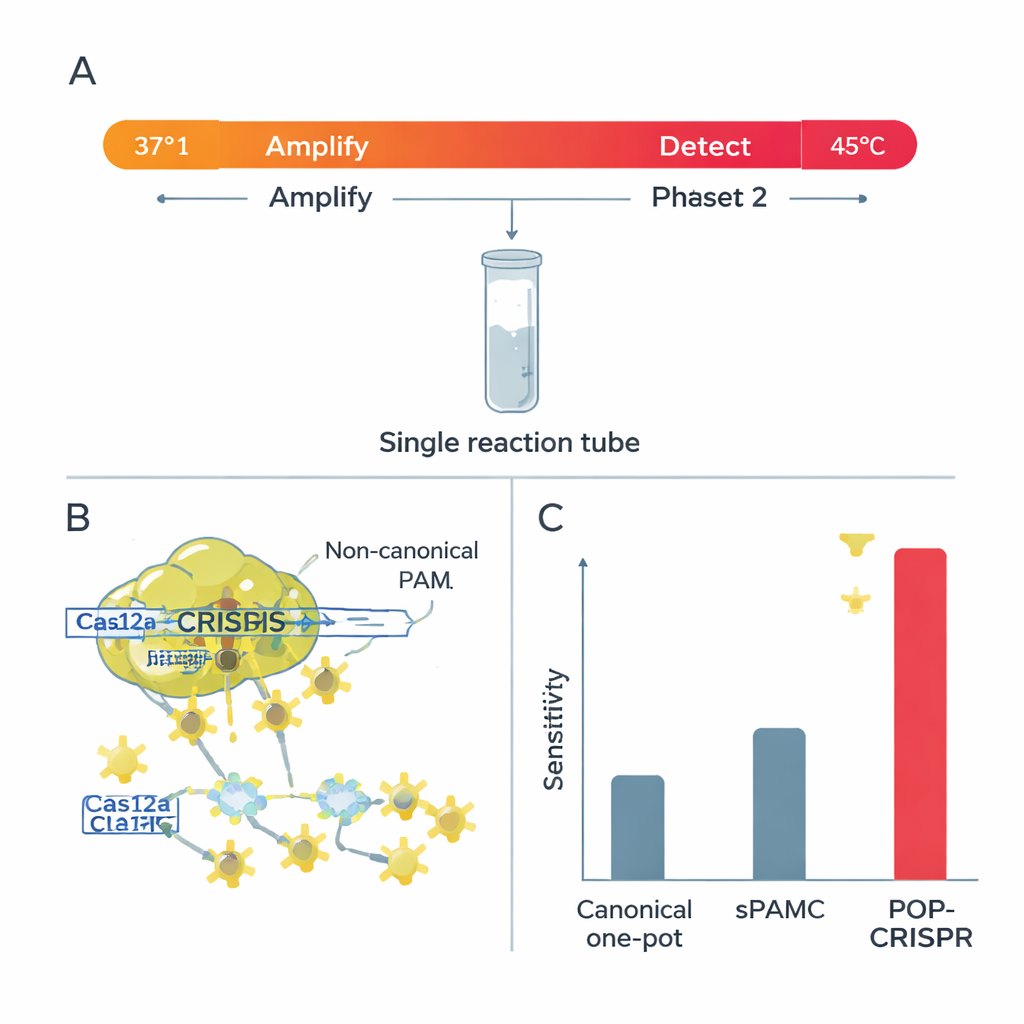
Ein schlauerer One-Pot-Test: POP-CRISPR
Auf Basis dieser Erkenntnisse entwickelten die Autor:innen POP-CRISPR, ein „poikilothermes“ (variabel temperiertes) One‑Pot‑Assay. Die Reaktion startet bei rund 37 °C, wo eine isotherme Amplifikationsmethode unauffällig jede Ziel‑DNA oder -RNA vervielfältigt, während Cas12a relativ inaktiv bleibt. Nach etwa 10 Minuten wird die Mischung auf circa 45 °C erwärmt, ein Bereich, in dem Cas12a—nun zu nicht-kanonischen PAM‑Stellen geführt—starke trans‑Aktivität zeigt und ein intensives Fluoreszenzsignal erzeugt. Dieses einfache zweistufige Temperaturprogramm steigerte die Nachweisempfindlichkeit um etwa das Zehnfache gegenüber früheren One‑Pot‑CRISPR‑Methoden, die ebenfalls schwächere PAMs nutzten, und übertraf deutlich konventionelle One‑Pot‑Formate mit kanonischen PAMs.
Vom Labor zur Praxis in Minuten
Das POP-CRISPR-System wurde an klinischen Proben getestet. Es detektierte sensitiv humanes Papillomvirus (HPV‑16) in Vaginalabstrichen und Mycoplasma pneumoniae in Rachenabstrichen, einschließlich sehr niedrig konzentrierter „Grauzonen“-Fälle, die Standardverfahren herausfordern. Entscheidenderweise konnte POP-CRISPR Mycoplasma‑Stämme mit einzelner Basenänderung in einem ribosomalen Gen unterscheiden—auch wenn in der Nähe dieser Mutation kein klassischer PAM lag—eine Aufgabe, die viele bestehende Cas12a‑Tests scheitern lässt. Um den Ansatz feldtauglich zu machen, kombinierten die Autor:innen einen schnellen zweiminütigen Heat‑and‑Chelex‑Lyseschritt (statt vollständiger DNA‑Extraktion) mit einem handflächengroßen Fluoreszenzleser, der über ein Smartphone gesteuert wird. Zusammen kann dieser Workflow einen Rohabstrich in etwa 20 Minuten in ein digitales Ja/Nein‑Ergebnis verwandeln.
Was das für den Alltagstest bedeutet
Durch die Erhöhung der Reaktionstemperatur und die Nutzung einer viel breiteren Palette von PAM‑„Eingängen“ wird Cas12a zu einem flexibleren und präziseren Sensor. POP-CRISPR liefert schnelleren, empfindlicheren und spezifischeren Nukleinsäure‑Nachweis in einer einzigen geschlossenen Röhre und erweitert zugleich die Bandbreite genetischer Stellen, die anvisiert werden können—einschließlich einzelner Basenmutationen, die mit Medikamentenresistenz oder Krebs assoziiert sind. Für Patient:innen kann das schnellere Vor-Ort‑Diagnosen und besser angepasste Therapien bedeuten; für Forschende und Testentwickler bietet es eine kraftvolle neue Möglichkeit, CRISPR‑Diagnostika robuster und diskriminierender zu gestalten.
Zitation: Tian, T., Zhang, T., Zhang, W. et al. Identification of thermotolerant non-canonical PAMs for robust one-pot CRISPR-Cas12a detection. Nat Commun 17, 1771 (2026). https://doi.org/10.1038/s41467-026-68476-3
Schlüsselwörter: CRISPR-Diagnostik, Cas12a, PAM-Stellen, Point-of-Care-Tests, Nukleinsäure-Nachweis