Clear Sky Science · de
Strukturelle Mechanismen für Hemmung und Aktivierung des menschlichen kleinleitfähigen Ca2+-aktivierten Kaliumkanals SK2
Warum winzige Kaliumkanäle wichtig sind
Jeder Gedanke und jeder Herzschlag beruht auf elektrischen Signalen in Ihren Zellen. Diese Signale werden von winzigen Poren, sogenannten Ionenkanälen, geformt, die geladene Teilchen hinein- und herausströmen lassen. Eine dieser Familien, die kleinleitfähigen calciumaktivierten Kaliumkanäle (SK-Kanäle), trägt dazu bei, wie Nervenzellen feuern und wie das Herz seinen Rhythmus hält. Diese Arbeit zeigt auf atomarer Ebene, wie verschiedene Wirkstoffe und ein Bienengift ein wichtiges Mitglied dieser Familie, den menschlichen SK2-Kanal, abschalten oder verstärken können — Erkenntnisse, die die Entwicklung neuer Behandlungen für Erkrankungen von Vorhofflimmern über Tremor bis hin zu Gedächtnisstörungen leiten könnten.
Wie SK2-Kanäle als zelluläre Bremsen wirken
SK2-Kanäle sitzen in der Zellmembran und wirken als winzige Bremsen der elektrischen Aktivität. Wenn das Zellinnere während eines elektrischen Signals kurzzeitig mit Calciumionen ansteigt, erkennt ein Helferprotein namens Calmodulin diesen Anstieg. Calmodulin ist an der Innenseite des SK2 befestigt und zieht beim Kalziumbindunг wie an einer Zugleine an einem Kanalteil, wodurch ein Tor geöffnet wird, das Kaliumionen nach außen strömen lässt. Dieser Auswärtsstrom hilft, die Zelle nach einem Aktionspotenzial zu beruhigen, bestimmt mit, wie oft Neuronen Signale senden können, und wie zuverlässig Herzmuskelzellen schlagen. Da SK1–3-Kanäle im Gehirn und Herzen weit verbreitet sind und SK2 ein besonders wichtiges Subtyp ist, ist das genaue Verständnis, wie sie öffnen, schließen und auf Arzneistoffe reagieren, entscheidend für die gezielte Medikamentenentwicklung.
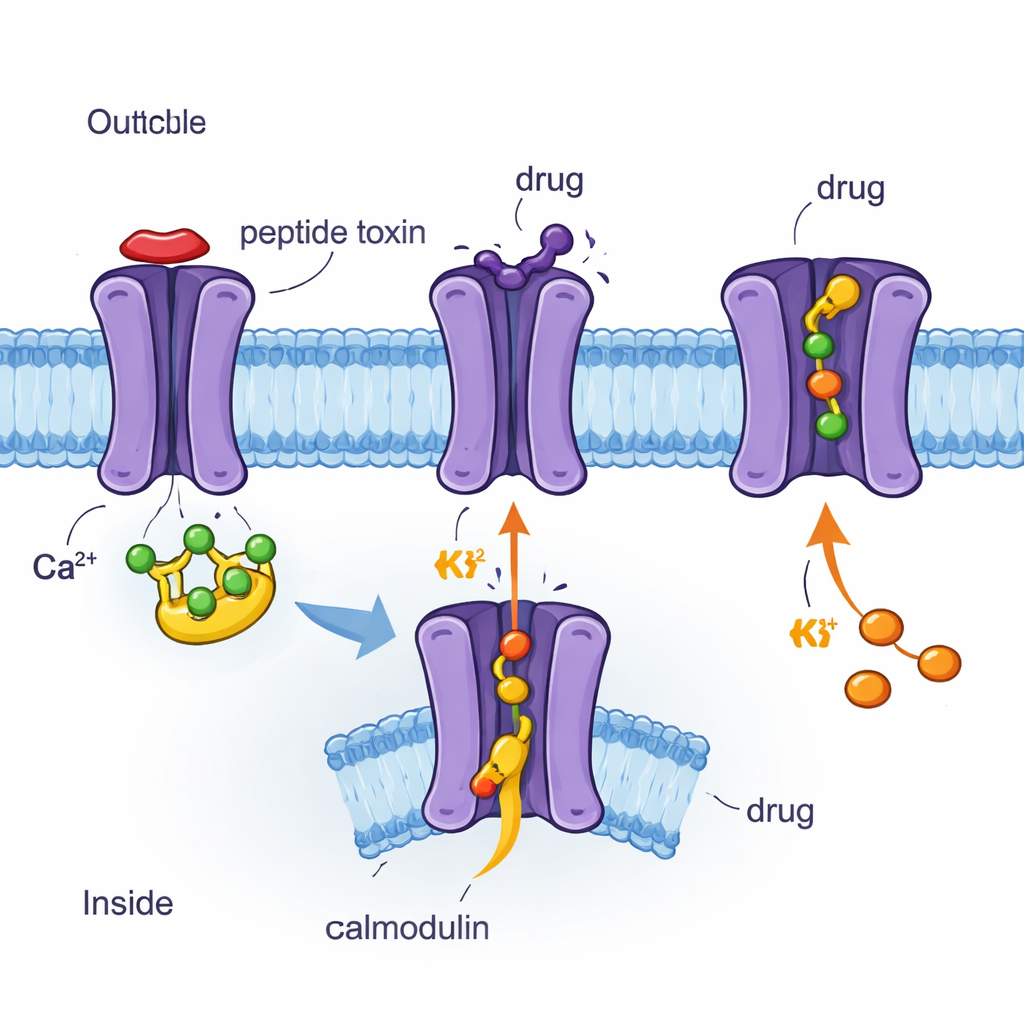
Mit cryo-EM Kanäle und Wirkstoffe atomar sehen
Die Autoren verwendeten Kryo-Elektronenmikroskopie (cryo-EM), eine Methode, die blitzgefrorene Proteine in nahezu atomarer Auflösung abbildet, um vier dreidimensionale Strukturen des menschlichen SK2-Kanals in Komplex mit Calmodulin und verschiedenen Molekülen zu bestimmen. Dazu gehörten das Bienengiftpeptid Apamin, der synthetische Blocker UCL1684, der klinische Inhibitor AP30663 und der klinische Aktivator CAD-1883. Alle vier Strukturen zeigen SK2 als vierteilige Anordnung, die die Membran durchspannt, mit Calmodulin an der Innenseite. Der Vergleich dieser Momentaufnahmen machte deutlich, welche Kanalbereiche starr oder flexibel sind und wie sich Calmodulin bewegt, wenn der Kanal geschlossen oder geöffnet ist. Die Forscher kombinierten diese Bilder zudem mit elektrischen Messungen in Zellen und prüften, wie spezifische Aminosäureänderungen die Reaktion des Kanals auf jede Verbindung verändern.
Ein Bienengift und ein Labormittel, die den äußeren Mund verschließen
Apamin, ein kleines Peptid aus Bienengift, ist seit langem als extrem potenter und selektiver SK2-Blocker in der Forschung bekannt. Die neuen Strukturen zeigen, dass Apamin wie ein Korken am äußeren Mund des SK2-Pores bindet. Es liegt in einem kelchförmigen Vorhof, gebildet von einer kurzen Schleife zwischen zwei Helices (dem S3–S4-Linker), die in SK2 gut geordnet, in einem verwandten Kanal, SK4, jedoch schlaff ist — das erklärt, warum SK4 gegenüber Apamin unempfindlich ist. Wichtige positiv geladene Reste auf Apamin reichen zwischen vier aromatischen Seitenketten des Kanals hindurch und bilden starke elektrostatische und Stacking-Wechselwirkungen, die den Kaliumweg vollständig versiegeln. UCL1684, eine synthetische Bis‑Chinolinium‑Verbindung, besetzt im Wesentlichen dieselbe äußere Tasche und blockiert ebenfalls den Ionaustritt, doch seine geringere Größe erlaubt ein tieferes Sitzen, das die Position der kritischen positiven Ladungen von Apamin nachahmt. Mutationen der Kanalreste, die diesen Vorhof formen, verringern die Empfindlichkeit gegenüber Apamin deutlich und in geringerem Maße gegenüber UCL1684, was bestätigt, dass diese ausgeformte äußere Schleife ein wichtiger Determinant für Toxin- und Arzneiwirkung ist.
Ein zentraler Pfropfen und ein innerer Keil, die die Aktivität justieren
Im Gegensatz dazu bindet der klinische Kandidat AP30663 in die zentrale Kavität von SK2, direkt unter dem Selektivitätsfilter, der Kaliumionen auswählt. Dort wirkt er als physischer Pfropfen, geklemmt zwischen spezifischen Seitenketten, die die Pore auskleiden. Änderungen dieser Auskleidungsreste schwächen die Fähigkeit von AP30663, SK2 zu hemmen, und Sequenzvergleiche erklären, warum nahe Analoga SK1–3 von SK4 unterscheiden können. CAD-1883, ein positiver Modulator, der für Bewegungsstörungen entwickelt wurde, nutzt eine andere Strategie: Es schlüpft in eine Tasche an der Schnittstelle zwischen der N-Lobe von Calmodulin und einem kurzen Linker (S4–S5), der die Bewegung von Calmodulin mit dem Kanalverschluss koppelt. Indem CAD-1883 die Kontakte in dieser Tasche verstärkt, klebt es effektiv Calmodulin und SK2 in einer Konfiguration zusammen, die das innere Tor aufzieht und die Pore weitet. Strukturelle Vergleiche zeigen, dass dieser CAD-1883-gebundene Zustand einem vollständig geöffneten Kanal ähnelt, obwohl der Selektivitätsfilter nach längerer Öffnung eine inaktivierte Form annehmen kann.
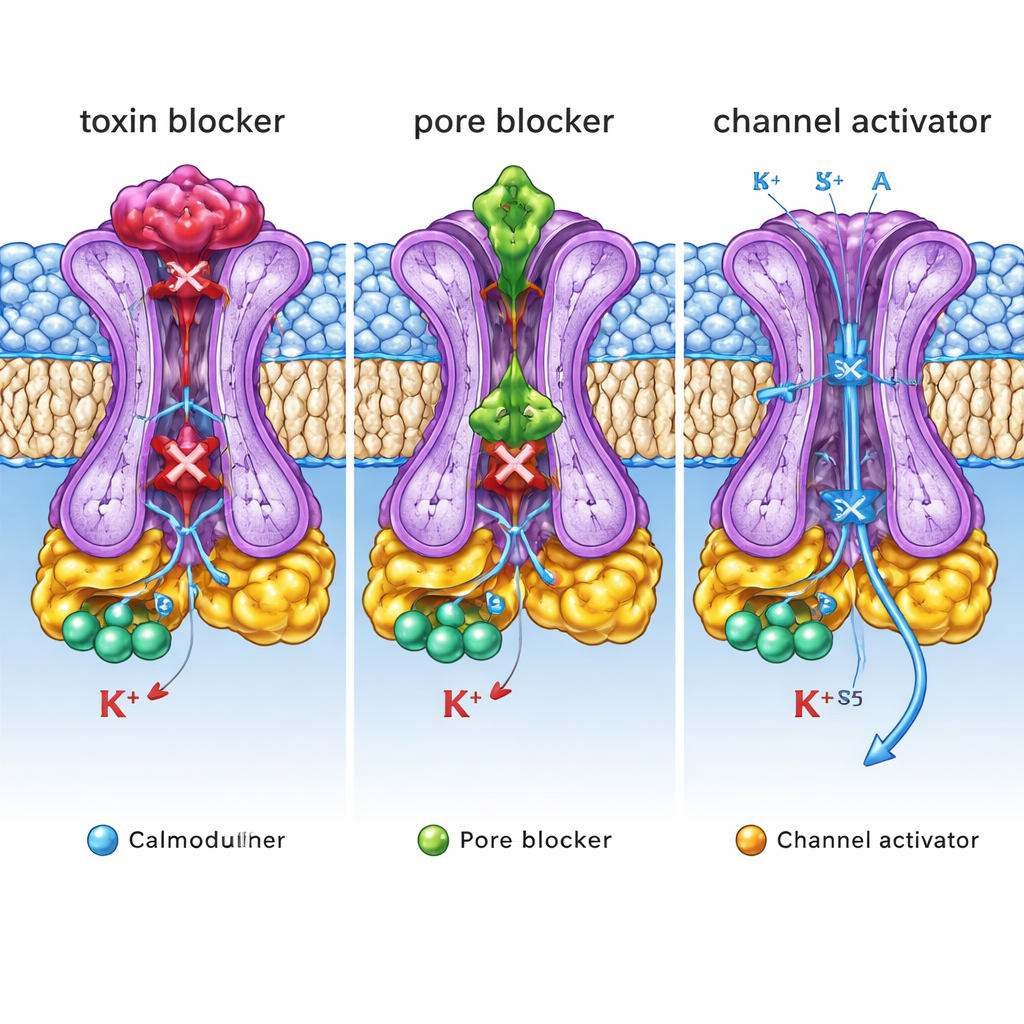
Was diese strukturellen Blaupausen für die Medizin bedeuten
Zusammen zeigen diese Strukturen drei unterschiedliche „Steuerknöpfe“ an einem einzigen SK2-Kanal: einen äußeren Deckel, an dem Toxine und einige Blocker sitzen, eine innere Porenkavität, in der andere Inhibitoren den Fluss verstopfen, und eine seitliche Tasche, in der Aktivatoren die Öffnung stabilisieren. Für den Nichtfachmann ist die zentrale Botschaft, dass derselbe Ionenkanal durch Arzneistoffe, die sehr unterschiedliche strukturelle Griffe ergreifen, nach oben oder unten reguliert werden kann. Indem diese Griffe mit atomarer Präzision kartiert und mit funktionellen Effekten verknüpft wurden, liefert diese Arbeit eine detaillierte Blaupause zur Entwicklung der nächsten Wirkstoffgeneration, die SK2 selektiv dämpft oder verstärkt. Solche maßgeschneiderten Arzneimittel könnten eines Tages helfen, abnorme Hirnrhythmen zu normalisieren, Tremor zu lindern oder unregelmäßige Herzschläge mit weniger Nebenwirkungen zu korrigieren.
Zitation: Ma, B., Wu, D., Cao, E. et al. Structural mechanisms for inhibition and activation of human small-conductance Ca2+-activated potassium channel SK2. Nat Commun 17, 1770 (2026). https://doi.org/10.1038/s41467-026-68475-4
Schlüsselwörter: SK2-Kaliumkanäle, calciumaktivierte Kanäle, cryo-EM-Strukturen, Ionenkanal-Modulatoren, Vorhofflimmern und Tremor