Clear Sky Science · de
Beeinträchtigte Wanderung und Teilung von Stammzellen bei Duchenne-Muskeldystrophie durch Live‑Imaging aufgedeckt
Warum diese Muskelgeschichte wichtig ist
Duchenne‑Muskeldystrophie (DMD) ist eine tödliche Kinderkrankheit, die die Muskeln nach und nach zerstört. Jahrzehntelang richtete sich die Forschung hauptsächlich auf die großen Muskelfasern, die bei DMD zugrunde gehen. Diese Studie zeigt, dass ein zweiter, leiserer Akteur ebenfalls gestört ist: die körpereigenen Muskelstammzellen, die normalerweise Schäden reparieren. Indem die Autorinnen und Autoren diese Zellen lebend in Mausmuskeln und an einzelnen Fasern beobachteten, zeigen sie, wie Stammzellen bei DMD die Orientierung verlieren, und liefern neue Ansatzpunkte für Therapien, die die Muskelregeneration wirksamer machen könnten.
Die eingebaute Reparaturmannschaft des Muskels
Jede Skelettmuskelfaser wird von einigen residenten Stammzellen flankiert, den sogenannten Satellitenzellen. In gesundem Muskel sind diese Zellen meist in Ruhe. Bei Verletzung erwachen sie, teilen sich und bilden entweder neue Stammzellen, um das Reservoir aufzufüllen, oder spezialisierte Zellen, die in beschädigte Fasern fusionieren. Dieses ausgewogene Verhältnis zwischen Selbsterneuerung und Differenzierung erhält die Muskulatur ein Leben lang. Bei DMD reißen die Muskelfasern jedoch wiederholt, weil ihnen Dystrophin fehlt, ein zentrales Strukturprotein, weshalb sich die Frage stellt, ob die Reparaturmannschaft selbst erschöpft oder fehlgeleitet wird.
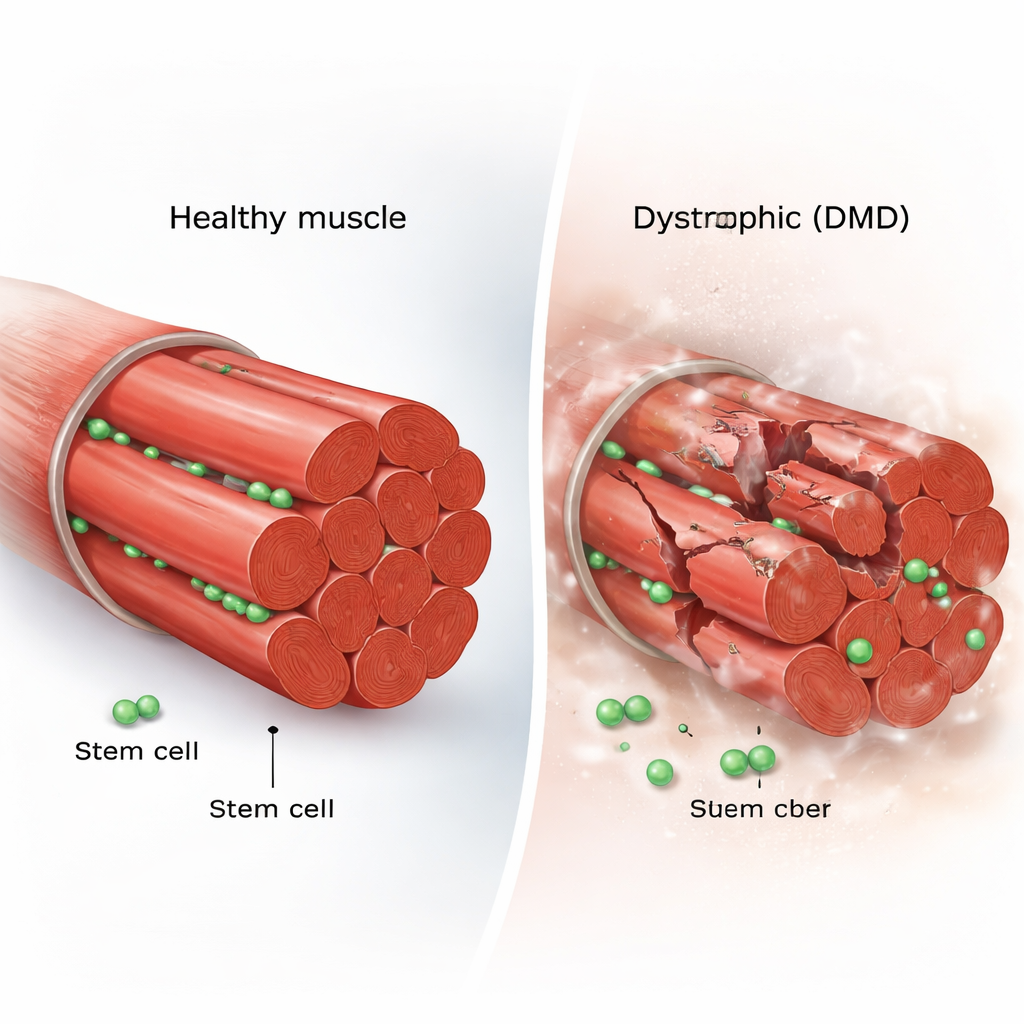
Stammzellen in Aktion filmen
Um das zu klären, nutzten die Forschenden die mdx‑Maus, ein Standardmodell für DMD, und brachten die Muskelstammzellen so zum Leuchten, dass man sie im Mikroskop verfolgen konnte. Sie führten intravitale Bildgebung durch, eine Technik, mit der man lebende Zellen im Inneren eines narkotisierten Tieres über viele Stunden filmen kann. Zusätzlich entwickelten sie ein maßgeschneidertes "Mikrowell"‑System, um einzelne Muskelfasern in Kultur zu halten und jede Stammzellteilung und -bewegung zu verfolgen. Dieser Doppelansatz erlaubte es, einzelne Zellen vom ruhenden Zustand über wiederholte Teilungen und Wanderungen bis zur Fusion in neuen Muskel zu begleiten und Verhaltensweisen zu erfassen, die in statischen Aufnahmen leicht übersehen würden.
Wenn Reparaturzellen hetzen und stolpern
In verletzten gesunden Muskeln dehnten sich die aus Stammzellen hervorgegangenen myogenen Zellen aus und krabbelten mit relativ geradlinigen, gerichteten Bahnen entlang der Fasern; sie teilten sich und breiteten sich effizient aus. Im Gegensatz dazu wurden dystrophische (mdx) Zellen häufig rund und träge. Sie bewegten sich langsamer und weniger zielgerichtet, und ein auffälliger Anteil blieb nahezu unbeweglich. Das Team fand außerdem, dass mdx‑Zellen früher als normal in neue Muskelfasern fusionierten und viele Tochterzellen nach der Teilung zusammenwanderten, anstatt sich zu trennen. Insgesamt zeigten mdx‑Muskeln Anzeichen einer "vorzeitigen Differenzierung": Stammzellen stürzten sich schneller in Muskelzellen und Faserbildung, statt einen belastbaren Vorrat für fortlaufende Reparatur zu erhalten.
Unausgewogene Zellteilungen und eine verwirrte Nachbarschaft
An isolierten Fasern konnten die Forschenden die Teilungsmodi jeder Stammzelle klassifizieren. In gesunden Muskeln waren die meisten Teilungen symmetrisch, aber ausgewogen: viele erzeugten zwei proliferierende Töchter, die den Reparaturpool weiter vergrößern konnten, und weniger erzeugten zwei terminal differenzierte Zellen. Asymmetrische Teilungen, bei denen eine Tochter Zelle Stammzelle blieb und die andere zur Reparatur verpflichtete, waren relativ selten, aber vorhanden. In mdx‑Muskeln verschob sich das Muster deutlich: symmetrische Teilungen gingen zugunsten von zwei differenzierenden Zellen aus, während deutlich weniger Teilungen zwei erneuernde Zellen erzeugten. Kreuztransplantations‑Experimente, bei denen gesunde Stammzellen auf dystrophische Fasern und umgekehrt gesetzt wurden, zeigten, dass Migrationsdefekte weitgehend von der geschädigten Faserumgebung bestimmt werden, während das übermäßige Differenzierungsverhalten der mdx‑Stammzellen in den Zellen selbst verankert war und teilweise durch ihre entzündliche Vorgeschichte geprägt wurde.
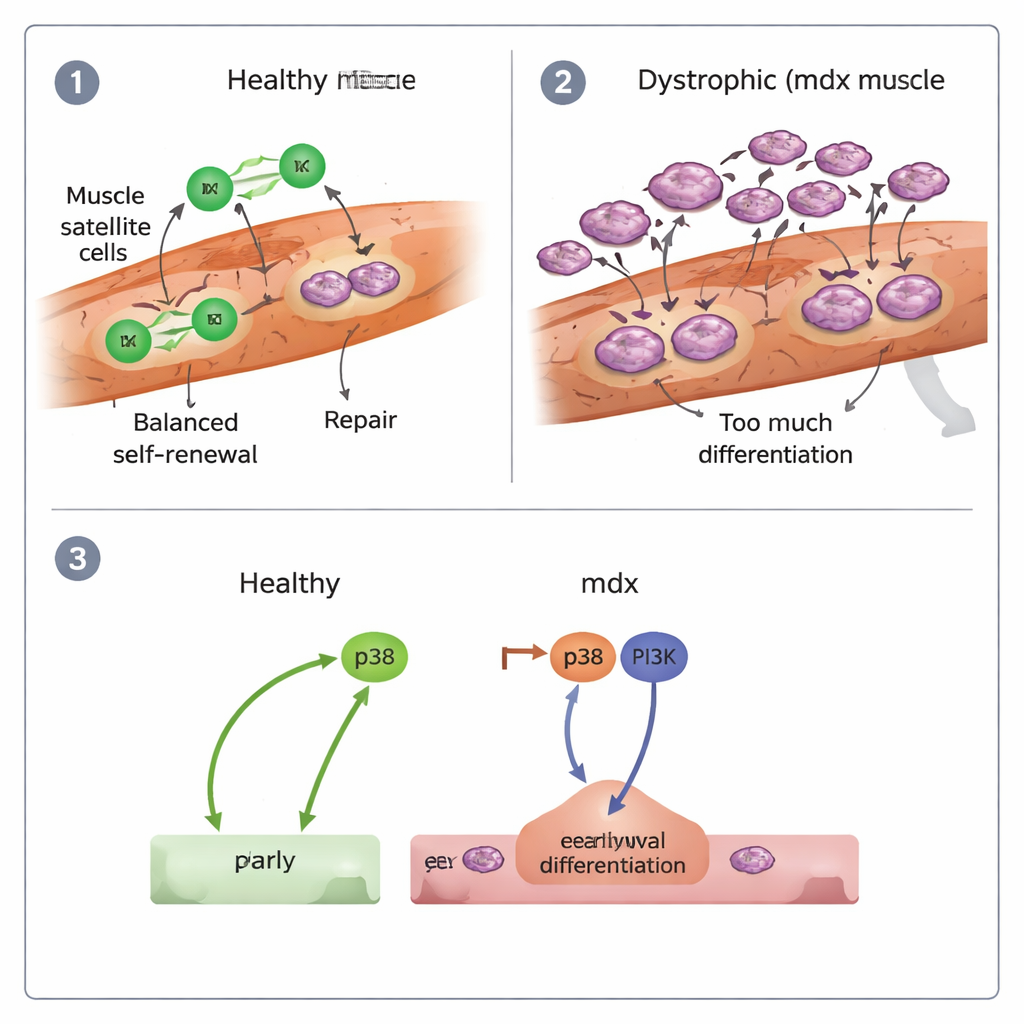
Fehlgeleitete Signale und die Konsequenzen für Therapien
Die Autorinnen und Autoren untersuchten auch die molekularen Schalter, die Stammzellen zur Differenzierung treiben. Sie konzentrierten sich auf zwei Signalwege, bekannt als p38 und PI3K. In gesunden Zellen reduzierte die Blockade von p38 die Differenzierung deutlich, während die Hemmung von PI3K wenig Effekt hatte. In mdx‑Zellen jedoch mussten beide Wege gemeinsam blockiert werden, um das übermäßige Vorpreschen in die Spezialisierung zu bremsen, und selbst dann blieb ihre Fähigkeit zur Proliferation gering. Das deutet darauf hin, dass DMD‑Stammzellen durch kombinierte p38‑ und PI3K‑Aktivität in einen "frühen Burnout" getrieben werden, was zu einer Regeneration führt, die zwar schnell beginnt, aber nicht nachhaltig aufrechterhalten werden kann.
Eine neue Sicht auf Duchenne: auch eine Stammzellkrankheit
Für eine allgemein lesende Zielgruppe lautet die Kernbotschaft: DMD ist nicht nur ein Problem fragiler Muskelfasern; es ist auch ein Problem des Reparatursystems, das diese Fasern wiederherstellen soll. In dystrophischem Muskel bewegen sich Stammzellen weniger effizient, teilen sich auf eine Weise, die das Reservoir erschöpft, und reagieren abnormal auf wichtige Wachstumssignale. Indem diese Arbeit herausarbeitet, welche Aspekte durch die beschädigte Muskelumgebung verursacht werden und welche fest in dem veränderten Zustand der Stammzellen verankert sind, ergeben sich neue Strategien: Therapien, die p38‑ und PI3K‑Signalgebung dämpfen, ausgewogene Zellteilungen wiederherstellen oder die lokale Nische verbessern, könnten helfen, Muskeln effektiver aufzubauen und die Wirksamkeit von Gen‑ oder Zelltherapien für Menschen mit Duchenne‑Muskeldystrophie zu verlängern.
Zitation: Sarde, L., Letort, G., Varet, H. et al. Impaired stem cell migration and divisions in Duchenne muscular dystrophy revealed by live imaging. Nat Commun 17, 1769 (2026). https://doi.org/10.1038/s41467-026-68474-5
Schlüsselwörter: Duchenne‑Muskeldystrophie, Muskelstammzellen, Zellmigration, Stammzellteilung, Regenerative Medizin