Clear Sky Science · de
Coiled-coil-Heterodimer-vermittelte, geteilte Baseneditorsysteme ermöglichen flexible und robuste Nukleotidaustausche
DNA-Reparatur mit weniger Nebenwirkungen
Viele Krankheiten werden durch winzige Tippfehler in unserer DNA verursacht – einstellige Fehler, die lebensbedrohliche Folgen haben können. Forschende verfügen über mächtige Werkzeuge, sogenannte Baseneditoren, die diese Fehler korrigieren können, ohne die DNA zu zerschneiden. Diese Werkzeuge sind jedoch sperrig und schwer sicher in den Körper zu transportieren. Diese Arbeit stellt eine neue Methode vor, Baseneditoren in kleinere, intelligentere Teile zu spalten, die dennoch ebenso gut oder sogar besser funktionieren als das Original, und eröffnet damit neue Wege zur Behandlung genetischer Erkrankungen in der Leber, in Muskeln und darüber hinaus.
Warum Größe ein Problem für Genreparatur‑Werkzeuge ist
Baseneditoren kombinieren Teile des CRISPR‑Systems mit Enzymen, die einen DNA‑Buchstaben gegen einen anderen austauschen können, etwa ein A gegen ein G oder ein C gegen ein T. Solche präzisen Austauschvorgänge sind vielversprechend zur Behandlung von Erkrankungen wie hohem Cholesterinspiegel oder Muskeldystrophie. Ein führender Lieferweg für Gentherapie, das Adeno‑assoziierte Virus (AAV), kann jedoch nur etwa 4,7 Tausend DNA‑Basen tragen, während Standard‑Baseneditoren größer sind. Frühere Ansätze versuchten, diese Editor‑Systeme mithilfe spezieller Proteinscheren (Inteine) zu teilen oder sie durch verkleinerte Enzyme zu schrumpfen, doch diese Strategien verringerten oft die Effizienz, erhöhten die Designkomplexität oder schränkten die Zielbereiche im Genom ein.
Molekulares Klettband zum Wiederaufbau des Editors
Um dieses Problem zu lösen, entwarfen die Forschenden einen „geteilten“ Baseneditor, der durch winzige Protein‑Reißverschlüsse, sogenannte Coiled‑coil‑Heterodimere, zusammengehalten wird – vergleichbar mit molekularem Klett. Sie teilten den Baseneditor in zwei Hälften: eine trägt die DNA‑zielende Cas9‑Nickase, die andere das Editierenzym. Kurze Coiled‑coil‑Peptide an jeder Hälfte suchen einander und verbinden sich, sobald beide Hälften an derselben DNA‑Stelle ankommen. So entstehen Coiled‑coil‑Baseneditoren (CC‑BEs), einschließlich Typen, die C bearbeiten (CC‑CBE), A (CC‑ABE) und komplexeren Varianten, die verschiedene Arten von Basenaustauschen ermöglichen. 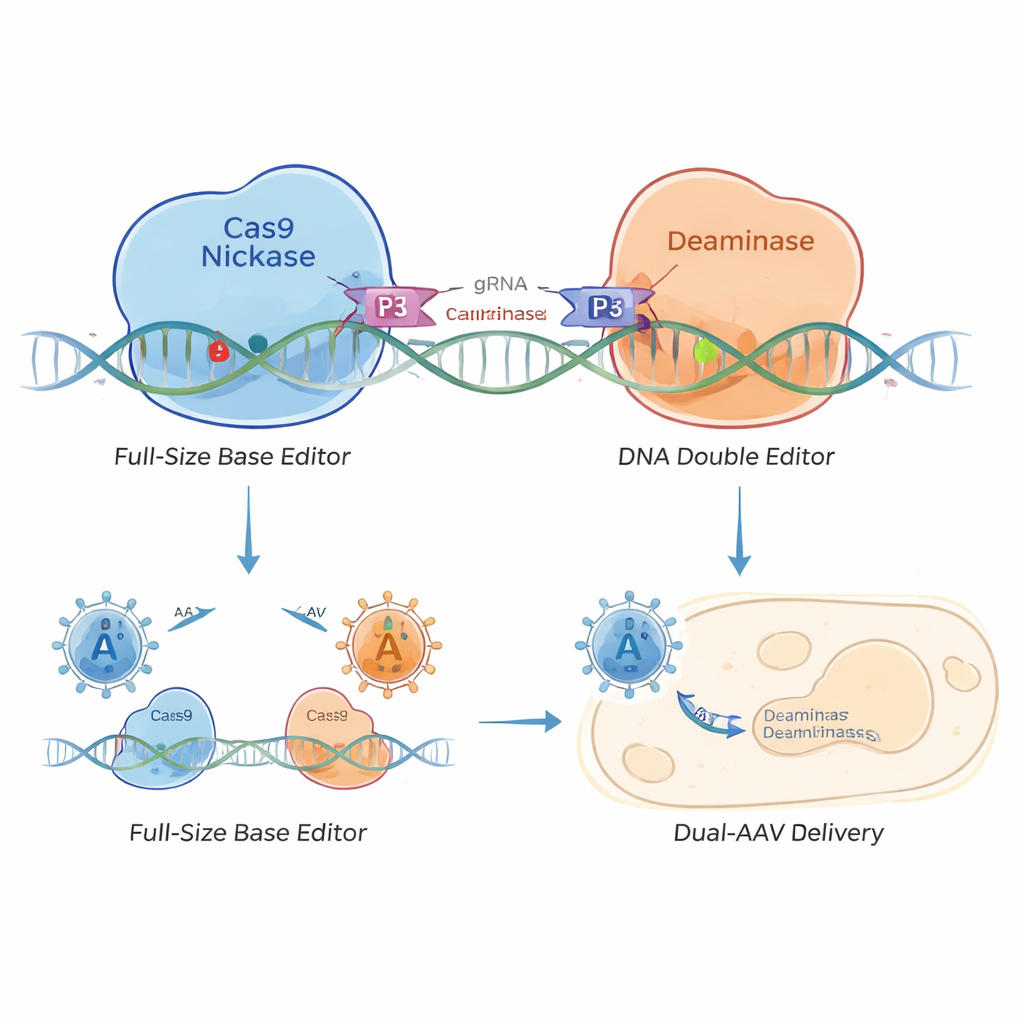
Flexibles, leistungsfähiges und präzises Editieren
Das Team testete CC‑BEs in verschiedenen Zelltypen, darunter menschliche Zellen und primäre Schweinezellen, und mit unterschiedlichen Cas9‑Varianten, die ein breiteres Spektrum an DNA‑Sequenzen erkennen. Die CC‑CBE‑Versionen funktionierten nicht nur zuverlässig an vielen Stellen, sondern zeigten auch ein erweitertes „Editierfenster“, das heißt, sie konnten Zielbasen über einen größeren DNA‑Abschnitt verändern und gaben Forschenden mehr Flexibilität bei der Auswahl von Guide‑RNAs. Die CC‑ABE‑Versionen erreichten ähnliche Effizienzen wie die besten vorhandenen Adenin‑Editoren und produzierten häufig weniger Off‑Target‑Nebenprodukte. Die Autoren passten die Coiled‑coil‑Strategie außerdem an neuere Editor‑Designs an – etwa kompakte TadCBE und präzise ABE9 – und stellten erneut fest, dass das Teilen der Werkzeuge mit Coiled‑coil‑Paaren die Leistung bewahrte oder verbesserte.
Von Zellkulturen zu lebenden Mäusen
Wesentlich ist, dass die Autoren zeigten, dass diese geteilten Editoren in lebenden Tieren mit dualer AAV‑Auslieferung funktionieren, wobei jedes Viruspartikel die halbe Maschinerie trägt. In Mäusen erzielte ein CC‑ABE, das das Pcsk9‑Gen in der Leber anvisierte, A‑zu‑G‑Editierungen mit Raten bis zu etwa 70 %, was Pcsk9‑Protein und LDL‑Cholesterin im Blut deutlich senkte, ohne Anzeichen von Leberschäden. 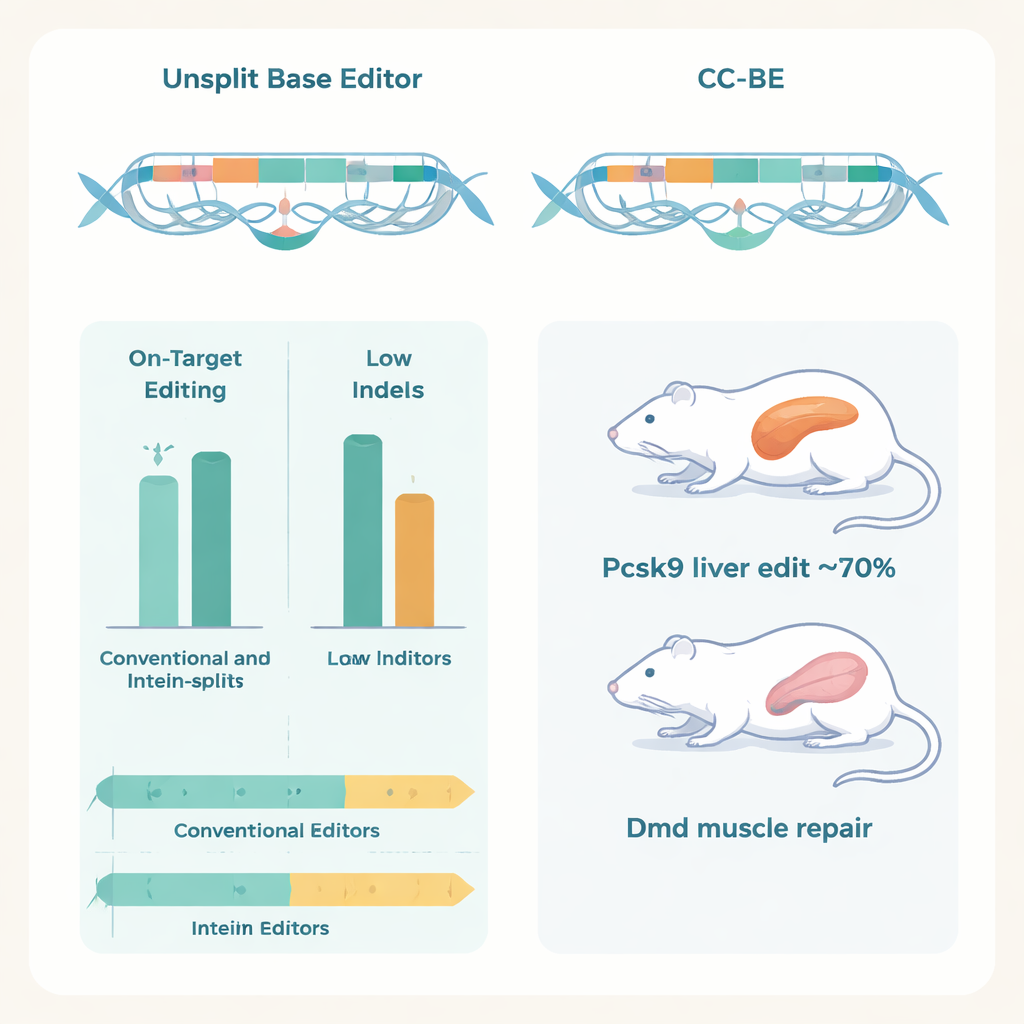
Ein neuer Weg hin zu praktikabler DNA‑Reparatur
Im Kern stellt diese Studie einen einfachen, aber wirkungsvollen ingenieurtechnischen Trick vor: kleine Coiled‑coil‑„Haken“ verwenden, um große Baseneditoren in AAV‑kompatible Module zu zerlegen, die sich nur dort wieder zusammenfügen, wo sie gebraucht werden. Für Nicht‑Fachleute lautet die Quintessenz, dass Forschende nun leistungsfähige DNA‑Reparaturwerkzeuge in klinisch erprobte virale Träger verpacken können, ohne Genauigkeit oder Wirksamkeit zu opfern. Dieser Coiled‑coil‑Ansatz könnte es erleichtern, Therapien für eine breite Palette einzelner Basenfehler in Organen wie Leber, Herz und Muskel zu entwickeln und damit fein abgestimmte Genkorrekturen einen Schritt näher an die klinische Anwendung zu bringen.
Zitation: Mu, S., Li, Q., Chen, M. et al. Coiled-coil heterodimer-mediated split base editing systems enable flexible and robust nucleotide substitutions. Nat Commun 17, 1765 (2026). https://doi.org/10.1038/s41467-026-68469-2
Schlüsselwörter: Baseneditor, Gentherapie, CRISPR, AAV‑Verabreichung, genetische Erkrankung