Clear Sky Science · de
H3K27me3-abhängige Prägung und transkriptionelle Regulation in frühen Maus-Embryonen erfordert EZHIP-vermittelte Einschränkung der PRC2-Aktivität
Warum winzige Embryonen sorgfältiges genetisches Timing brauchen
Jedes Säugetier beginnt das Leben als einzelne Zelle, die ein Chromosomensatz von der Mutter und einen von dem Vater trägt. Obwohl diese beiden genetischen Pakete nahezu dieselben DNA‑Bausteine enthalten, kommen sie mit unterschiedlichen chemischen Markierungen an, die mitentscheiden, welche Gene an‑ oder abgeschaltet werden. Diese Untersuchung beleuchtet, wie eines dieser Markiersysteme in den ersten Tagen nach der Befruchtung bei Mäusen im Gleichgewicht gehalten wird und warum eine Störung dieses Gleichgewichts die normale Entwicklung aus der Bahn werfen kann.
Zwei Eltern, zwei unterschiedlich verpackte Genome
Bei Säugetieren verhalten sich bestimmte Gene unterschiedlich, je nachdem, ob sie von der Mutter oder vom Vater stammen — ein Phänomen, das als genomische Prägung bezeichnet wird. Klassische Prägung beruht auf chemischen Markierungen direkt an der DNA, doch in den letzten Jahren entdeckten Forschende eine zweite, kurzlebigere Form, die von einer Modifikation von Histonproteinen namens H3K27me3 abhängt. Diese Histone wirken wie Spulen, um die sich die DNA windet, und H3K27me3 führt dazu, dass benachbarte Gene abgeschaltet werden. In normalen Maus‑Embryonen trägt das maternale Genom unmittelbar nach der Befruchtung mehr von diesem Marker als das paternale Genom, was hilft, bestimmte mütterliche Genkopien zu stummschalten, während die väterlichen Kopien arbeiten können.
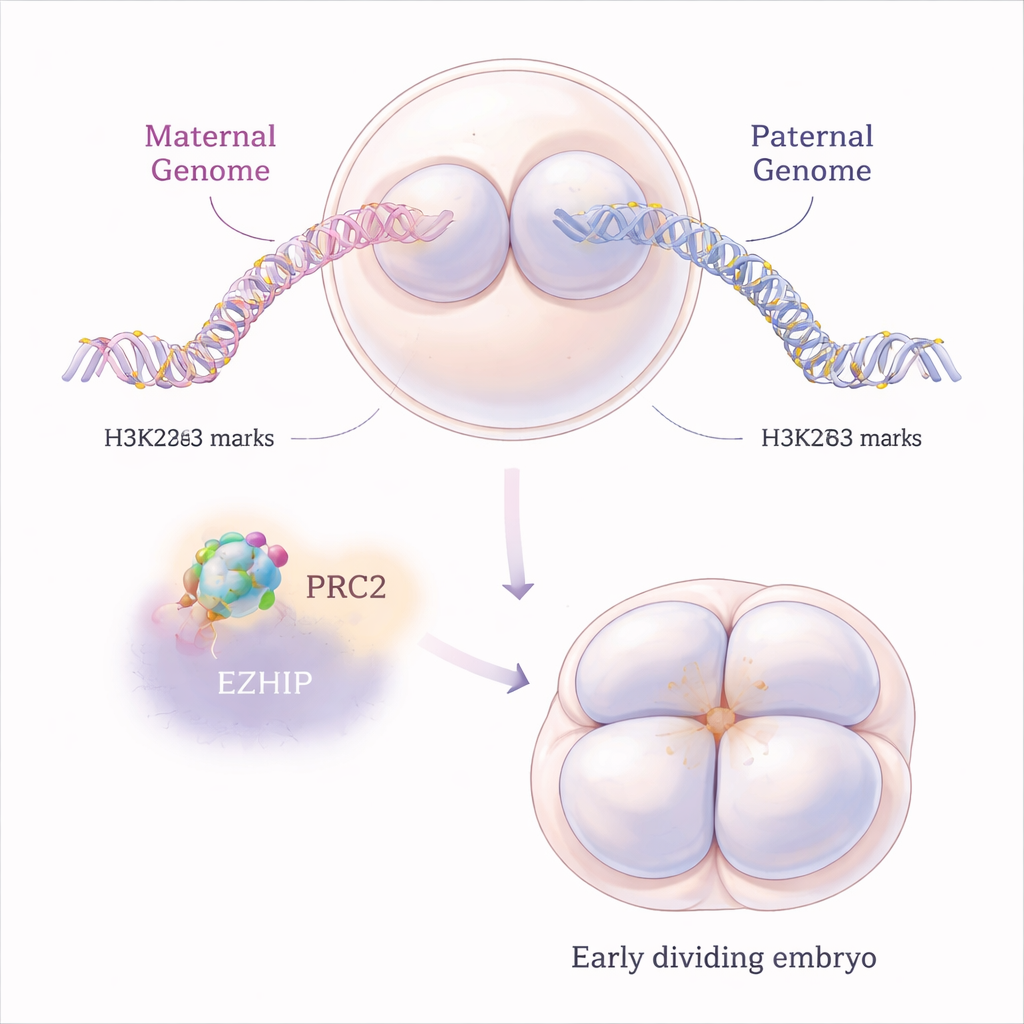
Eine molekulare Bremse für einen starken Repressor
H3K27me3 wird auf Chromatin von einer großen Proteinfabrik namens PRC2 aufgebracht. Die Autorinnen und Autoren konzentrierten sich auf EZHIP, ein weniger bekanntes Protein, das an PRC2 bindet und dessen Aktivität verlangsamt. Eizellen von Mäusen produzieren viel Ezhip‑RNA, und das daraus entstehende EZHIP‑Protein bleibt in Embryonen während der ersten Zellteilungen erhalten. Durch Untersuchungen an Mäusen, deren Mütter Ezhip nicht besitzen, fragten die Forschenden, was passiert, wenn diese natürliche Bremse entfällt. Sie stellten fest, dass ohne EZHIP Eizellen und frühe Embryonen zusätzliche H3K27me3‑Marken anhäuften, jedoch auf überraschend "abgeflachte" Weise: statt scharfer, klar abgegrenzter Bereiche breitete sich die Repressionsmark weiter aus und verwischte normale Muster, wobei sowohl maternale als auch paternale Chromosomen betroffen waren.
Wenn zu viel Repression die Prägung zerstört
Mithilfe empfindlicher Genom‑Kartierungsmethoden zeigte das Team, dass die übliche Asymmetrie zwischen den maternalen und paternalem H3K27me3‑Landschaften in Embryonen, die aus Ezhip‑defizienten Eiern entstehen, weitgehend verloren geht. Viele Regionen, die normalerweise H3K27me3 nur auf einer elterlichen Kopie tragen, erhielten die Markierung nun auf beiden oder zeigten verwischte Muster. Diese Veränderung hatte wichtige Folgen für geprägte Gene, die normalerweise durch H3K27me3 statt durch DNA‑Methylierung kontrolliert werden. In Kontroll‑Embryonen werden diese Gene meist überwiegend vom väterlichen Allel exprimiert. In Embryonen ohne maternales EZHIP jedoch waren dieselben Gene häufig von beiden Elternteilen ablesbar, und die Gesamt‑RNA‑Mengen vieler dieser Gene stiegen an, anstatt doppelt stummgeschaltet zu sein.
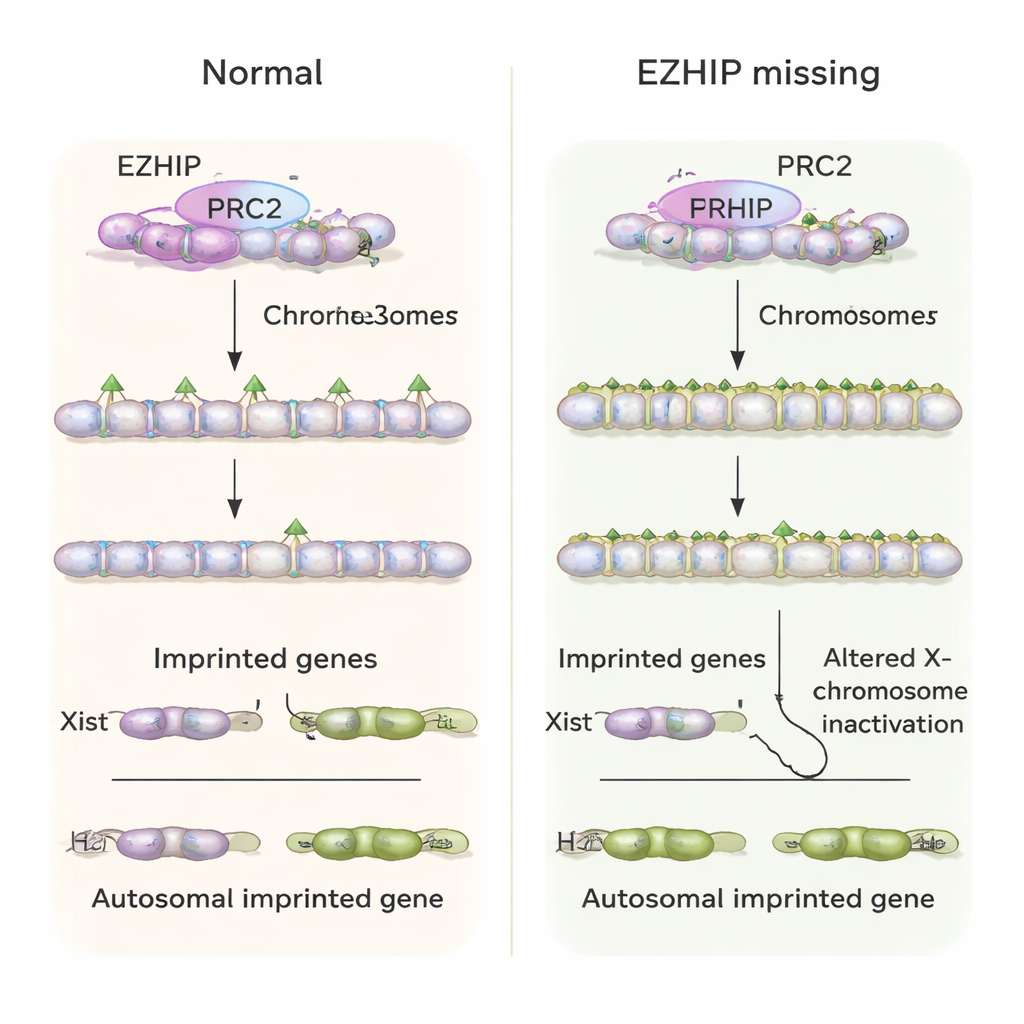
Gestörte X‑Chromosomen‑Kontrolle und Embryonengesundheit
Ein wichtiges H3K27me3‑abhängiges geprägtes Gen ist Xist, eine lange RNA, die ein X‑Chromosom in weiblichen Zellen überzieht und inaktiviert, um die Genmenge gegenüber Männchen auszugleichen. Normalerweise exprimieren frühe Maus‑Embryonen Xist nur vom väterlichen X in Weibchen und gar nicht in Männchen. In Abwesenheit von maternalen EZHIP beobachteten die Autorinnen und Autoren, dass weibliche Embryonen häufig Xist von beiden X‑Chromosomen exprimierten, während männliche Embryonen "unangemessen" Xist von ihrem einzigen X einschalteten. Dies führte zu abnormen Inaktivierungsmustern X‑verknüpfter Gene. Auf der Ebene des gesamten Tieres wurden weniger Mäuse von Ezhip‑defizienten Müttern geboren, und Embryonen zeigten verändertes Wachstum sowie Probleme in extraembryonalen Geweben, die die Plazenta stützen — Hinweise auf anhaltenden Entwicklungsstress durch frühe Versagen der Prägung.
Zu viel des Guten kann schädlich sein
Für Laien mag es intuitiv erscheinen, dass mehr von einer silenzierenden Markierung wie H3K27me3 einfach mehr Gene zum Schweigen bringen würde. Diese Arbeit zeigt stattdessen, dass das Überladen des Genoms mit solchen Markierungen in falschem Muster deren Fähigkeit, als präzise Schalter zu fungieren, untergraben kann. Durch das Entfernen von EZHIP setzten die Forschenden PRC2 frei, wodurch H3K27me3 sich so weit ausbreitete, dass Prägungssignale verwischten und kritische Regulatoren wie Xist fehlreguliert wurden. Die Studie macht deutlich, dass frühe Embryonen nicht nur die richtigen Moleküle benötigen, sondern deren Aktivität auch eng abgestimmt sein muss, damit maternale und paternale Genome im richtigen Gleichgewicht abgelesen werden.
Zitation: Diop, S., Richart, L., Petitalot, A. et al. H3K27me3-dependent imprinting and transcriptional regulation in early mouse embryos requires EZHIP-mediated restriction of PRC2 activity. Nat Commun 17, 1758 (2026). https://doi.org/10.1038/s41467-026-68467-4
Schlüsselwörter: Epigenetik, genomische Prägung, frühe Embryonalentwicklung, X‑Chromosomen-Inaktivierung, Polycomb PRC2