Clear Sky Science · de
Ausnutzung von Glucan‑induzierter „trained immunity“ für die epigenetische und metabolische Umlenkung von Makrophagen zur Verbesserung der Reaktion auf ein Kolorektalkarzinom‑Vakzin
Die Ersthelfer des Körpers wiederbeleben
Kolorektales Karzinom zählt zu den weltweit tödlichsten Krebsarten, und die Mehrheit der Patienten profitiert nicht von den heutigen Immuntherapien. Diese Studie verfolgt eine spannende Idee: Was wäre, wenn sich das angeborene Immunsystem — die Ersthelfer des Körpers — „trainieren“ ließe, um sich Gefahren zu merken und Impfstoffe wirksamer gegen kolorektale Tumoren zu machen? Mithilfe eines natürlichen Zuckers aus Hefezellwänden, dem Beta‑Glucan, zeigen die Forschenden, wie frühe Immunzellen umprogrammiert werden können, sodass Krebsimpfstoffe stärkere und länger anhaltende Angriffe auf Tumoren auslösen.
Warum kolorektaler Krebs neue Abwehrstrategien braucht
Kolorektales Karzinom verursacht weltweit jährlich fast eine Million Todesfälle, und die Fälle bei jüngeren Erwachsenen nehmen zu. Standardbehandlungen wie Operation, Chemotherapie und Strahlentherapie können wirksam sein, doch viele Patienten erleiden Rückfälle und schwere Nebenwirkungen. Neuere immunbasierte Medikamente, etwa Checkpoint‑Inhibitoren, wirken sehr gut nur bei einem kleinen Subtyp kolorektaler Tumoren mit speziellen DNA‑Reparaturdefekten. Für die Mehrheit der Patienten versagen diese Medikamente und selbst experimentelle Krebsimpfstoffe oft, weil das Tumor‑Mikromilieu von Zellen und Signalen dominiert wird, die die Immunantwort dämpfen.
Dem angeborenen Immunsystem neue Tricks beibringen
Die angeborenen Immunzellen des Körpers — insbesondere Makrophagen — reagieren normalerweise schnell, aber kurz auf Bedrohungen und galten lange als gedächtnislos. Die Forschung der letzten Dekade hat jedoch das Konzept der „trained immunity“ hervorgebracht: Ein starker Erstreiz hinterlässt dauerhafte Spuren in diesen Zellen, sodass sie später kräftiger reagieren. Die Autor:innen nutzten Beta‑Glucan, einen Bestandteil der Hefezellwand, um diesen trainierten Zustand zu induzieren. In Mäusen führte eine kurze Behandlung mit ganzen Beta‑Glucan‑Partikeln zu einer Umprogrammierung der Makrophagen sowohl auf Ebene der Genaktivität als auch des Zellstoffwechsels. Als diese trainierten Tiere später einen kolorektalen Krebsimpfstoff auf Basis eines gentechnisch veränderten Adenovirus (genannt PeptiCrad) erhielten, bildete ihr Immunsystem mächtigere Killer‑T‑Zellen, die tumorspezifische Ziele besser erkannten und angriffen. 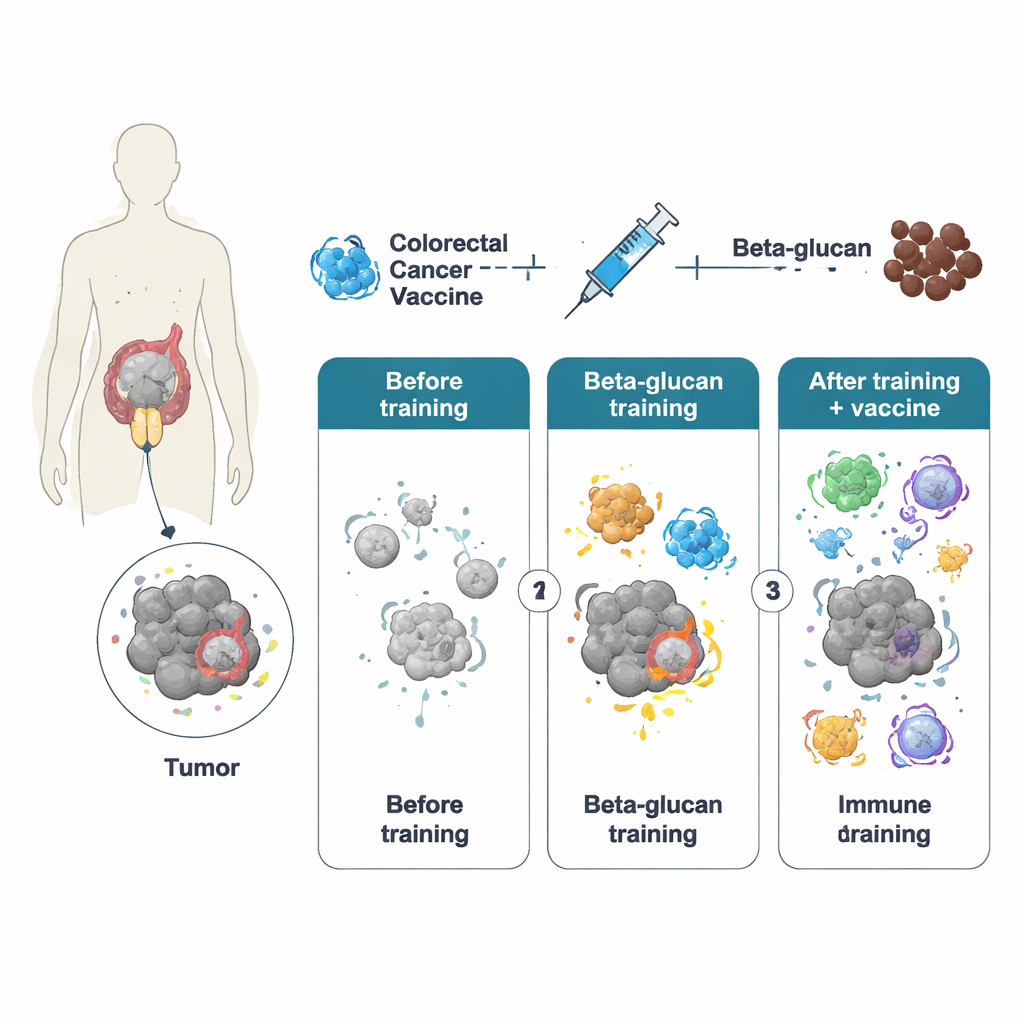
Umlenkung von Energie und Kommunikation im Tumor
Bei tiefergehender Analyse isolierten die Forschenden Immunzellen aus Tumoren und untersuchten deren Stoffwechsel und Genaktivität einzeln. Sie stellten fest, dass trainierte Makrophagen in einen hochaktiven Stoffwechselmodus wechselten, der dem sogenannten Warburg‑Effekt ähnelt, bei dem Zellen Zucker schnell verbrennen und Ressourcen in Bausteine für Wachstum und Funktion umlenken. Diese Zellen steigerten zudem den Kreatin‑Stoffwechsel — bekannt aus Sportergänzungen — was half, die zusätzliche Energie bereitzustellen, die zur Produktion entzündlicher Moleküle nötig ist. Gleichzeitig markierten spezifische chemische Anhänge an DNA‑gebundenen Proteinen (insbesondere eine Zunahme von H3K4me3) Gene, die an der Produktion von Chemokinen beteiligt sind, und verankerten so dauerhaft ein pro‑entzündliches, tumorkampfbereites Programm.
Ein immunologisches Staffelteam aufbauen
Einzelzellsequenzierung zeigte eine schrittweise Staffelung zwischen verschiedenen Immunzellen im Tumor. Zuerst setzten trainierte Makrophagen hohe Mengen zweier Schlüssel‑Signale frei, CXCL9 und CXCL10, die natürliche Killerzellen (NK‑Zellen) über den Rezeptor CXCR3 anlockten. Einmal rekrutiert, töteten diese NK‑Zellen nicht nur Krebszellen, sondern schütteten auch einen weiteren Botenstoff, CCL5, aus, der eine spezialisierte dendritische Zelluntergruppe namens cDC1 anzog. Diese dendritischen Zellen sind besonders gut darin, Tumorantigene T‑Zellen zu präsentieren. In der Folge wurden mehr CD8‑T‑Zellen aktiviert und in Effektormemoryzellen umgewandelt — Zellen, die bei Wiederbegegnung mit dem Tumor schnell und kräftig reagieren. Die Blockade der Kreatinnutzung, die Depletion von Makrophagen oder NK‑Zellen oder das Unterbrechen dieser Chemokinwege schwächte die Tumorkontrolle und unterstrich, wie sehr der Impferfolg von der Makrophagen–NK–dendritische‑Zelle–T‑Zell‑Schaltung abhängt. 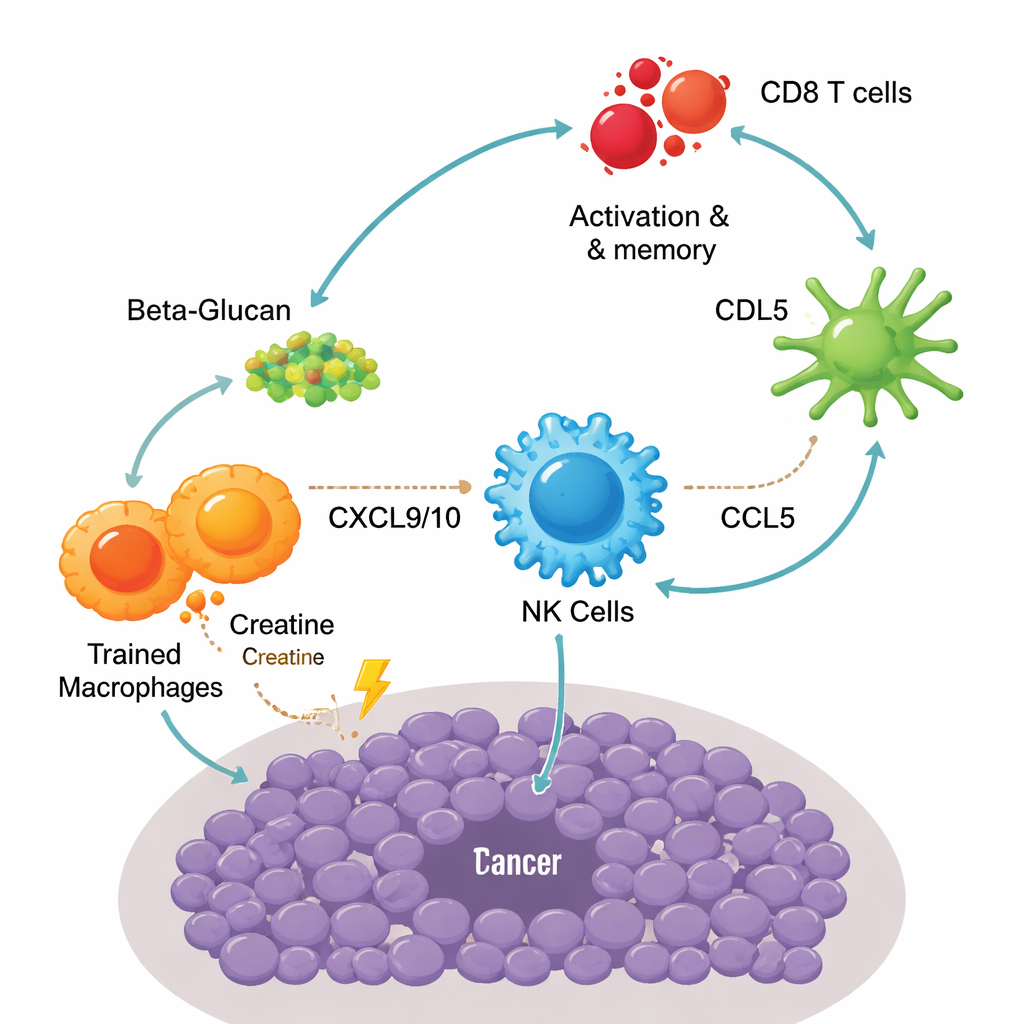
Von Mausmodellen zu menschlichen Tumor‑Organoiden
Das Team prüfte seinen Ansatz in mehreren Mausmodellen des kolorektalen Krebses, einschließlich eines besonders hartnäckigen Typs, der gegen gängige Immuntherapien resistent ist. In jedem Fall verlangsamte die Kombination aus Beta‑Glucan‑Training und dem Impfstoff das Tumorwachstum stärker als jede Einzelbehandlung. Wichtig ist: Die Forschenden gingen über Mäuse hinaus. Menschliche Blutzellen, die Beta‑Glucan ausgesetzt wurden, reagierten stärker auf ein kolorektales Krebsimpfstoffpeptid und produzierten mehr immunstimulierende Zytokine. Wurden diese trainierten Immunzellen vermehrt und mit patientenabgeleiteten Mini‑Kolorektaltumoren (Organoiden) ko‑kultiviert, töteten sie mehr Krebszellen als nicht trainierte Zellen. Entfernt man humane Monozyten und Makrophagen aus dem System, verschwindet dieser Vorteil — ein Beleg dafür, dass diese trainierten Zellen als wesentliche Organisatoren fungieren und nicht primär als direkte Tumorzellen‑Killer.
Was das für künftige Krebsimpfstoffe bedeuten könnte
Kurz gefasst zeigt diese Arbeit, dass ein sicheres, aus Hefe gewonnenes Zuckerfragment angeborene Immunzellen „coachen“ kann, um eine effektivere Impfung gegen kolorektalen Krebs zu unterstützen. Durch die Umlenkung, wie Makrophagen Energie nutzen und welche Gene sie einsatzbereit halten, löst Beta‑Glucan‑Training eine Dominowirkung aus: Makrophagen rufen NK‑Zellen herbei, NK‑Zellen rekrutieren erfahrene dendritische Zellen, und gemeinsam formen sie ein stärkeres Heer aus Gedächtnis‑CD8‑T‑Zellen. Vieles muss noch in klinischen Studien geprüft werden — einschließlich Sicherheit, Timing und optimaler Impfstoffkombinationen — doch erscheint trained immunity hier als vielversprechende Adjuvans‑Strategie, um mehr „kalte“, unterdrückende kolorektale Tumoren in solche zu verwandeln, die das Immunsystem erkennen und kontrollieren kann.
Zitation: Hamdan, F., Gandolfi, S., D’Alessio, F. et al. Leveraging glucan-induced trained immunity for the epigenetic and metabolic rewiring of macrophages to enhance colorectal cancer vaccine response. Nat Commun 17, 1757 (2026). https://doi.org/10.1038/s41467-026-68466-5
Schlüsselwörter: Immuntherapie bei kolorektalem Krebs, trained immunity, Beta‑Glucan, Makrophagen und NK‑Zellen, Krebsimpfstoffe