Clear Sky Science · de
In vivo-CRISPR-Screening identifiziert Mitglieder des SAGA-Komplexes als Schlüsselknoten der Hämatopoese
Warum es wichtig ist, die Blutbildung im Gleichgewicht zu halten
Jeden Tag produziert Ihr Körper unauffällig hunderte Milliarden neuer Blutzellen, die Sauerstoff transportieren, Infektionen bekämpfen und Blutungen stoppen. Diese ununterbrochene Produktion hängt von seltenen „Mutter“-Zellen im Knochenmark ab, den blutbildenden Stammzellen. Wenn die Steuerung dieser Zellen gestört ist, können Menschen Anämie, ein geschwächtes Immunsystem oder Krebsarten wie Leukämie entwickeln. Diese Studie stellt eine einfache, aber wirkungsvolle Frage: Von den Tausenden Genen in unserem Genom, welche sind wirklich essenziell, um die Blutbildung gesund und im Gleichgewicht zu halten?
Eine genomweite Schatzsuche in Maus-Stammzellen
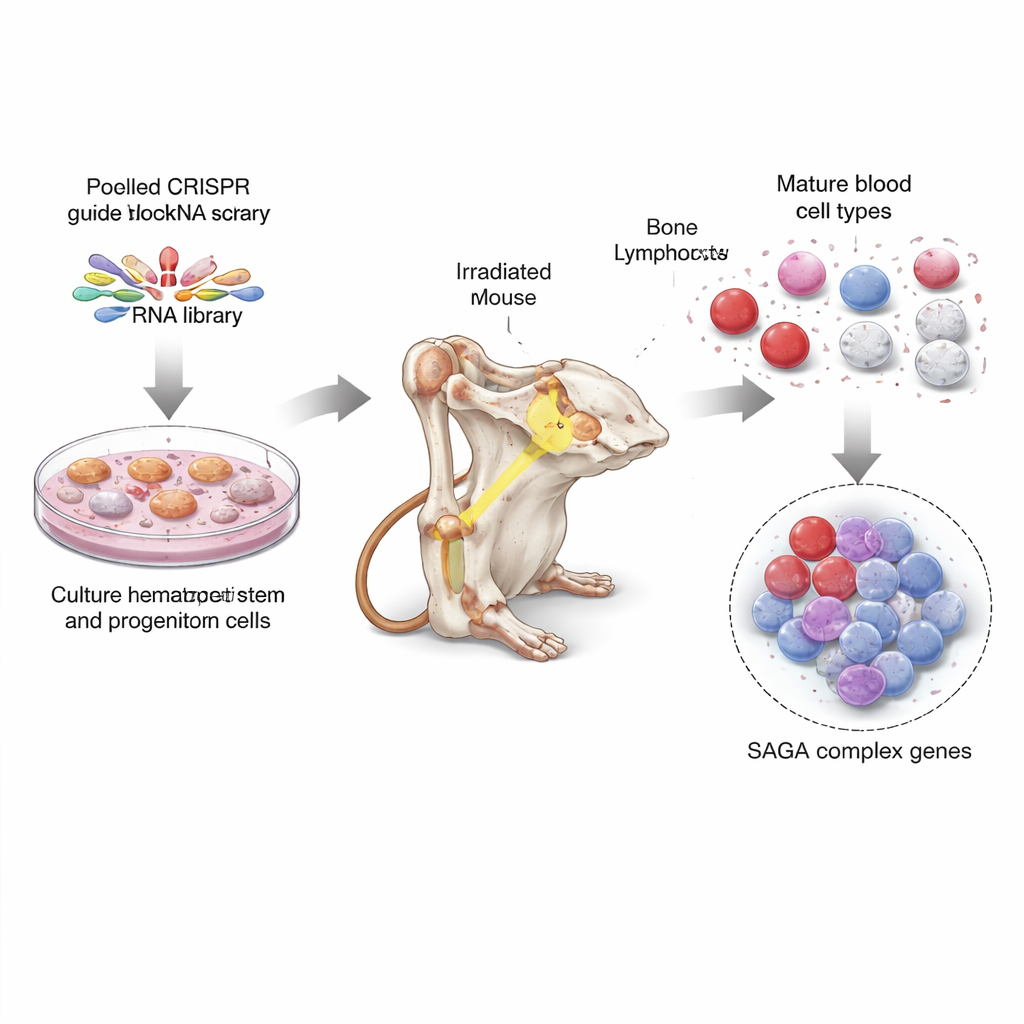
Um das herauszufinden, nutzten die Forschenden CRISPR, das Geneditierungswerkzeug, das oft mit molekularen Scheren verglichen wird, und schalteten nahezu jedes Gen im Mausgenom aus — mit zehn Guides pro Gen. Zunächst vermehrten sie große Mengen von Knochenmark-Stamm- und Vorläuferzellen unter speziellen Kulturbedingungen und infizierten diese Zellen dann mit gepoolten CRISPR-Guides, sodass jede Zelle einen anderen Genausfall trug. Anschließend transplantierten sie diese gemischten, editierten Zellen in dutzende bestrahlte Mäuse und ließen die editierten Zellen die Blutbildenden Systeme der Tiere wiederaufbauen. Monate später reinigten sie verschiedene reife Blutzelltypen und stammzellähnliche Zellen aus dem Knochenmark und bestimmten, welche CRISPR-Guides über- oder unterrepräsentiert waren. So zeigte sich, welche Genverluste unreife Zellen begünstigten und welche die Produktion vollständig ausgebildeter Blutzellen unterstützten.
Ein verborgenes Steuerzentrum namens SAGA tritt hervor
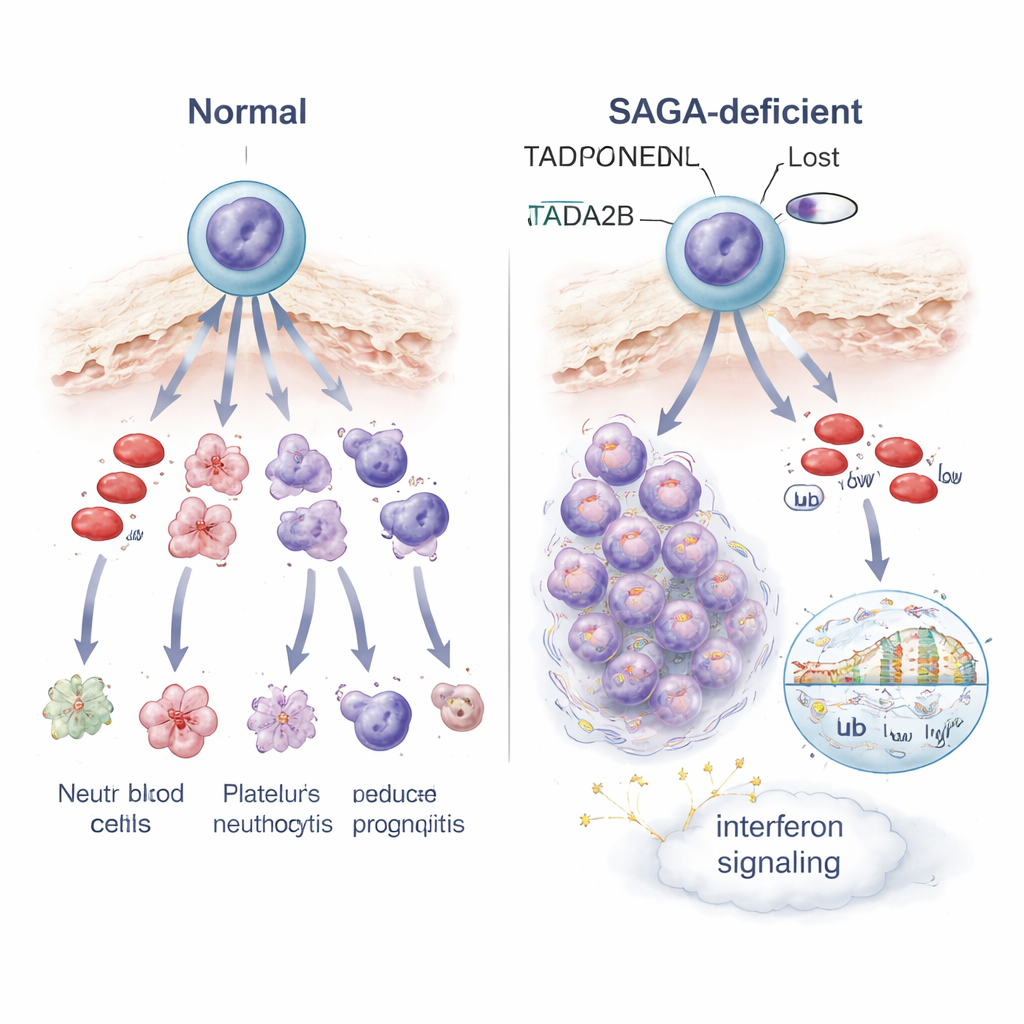
Unter vielen bekannten Regulatoren der Blutbildung tauchte eine überraschende Gruppe von Treffern auf: mehrere strukturelle Komponenten eines großen Proteinassemblats namens SAGA-Komplex, darunter Gene mit den Namen Tada2b, Taf5l und Tada1. SAGA stellt keine Blutzellen her; stattdessen hilft es, andere Gene an- oder auszuschalten, indem es DNA-verpackende Proteine, die Histone, chemisch markiert. Als das Team diese SAGA-Komponenten einzeln ausschaltete und die editierten Zellen in Mäuse transplantierte, zeigte sich ein konsistentes Muster. Unreife Knochenmarkzellen häuften sich an, während ihre Fähigkeit, zu zirkulierenden Leukozyten, Erythrozyten und bestimmten Immunzellen zu reifen, deutlich vermindert war. Im Wesentlichen steckten Stamm- und Vorläuferzellen in einem Engpass fest und konnten die Reise zu funktionsfähigen Blutzellen nicht abschließen.
Wie gestörte Genkontrolle Zellschicksal und Stresssignale verändert
Um zu verstehen, was in diesen blockierten Zellen schiefläuft, analysierten die Wissenschaftler die Genaktivität einzeln pro Zelle und im Bulk. Der Verlust von Tada2b oder Taf5l veränderte die Aktivität vieler Gene in Stammzellen und zeigte zwei auffällige Muster. Erstens wurden Gene der Interferon-Signalgebung — normalerweise Teil der antiviralen Abwehr des Körpers — hochreguliert, was auf einen inneren Alarm- oder Stresszustand hindeutet. Zweitens wurden die Mitochondrien, die winzigen Kraftwerke der Zellen, weniger aktiv, und die veränderten Zellen wurden empfindlicher gegenüber einem Wirkstoff, der die mitochondriale Energieproduktion angreift. Auf der Ebene der DNA-Verpackung zeigten Zellen ohne Tada2b reduzierte Mengen einer Histonmarkierung, die mit offenem, aktivem Chromatin verknüpft ist, sowie Veränderungen einer anderen Markierung, die beeinflusst, wie Gene abgelesen werden. Diese Verschiebungen in der Chromatin-Chemie erklären wahrscheinlich, warum viele Gene, einschließlich jener, die die ordnungsgemäße Blutreifung steuern, fehlreguliert werden.
Von grundlegenden Mechanismen zu Krankheitsmodellen
Das Team untersuchte dann, ob das Hoch- oder Runterregeln der SAGA-Aktivität diese Effekte umkehren kann. Das erzwungene Überexpressieren von Tada2b senkte die Interferon-assoziierte Genaktivität und verringerte den Anteil stammzellähnlicher Zellen — das Spiegelbild des Knockouts. Die Behandlung normaler Stammzellen mit einem Wirkstoff, der die enzymatischen Untereinheiten von SAGA hemmt, reproduzierte viele Aspekte des Tada2b-Verlust-Signatur und stärkte die Idee, dass die chromatinmodifizierende Aktivität von SAGA zentral für seine Funktion ist. Schließlich wandten sich die Forschenden einem menschlichen Zellmodell des myelodysplastischen Syndroms zu, einer Vorleukämie-Erkrankung, bei der die Blutbildung versagt und Interferonwege oft erhöht sind. Als sie in diesen menschlichen Zellen SAGA-Komponenten ausschalteten und sie in immundefiziente Mäuse transplantierten, erhielten die editierten Zellen einen Wachstumsvorteil und zeigten erneut eine Aktivierung von Interferon- und myeloiden Genprogrammen, was darauf hindeutet, dass dieses regulatorische Zentrum auch das Verhalten von Krankheiten prägt.
Was das für Blutgesundheit und zukünftige Therapien bedeutet
Für eine allgemeine Leserschaft lautet die Kernbotschaft: Diese Studie enthüllt ein mächtiges Steuerzentrum — den SAGA-Komplex — das blutbildenden Stammzellen hilft zu entscheiden, wann sie unreif bleiben, wann sie reifen und wie sie schädliche Stressreaktionen vermeiden. Wenn zentrale SAGA-Teile fehlen, sammeln sich Stammzellen an, produzieren jedoch nicht genügend funktionelle Blutzellen, während Stress- und antivirale Signale zunehmen und Mitochondrien schwächeln. Diese Entdeckungen vertiefen nicht nur unser Verständnis darüber, wie gesunde Blutbildung über die Lebenszeit erhalten wird, sie deuten auch darauf hin, dass feine Veränderungen der SAGA-Aktivität zu altersbedingten Blutproblemen und Erkrankungen wie dem myelodysplastischen Syndrom beitragen könnten. Langfristig könnte das Aufzeichnen dieser Steuerungsnetzwerke Forschern helfen, Therapien zu entwickeln, die fehlerhafte Stammzellen wieder zu einer ausgewogenen, widerstandsfähigen Blutproduktion zurückführen.
Zitation: Shankar, A., Olender, L., Hsu, I. et al. In vivo CRISPR screening identifies SAGA complex members as key regulators of hematopoiesis. Nat Commun 17, 1756 (2026). https://doi.org/10.1038/s41467-026-68465-6
Schlüsselwörter: hämatopoetische Stammzellen, CRISPR-Screening, SAGA-Komplex, Interferon-Signalgebung, myelodysplastisches Syndrom