Clear Sky Science · de
Intranasale Verabreichung eines breit wirksamen makrozyklischen Peptid-Inhibitors schützt vor SARS-CoV-2-Omikron-Varianten
Warum ein Nasenspray gegen COVID weiterhin wichtig ist
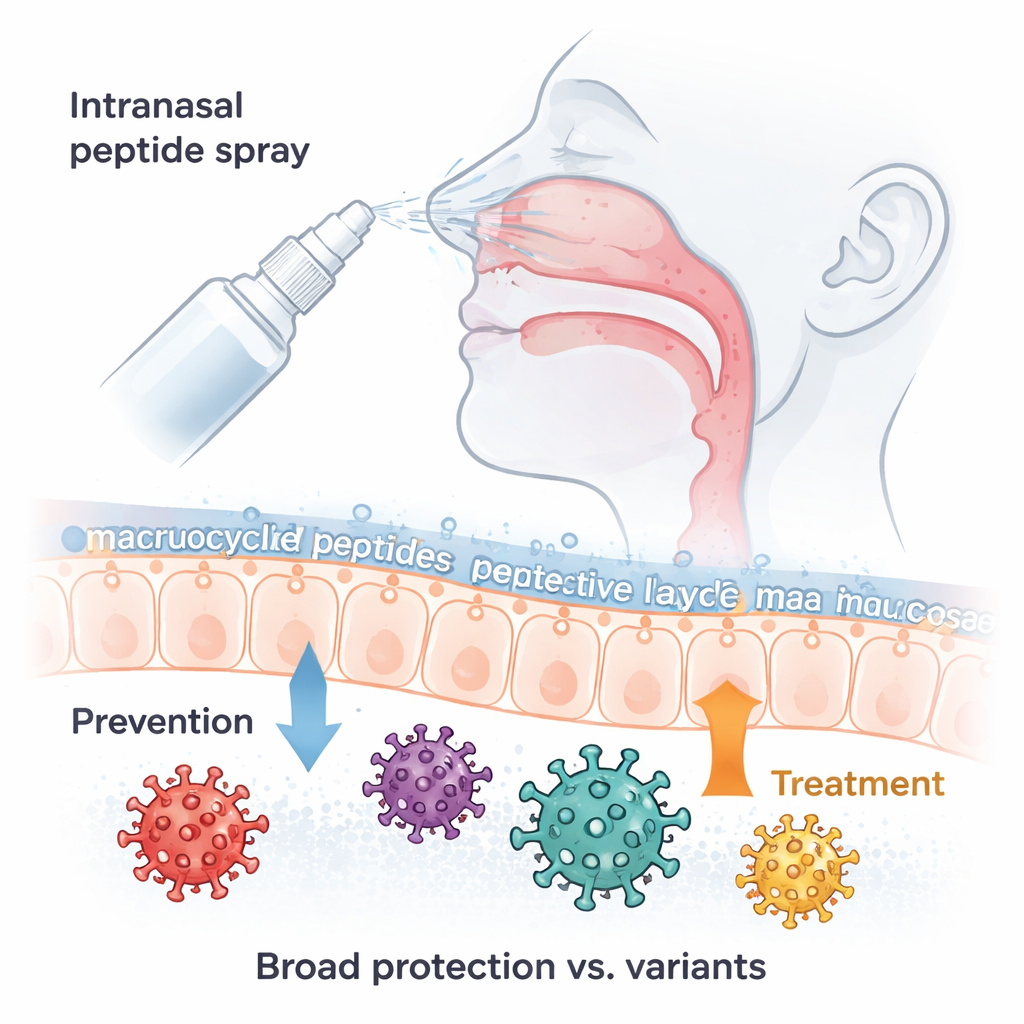
Obwohl der pandemische Notfall von COVID-19 vorbei ist, infiziert das verantwortliche Virus SARS-CoV-2 weiterhin Menschen weltweit und verursacht Todesfälle, vor allem bei älteren Personen und Menschen mit geschwächtem Immunsystem. Neue Varianten wie Omikron entwickeln fortlaufend Wege, unsere Impfstoffe und Antikörpertherapien zu umgehen. Diese Studie beschreibt eine neue Art von Medikament: ein winziges, ringförmiges Molekül, das als einfaches Nasenspray verabreicht wird und eine breite Palette von Omikron- und anderen SARS-CoV-2-Varianten daran hindern kann, sich festzusetzen, und das auch zur Behandlung einer bestehenden Infektion eingesetzt werden kann.
Designer-Ringe als Virusblocker
Die Forschenden konzentrierten sich auf makrozyklische Peptide—kleine, ringförmige Proteinfragmente, die bereits als vielversprechende Arzneimittelkandidaten gelten, weil sie ihre Zielstrukturen fest umschließen können, in Gewebe eindringen und relativ einfach herstellbar sind. Mit einer leistungsfähigen Screening-Plattform, dem sogenannten RaPID-System, bauten und testeten sie riesige Bibliotheken solcher Ringe, um jene zu finden, die an einen kritischen Teil des Coronavirus-Spike-Proteins, die Rezeptorbindungsdomäne (RBD), andocken. Aus dieser Suche identifizierten sie eine Leitverbindung namens 6L3 und verbesserten sie schrittweise durch präzise Änderungen ihrer Aminosäurebausteine. Schließlich entstanden deutlich potentere Varianten mit den Bezeichnungen 6L3-3P und 6L3-3P11K, die die Infektion durch viele Omikron-Subvarianten in Zellkulturen stark blockieren.
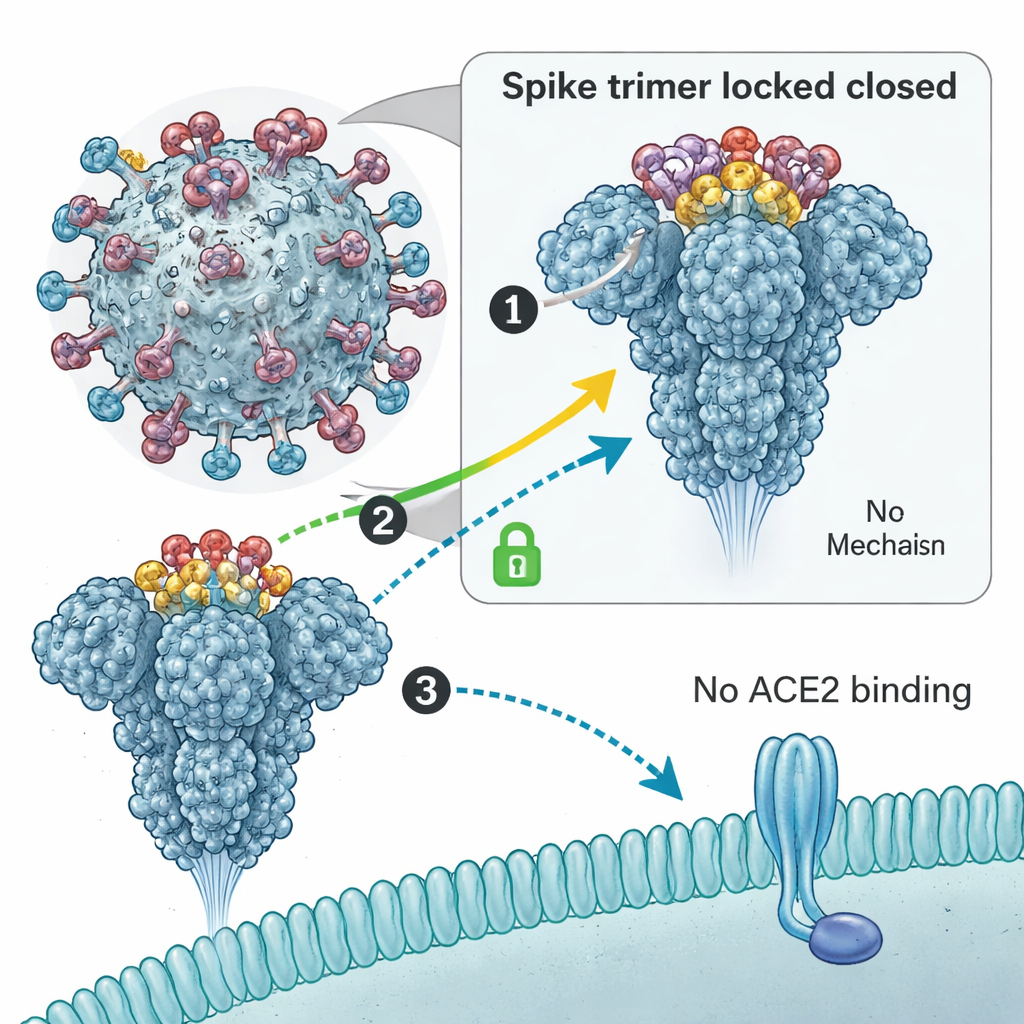
Den Spike zukleben
Um zu verstehen, wie diese Ringe das Virus stoppen, nutzte das Team Kryo-Elektronenmikroskopie, um sie gebunden am Spike-Protein in hoher Auflösung zu visualisieren. Sie fanden heraus, dass drei Kopien des makrozyklischen Peptids als kleiner Trimer zusammenkommen und in eine Vertiefung an der Spitze des Spikes passen, die aus drei RBDs gebildet wird. Das wirkt wie molekularer Klebstoff und sperrt alle drei RBDs in eine „down“- oder geschlossene Position. In dieser Haltung kann der Spike keines seiner RBDs in die „up“-Stellung bringen, um den ACE2-Rezeptor auf unseren Zellen zu fassen—ein notwendiger erster Schritt für die Infektion. Biophysikalische Messungen bestätigten, dass die Spike-Proteine ihre Fähigkeit verlieren, an ACE2 zu binden, wenn das Peptid vorhanden ist. Wichtig ist, dass das Peptid eine konservierte Region anvisiert, die nicht die übliche Antikörper-Bindungsstelle ist, womit häufige Mutationen in Varianten dieses Taschenstück bislang weitgehend verschont haben.
Vom Reagenzglas zu menschlichem Gewebemodell und Mäusen
Gestützt auf diese strukturellen Erkenntnisse verfeinerten die Wissenschaftler das Molekül, um es stärker und stabiler im Körper zu machen. Eine final optimierte Version, 6L3-1F3P11hR, widersteht dem Abbau durch Enzyme, toleriert Hitze und unterschiedliche pH-Werte und verbleibt beim Einsprühen in Mäusen größtenteils in den Nasengängen, wodurch die Belastung des restlichen Körpers minimiert wird. In im Labor gezüchteten humanen Nasen-Organoiden—dreidimensionalen Kulturen, die die echte Nasenschleimhaut nachahmen—verminderte dieses Peptid die Replikation aktueller Omikron-Varianten deutlich, selbst in niedrigen Dosen. In gentechnisch veränderten Mäusen, die humanes ACE2 exprimieren und eine schwere, COVID-ähnliche Lungenerkrankung entwickeln, reduzierte die intranasale Gabe des Peptids, kurz vor oder nach der Infektion verabreicht, die Virusmengen in Nase und Lunge, schützte das Lungengewebe vor Schäden und zeigte in diesen Tests eine vergleichbare Wirksamkeit mit der zugelassenen antiviralen Tablette Nirmatrelvir (Bestandteil von Paxlovid).
Den künftigen Varianten einen Schritt voraus
Weil das Peptid an eine hochkonservierte „nicht-rezeptorbindende“ Stelle des Spikes bindet und durch einen physikalischen Verriegelungsmechanismus wirkt statt ein einzelnes virales Enzym anzugreifen, könnte es für das Virus schwieriger sein, diesem Mechanismus auszuweichen, ohne seine eigene Infektionsfähigkeit zu beeinträchtigen. Die Autorinnen und Autoren zeigen außerdem, dass einfache Punktänderungen in der Peptidsequenz dessen Stärke und Wirkspektrum feinjustieren können, was einen Weg aufzeigt, das Arzneimittel künftig gegen verwandte Coronaviren anzupassen. Ihre pharmakokinetischen Studien deuten darauf hin, dass sich die Verbindung dort anreichert, wo das Virus zuerst landet—den Nasengängen—was sie zu einer logischen Kandidatin für ein präventives Spray oder eine frühzeitige Behandlung macht, die zu Hause angewendet werden könnte.
Was das für den Alltags-Schutz bedeuten könnte
Für Nicht-Fachleute lautet die Kernbotschaft: Diese Arbeit liefert einen gut charakterisierten, nasenapplizierten antiviralen Kandidaten, der das Coronavirus-Spike physikalisch zuklemmt und so daran hindert, an unsere Zellen anzudocken. In Zellkulturen, in menschlich anmutenden Nasengeweben und in einem empfänglichen Mäusemodell senkte das optimierte makrozyklische Peptid die Viruslast und Lungenschäden bei vielen Omikron-Subvarianten und einigen früheren Stämmen deutlich. Zwar sind noch klinische Studien am Menschen nötig, doch weist diese Strategie in Richtung einer Zukunft, in der ein lagerfähiges Nasenspray kurzfristigen Schutz und Behandlung gegen aktuelle und neu auftauchende SARS-CoV-2-Varianten und möglicherweise auch gegen andere verwandte Coronaviren bieten könnte.
Zitation: Wang, M., Yang, J., Tan, Y. et al. Intranasal administration of broad-spectrum macrocyclic peptide inhibitor protects against SARS-CoV-2 Omicron variants. Nat Commun 17, 1753 (2026). https://doi.org/10.1038/s41467-026-68462-9
Schlüsselwörter: COVID-19, SARS-CoV-2-Varianten, nasenspray antiviral, Spike-Protein-Inhibitor, makrozyklisches Peptid