Clear Sky Science · de
Chromatin-Architektur an einem einzelnen Locus durch probabilistische in situ-DNA-Lokalisierung erschließen
Wie die 3D‑Form der DNA steuert, wann Gene aktiviert werden
Unsere DNA wird oft als gerade Leiter dargestellt, doch in Zellen faltet sie sich zu komplexen Schleifen und Spiralen. Diese Formen sind bedeutsam: Sie beeinflussen, welche Gene aktiviert werden, wann und wo. In dieser Studie wird eine neue Methode vorgestellt, um die winzigen 3D‑Anordnungen der DNA um ein einzelnes Gen in sich entwickelnden Fruchtfliegen‑Embryonen zu untersuchen. Sie zeigt, wie subtile Verschiebungen in der DNA‑Faltung Muster der Genaktivität verändern können, die den Körperplan formen.
Genregulation in einem sich entwickelnden Embryo beobachten
Während der Embryonalentwicklung müssen Tausende Gene zur richtigen Zeit an‑ und ausgeschaltet werden. Viele dieser Entscheidungen trifft kurze DNA‑Abschnitte, sogenannte Enhancer, die zehntausende Basenpaare von den Genen entfernt liegen können, die sie steuern. Damit sie wirken, müssen Enhancer sich im 3D‑Raum dem Zielgen annähern und die DNA so schleifen, dass entfernte Stellen in Kontakt treten. Diese Schleifen sind jedoch winzig, dynamisch und schwer zu sehen. Die Autorinnen und Autoren konzentrierten sich auf ein einzelnes Gen, brinker (brk), in der Fruchtfliege Drosophila. Dieses Gen hilft, das frühe Embryo zu vermustern und wird in einem Streifen entlang der Seite des Eis aktiviert. Drei nahegelegene Kontrollelemente – zwei Enhancer (E1 und E2) und ein promoter‑nahes Element (PPE) neben dem Gen – arbeiten zusammen, um dieses präzise Muster zu erzeugen.
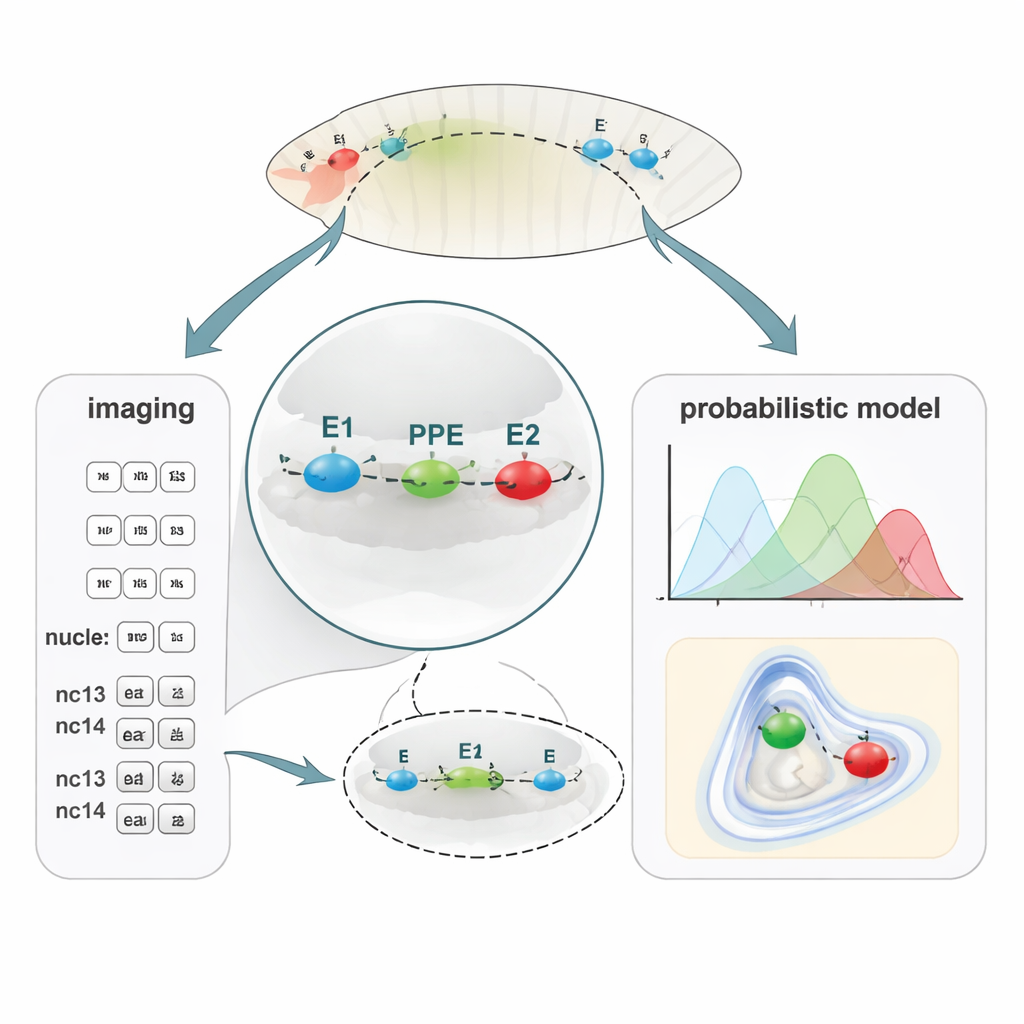
Eine neue Methode, winzige DNA‑Abstände zu kartieren
Um die DNA‑Faltung mit Genaktivität zu verknüpfen, entwickelte das Team PLOTTED (Probabilistic Localization of Oligopaint Tagged Target Element Distances). Zuerst nutzten sie die DNA‑Markierungsmethode Oligopaint FISH, um drei verschiedene fluoreszierende Farben an die Regionen E1, PPE und E2 in fixierten Fliegen‑Embryonen zu bringen. Mit einem superauflösenden Konfokalmikroskop maßen sie die 3D‑Abstände zwischen diesen drei farbigen Punkten in Zehntausenden von Zellkernen aus Embryonen in aufeinanderfolgenden Kernzyklen, von kurz vor Beginn der Genaktivität (pre‑nc13) bis zu späteren Stadien (nc13 und nc14). Alle diese Abstände flossen in eine maßgeschneiderte Rechenpipeline, die verrauschte Messungen herausfiltert und Wahrscheinlichkeitstagskarten erstellt, die zeigen, wo sich jedes Element mit welcher Wahrscheinlichkeit relativ zu den anderen befindet. Anstatt einer einzigen statischen »Schleife« liefert PLOTTED eine Landschaft wahrscheinlicher Chromatin‑Formen für jedes Entwicklungsstadium.
Wenn DNA sich verdichtet, erwacht das Gen
In normalen Embryonen beobachteten die Forschenden, dass mit Erreichen des Kernzyklus 13 beide Enhancer dem PPE näher rücken: die lokale DNA‑Nachbarschaft um das brk‑Gen wird kompakter. Nach diesem Zeitpunkt bleiben die Abstände zwischen den drei Elementen relativ stabil. Wichtig ist, dass dieses Timing mit dem Beginn der brk‑Expression übereinstimmt, was darauf hindeutet, dass die Verdichtung der DNA‑Konfiguration dazu beiträgt, das Gen einzuschalten. PLOTTED zeigte außerdem, dass diese kompakte Anordnung in Regionen des Embryos, in denen brk aktiv ist, häufiger auftritt, während lockerere Konfigurationen in Bereichen dominieren, in denen das Gen reprimiert ist. Das stärkt den Zusammenhang zwischen 3D‑Architektur und Transkription.
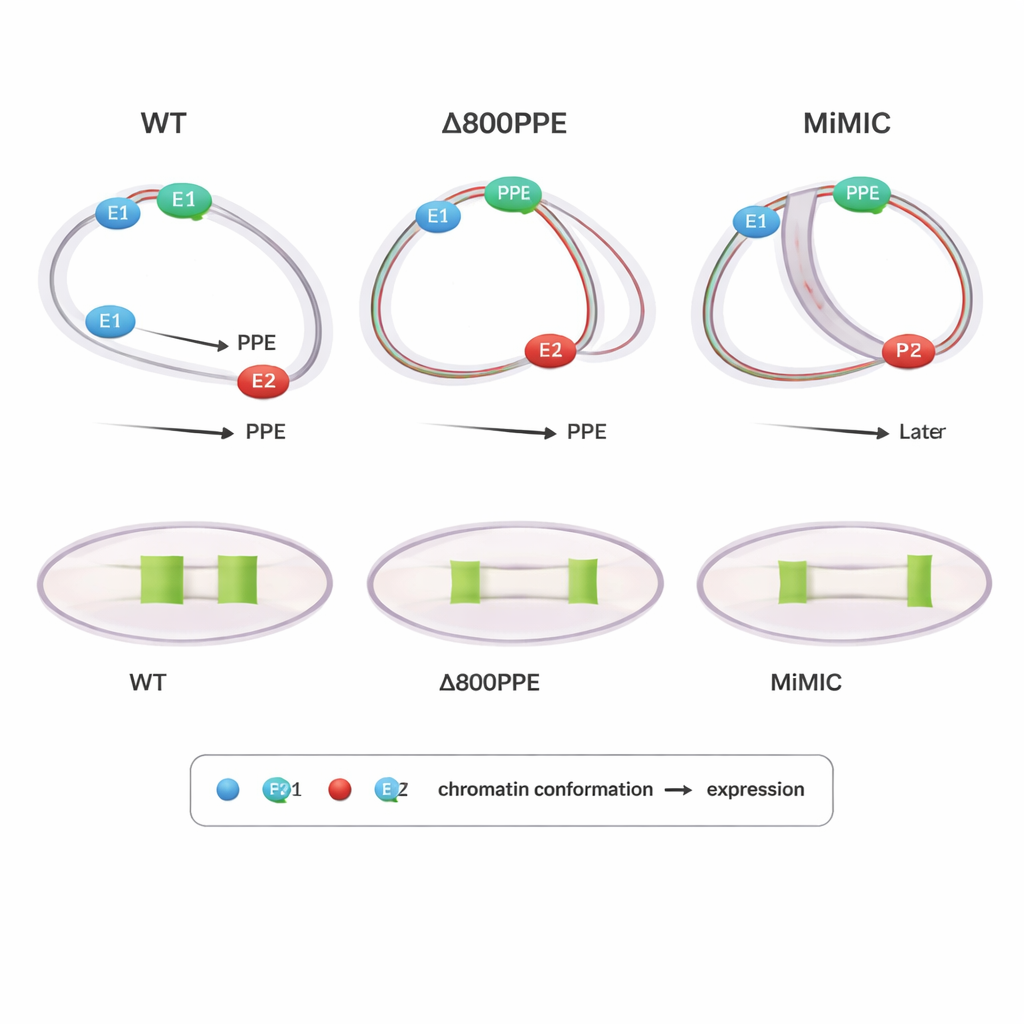
Mutationen zeigen, wie Timing und Position zählen
Um Ursache und Wirkung zu prüfen, untersuchten die Autorinnen und Autoren Fliegen mit gezielten Veränderungen am brk‑Locus. In einer Mutante wurden 800 Basenpaare des PPE gelöscht, wodurch dieses zentrale Element abgeschwächt wurde; in einer anderen wurde eine 7,3 Kilobasen lange DNA‑Kassette (MiMIC) zwischen E1 und dem PPE eingefügt, wodurch sie effektvoll weiter auseinandergerückt und zusätzlich ein weiterer Promoter eingebracht wurde. Beide Mutanten zeigten verzögerte oder reduzierte brk‑Expression. PLOTTED erklärte warum: In der PPE‑Deletion trat die Kompaktierung der Abstände zwischen PPE und beiden Enhancern später als normal auf, und in späten Stadien blieb das PPE zu nah bei E1, wodurch E2 daran gehindert wurde, das breite Expressionsmuster zu treiben, das im Wildtyp zu sehen ist. In der MiMIC‑Linie assoziierte das PPE zu früh und zu stark mit E2 und zog erst später näher zu E1, was erneut die normale Übergabe zwischen den Enhancern störte. Diese Ergebnisse legen nahe, dass nicht nur das Ob des Zusammentreffens von Elementen wichtig ist, sondern auch das Wann und mit welchem Partner sie am nächsten stehen, entscheidend für das richtige Genprodukt ist.
Die DNA‑Faltung variiert im Embryo
Weil PLOTTED räumliche Information in intakten Embryonen bewahrt, konnte das Team auch untersuchen, ob sich die DNA‑Architektur in verschiedenen Körperregionen unterscheidet. Beim Vergleich seitlicher Zonen, in denen brk aktiv ist, mit ventralen Zonen, in denen es reprimiert wird, stellten sie fest, dass die drei Elemente in aktiven Regionen dichter zusammensitzen und in reprimierten Domänen weiter auseinanderliegen. Entlang der Kopf‑Rumpf‑Achse beobachteten sie, dass sich die E1–PPE‑Abstände vorne anders verändern als hinten im Embryo, was darauf hindeutet, dass regionale Signale die Chromatin‑Architektur anpassen, um Genexpressionsmuster fein zu steuern. Diese Ergebnisse stützen die Vorstellung, dass die 3D‑Anordnung regulatorischer DNA kontextabhängig ist und sowohl Zeit als auch Position im sich entwickelnden Organismus widerspiegelt.
Warum das über Fruchtfliegen hinaus wichtig ist
Vereinfacht gesagt zeigt diese Studie, dass die Art und Weise, wie sich die DNA um ein einzelnes Gen faltet, eng damit verbunden ist, wann und wo dieses Gen aktiviert wird. Die neue PLOTTED‑Methode bietet einen praktikablen Weg, diese winzigen DNA‑Nachbarschaften in intakten Geweben mit weit verbreiteten Mikroskopen und einfacher Chemie in Kombination mit leistungsfähiger probabilistischer Modellierung zu kartieren. Obwohl die Methode an Fliegen‑Embryonen demonstriert wurde, lässt sie sich auf viele Organismen und Krankheitsmodelle anwenden. Da Forschende zunehmend entdecken, dass fehlgefaltetes Chromatin Entwicklungsstörungen und Krebs zugrunde liegen kann, werden Werkzeuge wie PLOTTED helfen, zu zeigen, wie kleine Verschiebungen in der 3D‑Anordnung von Enhancern und Genen große Veränderungen von Zellschicksal und Gesundheit nach sich ziehen können.
Zitation: Le, M.T., McGehee, J., Dunipace, L. et al. Inferring chromatin architecture at a single locus through probabilistic in situ DNA localization. Nat Commun 17, 1752 (2026). https://doi.org/10.1038/s41467-026-68460-x
Schlüsselwörter: Chromatin-Architektur, Enhancer-Promoter-Interaktionen, Drosophila-Embryogenese, Genregulation, Superauflösende Bildgebung