Clear Sky Science · de
Von Neuralleistenzellen stammendes DKK1 und NEDD4 modulieren Wnt-Signale im zweiten Herzfeld, um die Entwicklung des Ausflusstrakts zu steuern
Warum winzige Herzbauer wichtig sind
Das Herz des frühen Embryos beginnt als einfacher Schlauch, muss sich aber rasch zu einem komplexen Organ umbauen, das Blut sowohl in den Körper als auch in die Lungen pumpt. Schon kleine Fehler in diesem Aufbauprozess können schwere angeborene Fehlbildungen verursachen, darunter Zustände, die kurz nach der Geburt operativ behandelt werden müssen. Die vorliegende Studie zeigt, wie zwei Zellgruppen während der Formung des Hauptausgangs des Herzens miteinander kommunizieren, und deckt einen molekularen Defekt auf, der sowohl bei Mäusen als auch beim Menschen zu angeborenen Herzfehlern beitragen kann.
Zwei Teams, die die Herzrampe bauen
Der Teil des Herzens, der das Blut aus den Kammern hinausführt – der Ausflusstrakt – entsteht aus einer Region, dem sogenannten zweiten Herzfeld. Die Zellen dort müssen lange genug als flexible „Vorläufer“ erhalten bleiben, um dem wachsenden Ausflusstrakt hinzugefügt zu werden, und anschließend zur reifen Muskulatur differentiieren. Direkt daneben wandern Neuralleistenzellen, eine mobile Zellpopulation, die beim Aufbau der großen Arterien und Klappen mitwirkt. Frühere Arbeiten deuteten an, dass diese Neuralleistenzellen das zweite Herzfeld beeinflussen, doch wie diese Kommunikation funktionierte, war unklar. 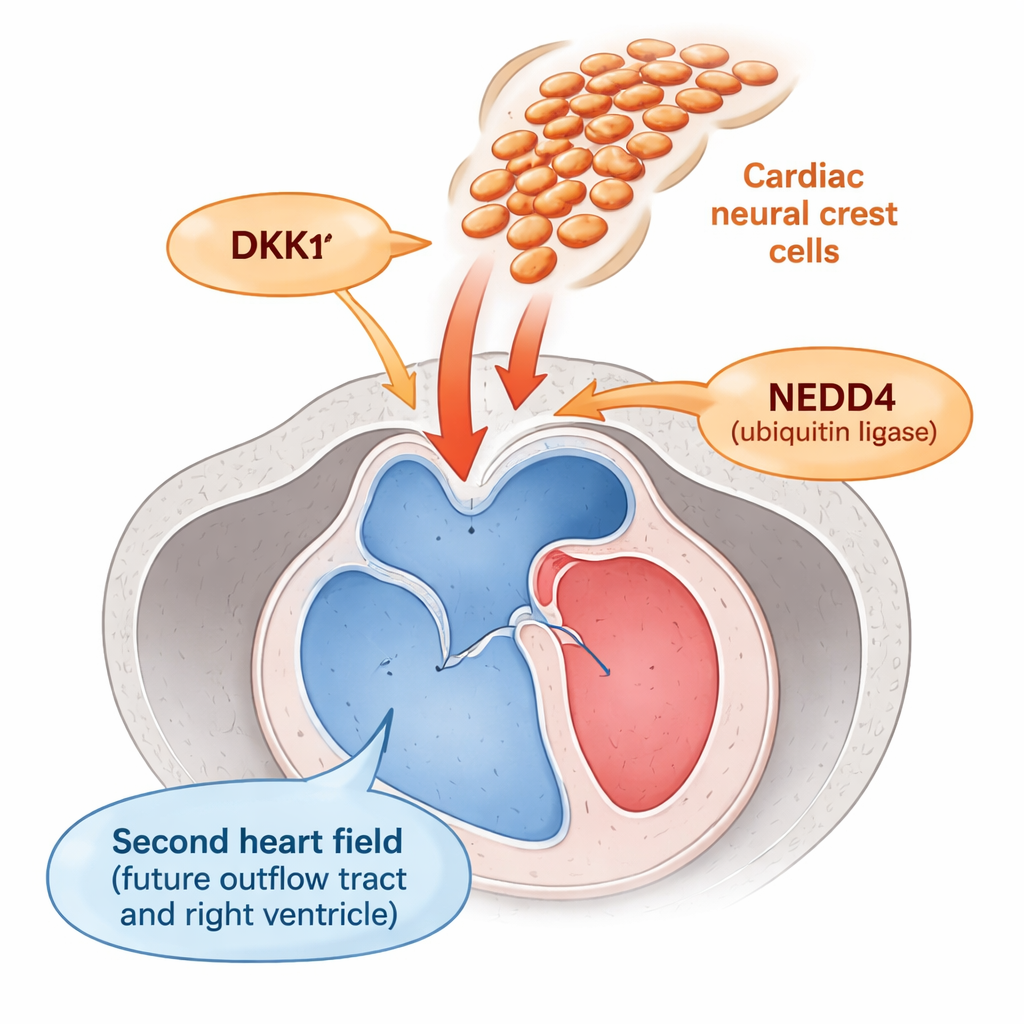
Ein molekularer Dimmschalter für Wachstumssignale
Die Autoren fanden heraus, dass Neuralleistenzellen wie ein Dimmschalter für ein zentrales Wachstumssignal namens Wnt wirken, das Vorläuferzellen proliferieren lässt und ihre Reifung verzögert. Sie entdeckten, dass Neuralleistenzellen eine wichtige Quelle von DKK1 sind, einem kleinen sezernierten Protein, das Wnt-Signale in benachbarten Zellen abschaltet. DKK1 selbst wird normalerweise durch NEDD4 in Schach gehalten, ein Protein, das DKK1 für den Abbau markiert. In Maus-Embryonen, denen Nedd4 speziell in Neuralleistenzellen fehlte, häufte sich DKK1 auf abnormal hohem Niveau an. Dieses überschüssige DKK1 dämpfte die Wnt-Aktivität im benachbarten zweiten Herzfeld, sichtbar durch reduziertes nukleäres beta‑Catenin – ein übliches Maß für Wnt-Signalgebung – sowie geringere Expression mehrerer Wnt-ansprechbarer Gene.
Wenn das Timing falsch läuft, misslingt die Herzgeometrie
Zu viel DKK1 und zu wenig Wnt hatten eine eindeutige Folge: Zellen des zweiten Herzfelds begannen zu früh, sich in Herzmuskel umzuwandeln. Marker reifer Muskulatur traten früh in dieser Vorläuferzone auf, und es blieben weniger undifferenzierte Zellen übrig, um den Ausflusstrakt zu verlängern. Durch zeitliche Verfolgung teilender Zellen zeigte das Team, dass in den Mutanten weniger Zellen des zweiten Herzfelds in den Ausflusstrakt eingebracht wurden. Infolgedessen war der Ausflusstrakt kürzer und falsch rotiert, was zu einer Fehlstellung zwischen den großen Gefäßen und den Kammern führte. Diese strukturellen Fehler glichen menschlichen Konotrunkaldefekten wie dem doppelt ausmündenden rechten Ventrikel und verwandten Fehlbildungen, wie sie auch bei vollständigen Nedd4-Knockout-Mäusen zu sehen sind.
Den Signalweg beweisen und Verbindung zur menschlichen Krankheit
Um zu bestätigen, dass veränderte Wnt-Signalgebung wirklich die Ursache für diese Probleme ist, manipulierten die Forschenden den Weg pharmakologisch bei trächtigen Mäusen. Das Blockieren von Wnt in ansonsten gesunden Embryonen brachte sie in Richtung derselben vorzeitigen Differenzierung und Rotationsfehler, die beim Verlust von Nedd4 beobachtet wurden, während eine Reduktion der Dkk1-Genkopienzahl im Nedd4-defizienten Hintergrund die Größe und Rotation des Ausflusstrakts teilweise rettete. Schließlich identifizierte das Team ein Kind mit Tetralogie der Fallot, das eine seltene vererbte Variante in NEDD4 trug, die dessen Fähigkeit schwächte, DKK1 für den Abbau zu markieren. Mäuse, die mit derselben Nedd4-Variante erzeugt wurden, entwickelten rechtsseitige Wand- und Septumdefekte, was die Idee stützt, dass fehlerhafte NEDD4–DKK1-Regulation zur menschlichen angeborenen Herzkrankheit beitragen kann. 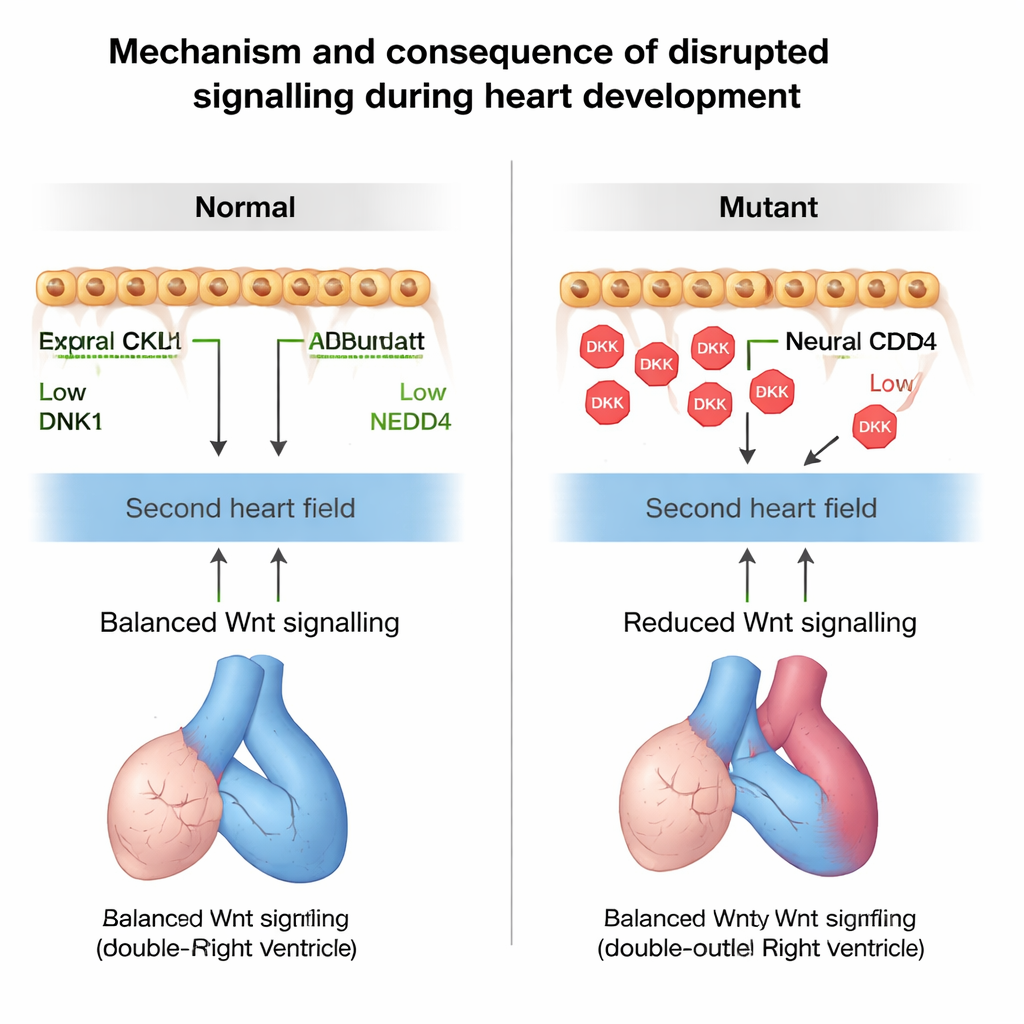
Was das für das Verständnis von Herzfehlern bedeutet
Für Nicht-Spezialisten ist die Kernbotschaft: Die „Ausfahrtsrampe“ des Herzens hängt von einer präzisen Taktung ab, wann ihre Bausteine aufhören sich zu vermehren und anfangen, Muskel zu werden. Dieses Timing wird nicht nur durch gehirneigene Mechanismen gesteuert, sondern auch von benachbarten Neuralleistenzellen feinabgestimmt, die ein Wachstumssignal über das NEDD4–DKK1-Paar regulieren. Wenn dieser molekulare Dimmschalter zu stark gedämpft ist, wird der Ausflusstrakt zu klein und falsch ausgerichtet, was zu schweren angeborenen Fehlbildungen führt. Indem die Studie diesen Signalweg kartiert und ihn mit einer menschlichen Genvariante verknüpft, liefert sie neue Hinweise darauf, wie einige angeborene Herzfehler entstehen, und hebt mögliche molekulare Ziele für zukünftige Diagnostik oder Intervention hervor.
Zitation: Wiszniak, S., Alankarage, D., Lohraseb, I. et al. Neural crest cell-derived DKK1 and NEDD4 modulate Wnt signalling in the second heart field to orchestrate outflow tract development. Nat Commun 17, 1751 (2026). https://doi.org/10.1038/s41467-026-68459-4
Schlüsselwörter: angeborener Herzfehler, Herzentwicklung, Neuralleistenzellen, Wnt-Signalgebung, kardialer Ausflusstrakt