Clear Sky Science · de
Af-CUT&Tag: eine empfindliche und antikörperfreie Methode zur Chromatinkartierung mit genetisch kodierten Tags und hochaffinen Bindern, die an Tn5 fusioniert sind
Ein Blick in unseren DNA-Schaltraum
Jede Zelle in Ihrem Körper entscheidet ständig, welche Gene ein- oder ausgeschaltet werden, und bestimmt damit alles von Leberreparatur bis Krebsrisiko. Wissenschaftler untersuchen diese Entscheidungen, indem sie kartieren, wo wichtige Proteine an unserer DNA sitzen; die besten Werkzeuge dafür beruhten jedoch lange auf fragilen, teuren Antikörpern, die nicht immer zuverlässig funktionieren. Diese Arbeit stellt eine neue, antikörperfreie Methode zur Darstellung von DNA–Protein-Interaktionen vor, Af-CUT&Tag, die sensitiver, verlässlicher und leistungsfähig genug ist, um sogar mit winzigen Proben und Einzelzellen zu arbeiten.
Warum Antikörper uns ausbremsen
Klassische Methoden zur Chromatinkartierung benötigen Antikörper – große Y-förmige Proteine, die ein bestimmtes Zielprotein erkennen –, um ein Enzym zu den richtigen Stellen auf der DNA zu führen. Wenn Antikörper perfekt funktionieren, erlauben sie Forschern zu sehen, wo Transkriptionsfaktoren und andere Regulatoren im Genom gebunden sind. In der Praxis sind Antikörper jedoch oft schwer zu beschaffen, in ihrer Qualität inkonsistent und können durch häufige chemische Modifikationen an Proteinen wie Phosphorylierung oder Acetylierung blockiert werden. Diese Probleme können die resultierenden Karten verschwimmen lassen, die untersuchbaren Proteine einschränken und Vergleiche zwischen Laboren oder Experimenten erschweren.
Kleine Tags und clevere Binder ersetzen Antikörper
Af-CUT&Tag umgeht Antikörper vollständig, indem das interessierende Protein einen winzigen genetischen Namensschild erhält. Mittels CRISPR-Genomeditierung fügen die Forschenden kurze Peptid-Tags wie HiBiT oder ALFA an das natürliche Protein in Zellen oder Geweben an. Anschließend verwenden sie gentechnisch veränderte Partnerproteine – hochaffine Binder, die diese Tags erkennen –, die direkt an das Tn5-Enzym fusioniert sind; dieses Enzym schneidet DNA und hängt Sequenzieradapter an. Wenn die Binder–Tn5-Fusion am Tag des Zielproteins ansetzt, schneidet sie die umliegende DNA und markiert diese Stellen für die Sequenzierung. Da die Tags sehr klein sind und die Binder–Tn5-Fusion deutlich kleiner als ein Antikörper ist, dringt das System leicht in Zellen und Zellkerne ein, bindet mit außergewöhnlicher Präzision und lässt sich nicht durch chemische Modifikationen des Zielproteins stören. 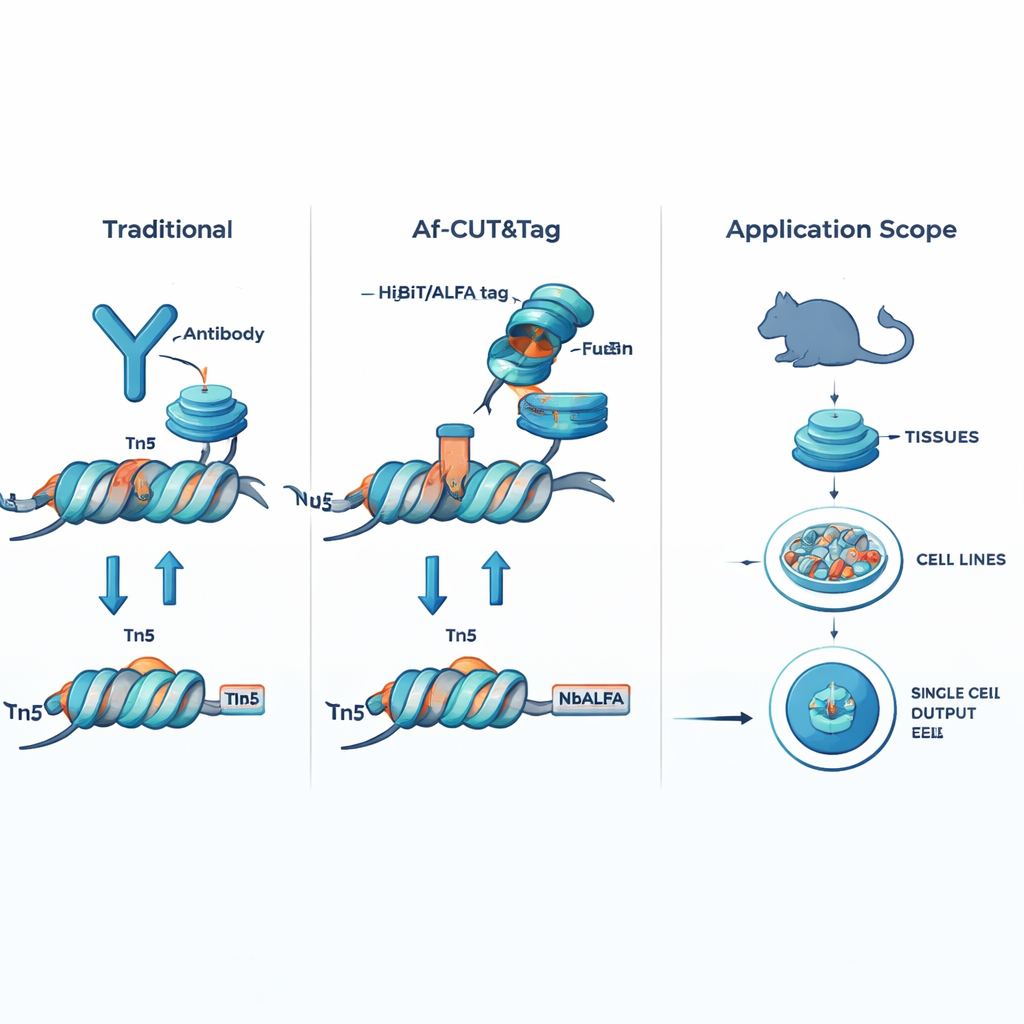
Scharfere Karten aus weniger Zellen
Das Team zeigte zunächst, dass ihre Binder–Tn5-Fusionen die Tags weiterhin sehr fest greifen und DNA effizient schneiden. Danach verglichen sie Af-CUT&Tag mit modernen, antikörperbasierten Methoden zur Kartierung der RNA-Polymerase II, des Enzyms, das proteinkodierende Gene abliest, sowie des CTCF-Proteins, einem wichtigen Organisator der Genomstruktur. In menschlichen Zelllinien erzeugte Af-CUT&Tag ein saubereres Signal an Genstartstellen, weniger Off-Target-Schnitte in offenen, aber irrelevanten DNA-Regionen und qualitativ hochwertigere Sequenzierbibliotheken. Bemerkenswert ist, dass robuste Karten bereits aus etwa 500 Zellen erzeugt werden konnten, und dieselbe Strategie ließ sich auf viele verschiedene Binder ausdehnen, die unterschiedliche DNA-Merkmale anvisieren. Die Methode wurde außerdem auf Einzelzellen erweitert, indem die Fragmente jeder Zelle barcodiert wurden, was den Aufbau detaillierter, zellindividueller Chromatin-Karten ermöglichte.
Leberreparatur in Echtzeit verfolgen
Um zu demonstrieren, was diese Technologie in lebenden Tieren offenlegen kann, wendeten die Autoren Af-CUT&Tag auf die Leberregeneration von Mäusen an. Sie nutzten Viren und CRISPR, um HiBiT-Tags an zwei Schlüsselregulatoren der „Hippo“-Signalgebung, YAP1 und TAZ, anzubringen, die Größe und Reparatur von Organen steuern. Nach teilweiser Leberentfernung isolierten sie Leberzellkerne vor der Operation und 24 Stunden danach und verwendeten Af-CUT&Tag, um zu sehen, wo YAP1 und TAZ im Genom gebunden waren. Die Karten zeigten, dass diese Proteine früh nach der Verletzung ihre Präsenz an Genen reduzieren, die Fettverarbeitung und -synthese antreiben, während Leberzellen vorübergehend Fetttröpfchen ansammeln. Gleichzeitig nehmen YAP1/TAZ die Bindung an Gene zu, die an der Entfernung von Häm beteiligt sind – einem potenziell toxischen Blutbestandteil – sowie an Mir122, einem Gen, das ein in der Leber stark angereichertes microRNA produziert.
miR-122 als Wächter der Regeneration
miR-122 ist ein kleines RNA-Molekül, das die Aktivität vieler anderer Gene fein abstimmt. Mit Af-CUT&Tag beobachteten die Forschenden stärkere YAP1/TAZ-Bindung in der Nähe der Mir122-Region, verbunden mit offenerem Chromatin und verstärkten chemischen Markern, die mit Genaktivierung assoziiert sind. Experimente bestätigten, dass die miR-122-Level während des frühen Regenerationsfensters ansteigen. Wenn das Team miR-122 gezielt in Leberzellen von Mäusen entfernte, zeigten die Tiere stärkere Fettansammlungen, ausgeprägtere entzündliche Reaktionen und weniger Leberzellen, die nach der Operation in den Zellzyklus eintraten. Zusammengenommen deuten diese Ergebnisse darauf hin, dass YAP1/TAZ der Leber helfen, während der Reparatur ein sorgfältiges Gleichgewicht zu halten: kurzzeitig Fett als Energiequelle anzulegen, Schäden durch Häm und Entzündung zu begrenzen und miR-122 zu nutzen, um übermäßigen Stress einzudämmen, während das Gewebe nachwächst. 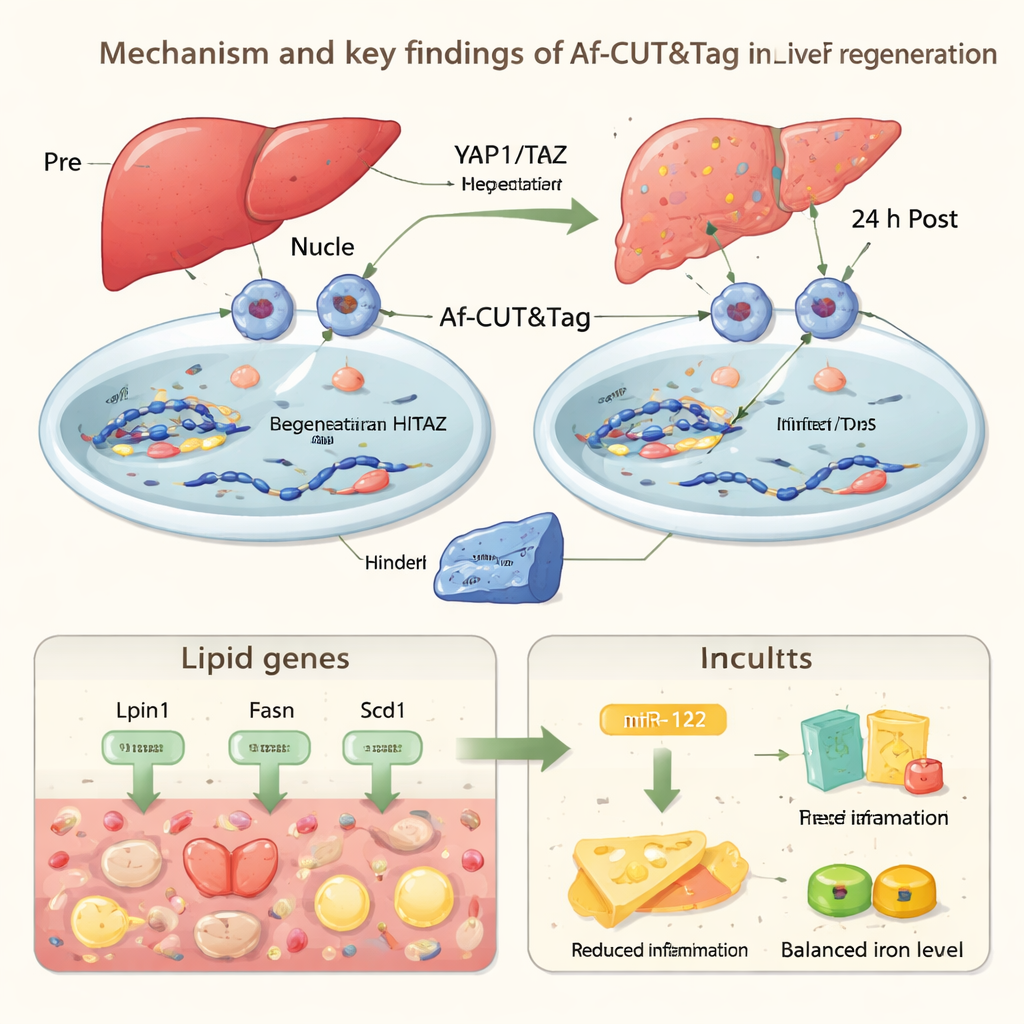
Ein vielseitiges neues Instrument zur Gensteuerung
Af-CUT&Tag bietet einen modularen, antikörperfreien Weg, um zu sehen, wo Schlüsselproteine in Zelllinien, Geweben und sogar Einzelzellen auf der DNA sitzen. Indem unberechenbare Antikörper durch kleine genetische Tags und designte Binder ersetzt werden, liefert die Methode schärfere, reproduzierbarere Karten aus deutlich weniger Zellen. Auf die Leberregeneration angewandt, zeigte sie, wie YAP1 und TAZ Stoffwechsel, Eisenhandhabung und das microRNA miR-122 koordinieren, um frühe Reparaturprozesse zu unterstützen. Mit fortschreitender Verbesserung von Genomeditierung und maßgeschneiderten Bindern könnte diese Strategie zu einem Standardwerkzeug werden, um zu untersuchen, wie Genregulation in Entwicklung und Regeneration gelingt – und wie sie bei Krankheiten wie Krebs und Leberversagen fehlgeht.
Zitation: Wang, X., Deng, X., Qiu, L. et al. Af-CUT&Tag: a sensitive and antibody-free chromatin profiling method using genetically encoded tags and high-affinity binders fused to Tn5. Nat Commun 17, 1746 (2026). https://doi.org/10.1038/s41467-026-68454-9
Schlüsselwörter: Chromatinkartierung, Epigenetik, Leberregeneration, YAP1 TAZ, microRNA-122