Clear Sky Science · de
Funktionelle Varianten bei 1p36.23 erhöhen das Schizophrenie-Risiko durch Modulation von RERE
Warum winzige DNA-Veränderungen für die psychische Gesundheit wichtig sind
Schizophrenie ist eine ernsthafte psychische Erkrankung, die Denken, Fühlen und das Verhältnis zu anderen beeinträchtigt. Sie tritt familiär gehäuft auf, doch die meisten beteiligten genetischen Veränderungen sind kleine, verstreute Modifikationen in unserer DNA. Diese Studie richtet den Fokus auf eine solche Genomregion und zeigt Schritt für Schritt, wie zwei subtile DNA-Varianten die Entwicklung und Kommunikation von Gehirnzellen verändern können, sodass das Schizophrenie-Risiko einer Person steigen könnte. 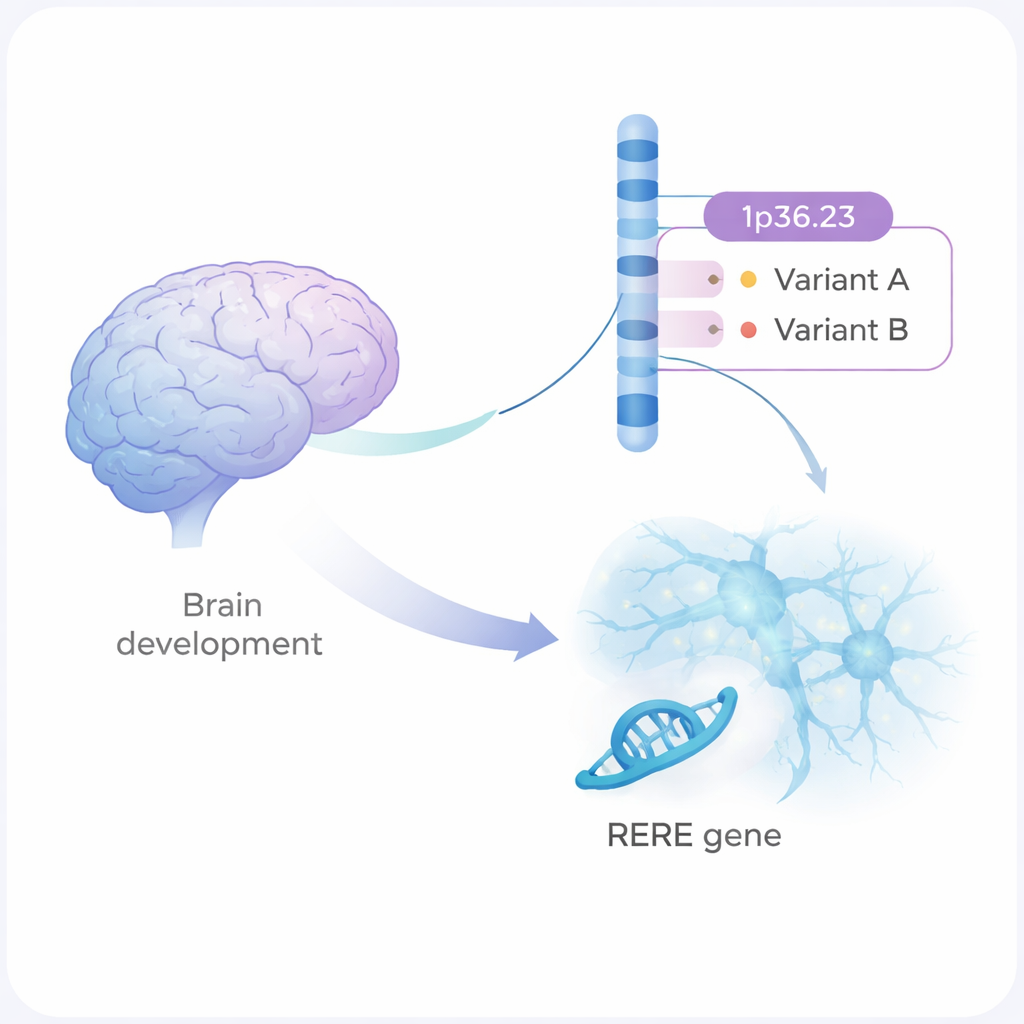
Ein genetischer Hotspot auf Chromosom 1
Große genetische Studien haben mehr als 300 Regionen im menschlichen Genom identifiziert, die mit Schizophrenie in Verbindung stehen. Eine davon liegt auf Chromosom 1 und wird 1p36.23 genannt. Bislang war unklar, welche genauen Veränderungen in dieser Region oder welches Gen die eigentliche Wirkung erklären. Die Autorinnen und Autoren kombinierten statistische Genetik mit Laborexperimenten und identifizierten zwei DNA-Varianten, rs159961 und rs301792, die innerhalb des Gens RERE liegen. Diese Varianten verändern nicht das RERE-Protein selbst; vielmehr befinden sie sich in regulatorischen „Schalter“-Bereichen innerhalb des Gens, die steuern, wie stark RERE angeschaltet wird.
Wie Risikovarianten die Lautstärke von RERE erhöhen
Das Team untersuchte zunächst, ob diese beiden Varianten tatsächlich als funktionelle Schalter wirken. Mit Reporter-Assays — Tests, bei denen ein DNA-Fragment ein lichtproduzierendes Gen antreibt — zeigten sie, dass die mit Schizophrenie assoziierten Allele von rs159961 und rs301792 in nervenähnlichen Zellen wie stärkere Enhancer (Verstärker) wirken, nicht jedoch in unzusammenhängenden Zelltypen. Biochemische Bindungsuntersuchungen erklärten warum: Die Risikoform der einen Variante schwächt die Bindung von REST, einem Protein, das normalerweise die Genaktivität dämpft, während die Risikoform der anderen Variante die Bindung von POLR2A, einem Kernbestandteil der Transkriptionsmaschinerie, verstärkt. Zusammen erhöhen diese Verschiebungen in der Proteinbindung die Aktivität der Enhancer-Abschnitte und treiben die RERE-Expression nach oben.
Von erhöhtem RERE zur veränderten Entwicklung von Gehirnzellen
Als Nächstes fragten die Forschenden, welche Folgen ein Überschuss an RERE im Gehirn hat. Sie fanden, dass Menschen mit diagnostizierter Schizophrenie in ihrem Hirngewebe höhere RERE-Level aufwiesen als unbetroffene Individuen. Um dies zu modellieren, erhöhten sie künstlich RERE in Maus-neuralen Stammzellen — unreifen Zellen, die zu Neuronen und Gliazellen heranreifen. Bei RERE-Überexpression teilten sich diese Stammzellen weniger, blieben in einem späten Zellzyklusstadium stecken und produzierten weniger reife Neuronen, während andere Zelltypen weitgehend unverändert blieben. In kultivierten Neuronen veränderte zu viel RERE außerdem die Verzweigungsmuster und verringerte Anzahl und Art winziger Ausstülpungen, sogenannter dendritischer Dornen (dendritic spines), an denen Synapsen entstehen. Diese Befunde passen zu langjährigen Hinweisen darauf, dass Schizophrenie mit gestörter Gehirnentwicklung und Verlust von Dornen einhergeht. 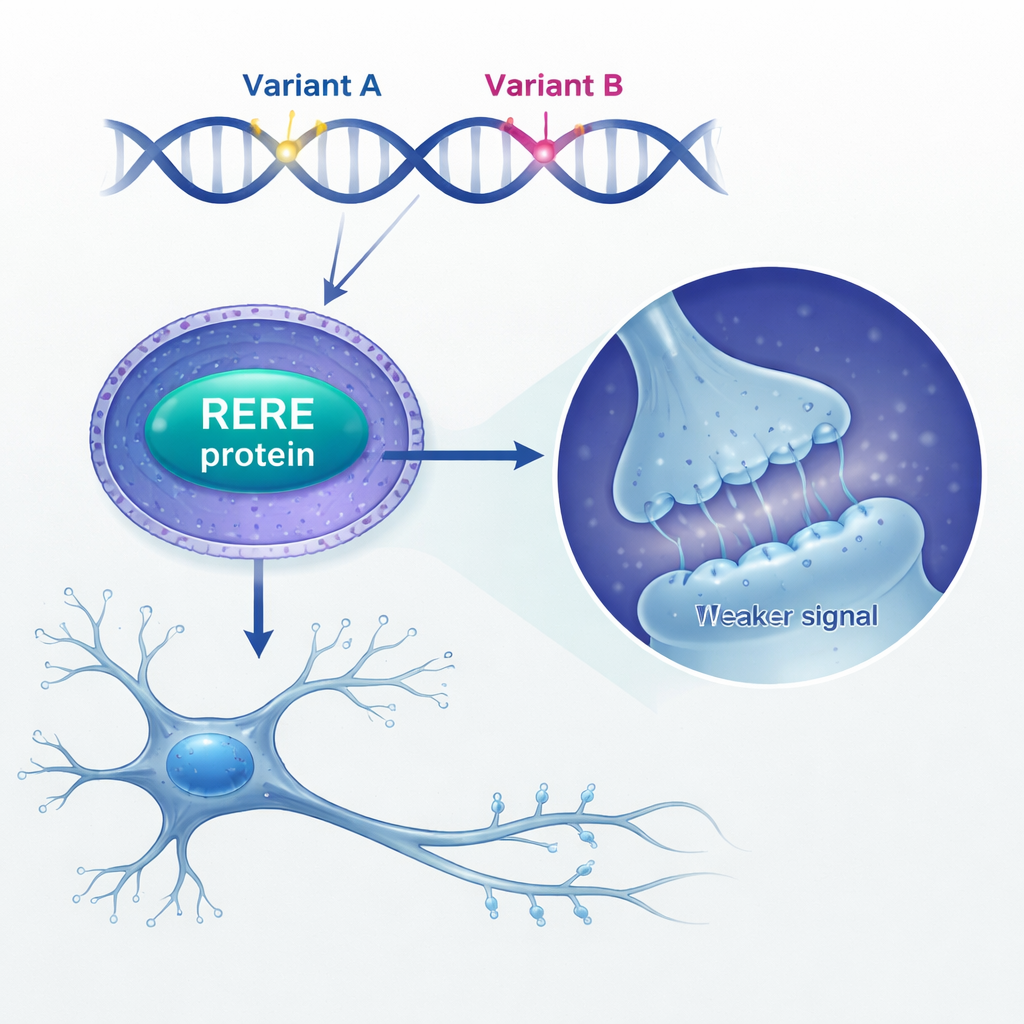
Störung der glutamatenen „Konversation“ im Gehirn
Bei genauerer Betrachtung der Genaktivität stellten die Forschenden fest, dass RERE-Überexpression Netzwerke von Genen störte, die an Dendritenwachstum und wichtigen chemischen Signalwegen beteiligt sind, insbesondere am Glutamatweg. Ein wichtiges Ziel stach heraus: das Gen GRIN2A, das eine zentrale Untereinheit (GluN2A) von NMDA-Glutamatrezeptoren kodiert und seit langem mit Schizophrenie in Verbindung gebracht wird. Die Autorinnen und Autoren zeigten, dass RERE zusammen mit zwei anderen nukleären Proteinen, RARB und RXRA, direkt an den Promotor von GRIN2A bindet und dessen Aktivität dämpft. In Neuronen mit überschüssigem RERE sanken die GluN2A-Spiegel, und elektrophysiologische Messungen zeigten abgeschwächte NMDA-Rezeptor-vermittelte synaptische Ströme, obwohl die Frequenz synaptischer Ereignisse unverändert blieb. Anders gesagt: Die „Lautstärke“ einzelner erregender Signale wurde heruntergeregelt.
Verbindung von DNA-Varianten zur Gehirnfunktion
Indem die Studie Genetik, Molekularbiologie, Zellkultur und Elektrophysiologie verknüpft, zeichnet sie eine klare Kausalkette nach: Risikovarianten bei 1p36.23 verstärken regulatorische Elemente innerhalb des RERE-Gens und führen zu höherer RERE-Expression in Gehirnzellen. Erhöhtes RERE beeinträchtigt wiederum das Wachstum und die Reifung von Neuronen, verändert Form und Anzahl ihrer synaptischen Dornen und schwächt glutamaterge Signalübertragung über NMDA-Rezeptoren — besonders solche mit GluN2A. Für Laien lautet die Kernbotschaft: Sehr kleine DNA-Veränderungen können die Aktivität eines einzelnen Gens leicht verschieben, und über viele Gehirnzellen hinweg und über viele Jahre können solche Verschiebungen die Gehirnentwicklung und -kommunikation in eine Richtung lenken, die zur Entstehung von Schizophrenie beiträgt.
Zitation: Liu, Y., Wang, J., Yang, H. et al. Functional variants at 1p36.23 confer risk of schizophrenia through modulating RERE. Nat Commun 17, 1742 (2026). https://doi.org/10.1038/s41467-026-68449-6
Schlüsselwörter: Genetik der Schizophrenie, RERE-Gen, Neuroentwicklung, Glutamatsignalgebung, synaptische Funktion