Clear Sky Science · de
Konstruktion entfernter dualer Stereozentren durch elektrochemisch cobalt-katalysierte enantioselektive Desymmetrisierung
Moleküle formen für bessere Medikamente
Chemiker wissen seit Langem, dass die 3‑dimensionale Gestalt eines Moleküls das Wirkspektrum eines Arzneimittels im Körper entscheidend beeinflussen kann. Viele erfolgreiche Medikamente und Katalysatoren funktionieren nur, weil bestimmte Atome in genau den richtigen Richtungen im Raum zeigen. Zwei weit auseinanderliegende „Steuerpunkte“ in einem einzigen Schritt präzise anzuordnen, war jedoch extrem schwierig. Diese Studie stellt eine elektrisch angetriebene Methode vor, die mit einem einzelnen cobaltbasierten Katalysator Moleküle mit zwei weit entfernten Stereozentren — entscheidenden 3‑D‑Merkmalen — formt und so neue Möglichkeiten für die Gestaltung von Arzneimitteln und speziellen chemischen Werkzeugen eröffnet.
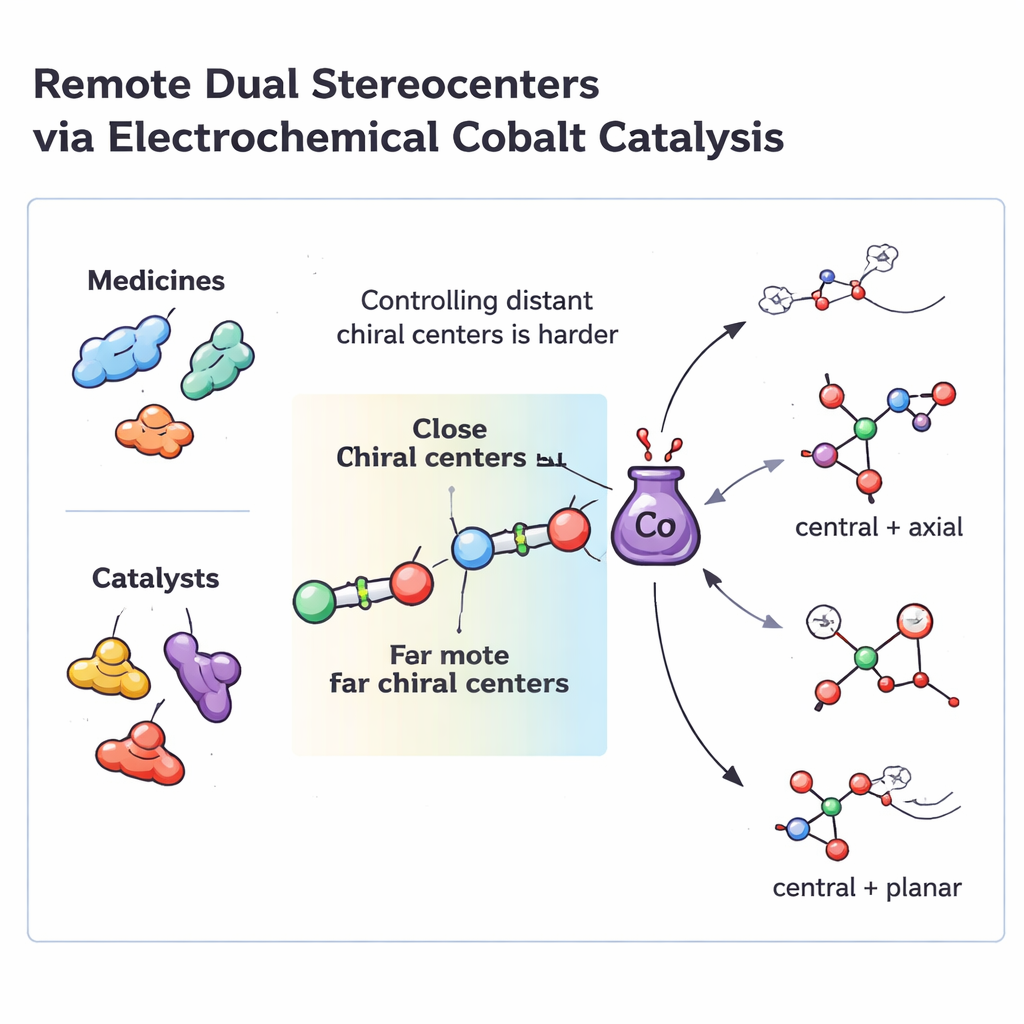
Warum entfernte Steuerpunkte wichtig sind
Viele moderne Medikamente und Hochleistungskatalysatoren enthalten zwei nicht benachbarte Stereozentren — spezifische Anordnungen von Atomen, die als links- oder rechtsgängige Formen existieren können. Diese entfernten Steuerpunkte sind oft ausschlaggebend dafür, wie ein Molekül in ein biologisches Ziel oder an ein Metallzentrum in einem Katalysator passt. Traditionelle asymmetrische Methoden sind sehr gut darin, benachbarte Stereozentren zu erzeugen, bei denen die beiden Punkte direkt nebeneinander liegen. Sind die Punkte jedoch durch fünf oder mehr Atome getrennt, versagen die üblichen „Steuer“-Modelle, und Chemiker benötigen häufig mehrstufige Syntheserouten oder zwei verschiedene Katalysatoren im Zusammenspiel. Solche Multi‑Katalysator‑Systeme sind schwer zu optimieren, anfällig für Inkompatibilitäten und meist nur für eng verwandte Ausgangsmaterialien geeignet.
Eine Ein‑Katalysator‑Abkürzung mit elektrischer Unterstützung
Die Autoren gingen dieses Problem an, indem sie Elektrochemie mit einem chiralen Cobalt‑Katalysator kombinierten. Anstelle chemischer Reduktionsmittel setzten sie einen kleinen elektrischen Strom in einer einfachen Zelle mit Zink‑ und Nickel-Elektroden ein. Dieser Strom verwandelt einen Cobaltkomplex mit chiraler Liganden in eine reaktive, niedrigvalente Spezies, die einfache Ausgangsmaterialien binden und umformen kann: symmetrische Dialdehyde und sogenannte Enyne, die sowohl eine Doppel- als auch eine Dreifachbindung enthalten. Der Schlüsselgedanke ist die Desymmetrisierung: Aus Molekülen mit zwei äquivalenten „Enden“ wird durch den chiralen Cobalt die Balance in kontrollierter Weise gebrochen, sodass jedes Ende Teil einer klar definierten 3‑D‑Struktur wird.
Symmetrie in Vielfalt verwandeln
Unter optimierten Bedingungen wandelt dieser elektrochemische Prozess zuverlässig eine große Bandbreite an Dialdehyden und Enynen in Produkte um, die zwei unterschiedliche chirale Elemente an entfernten Positionen enthalten. Je nach Ausgangsgerüst kann das Team in derselben vereinheitlichten Vorgehensweise vier verschiedene Arten von 3‑D‑Anordnungen erzeugen: ein zentrales Stereozentrum kombiniert mit einer verdrehten C–C‑Achse, ein zentrales Stereozentrum mit einer verdrehten C–O‑Achse sowie zwei Formen planarer Chiralität auf Basis von [2.2]paracyclophan‑ und Ferrocen‑Gerüsten. Praktisch bedeutet das, dass sie Molekülfamilien herstellen können, deren Gestalt jahrelang im Raum fixiert bleibt, mit sehr hoher Selektivität für eine 3‑D‑Form gegenüber allen anderen und mit Toleranz für viele verschiedene Substituenten an den aromatischen Ringen.
Ein Blick unter die Haube der Reaktion
Um zu verstehen, wie dieser Prozess abläuft, nutzten die Forscher Markierungsexperimente und mechanistische Untersuchungen. Durch das Ersetzen bestimmter Wasserstoffatome durch Deuterium (ein schwereres Isotop von Wasserstoff) zeigten sie, dass diese Atome im Endprodukt genau an den erwarteten Positionen landen und kein Austausch zwischen verschiedenen Molekülen stattfindet. Das schließt einige konkurrierende Reaktionswege aus und stützt einen schrittweisen Mechanismus, bei dem der Cobalt‑Katalysator zunächst ein ringförmiges Zwischenprodukt mit dem Enyn bildet und so das erste Stereozentrum etabliert. Das Dialdehyd fügt sich dann in dieses Zwischenprodukt ein und erzeugt das zweite Stereozentrum, gefolgt von Schritten, die das Produkt freisetzen und die aktive Cobalt‑Spezies regenerieren. Das Team zeigte außerdem, dass die Produkte weiter modifiziert werden können — oxidiert, gekoppelt oder in Liganden verwandelt — ohne die fein abgestimmte 3‑D‑Kontrolle zu verlieren.
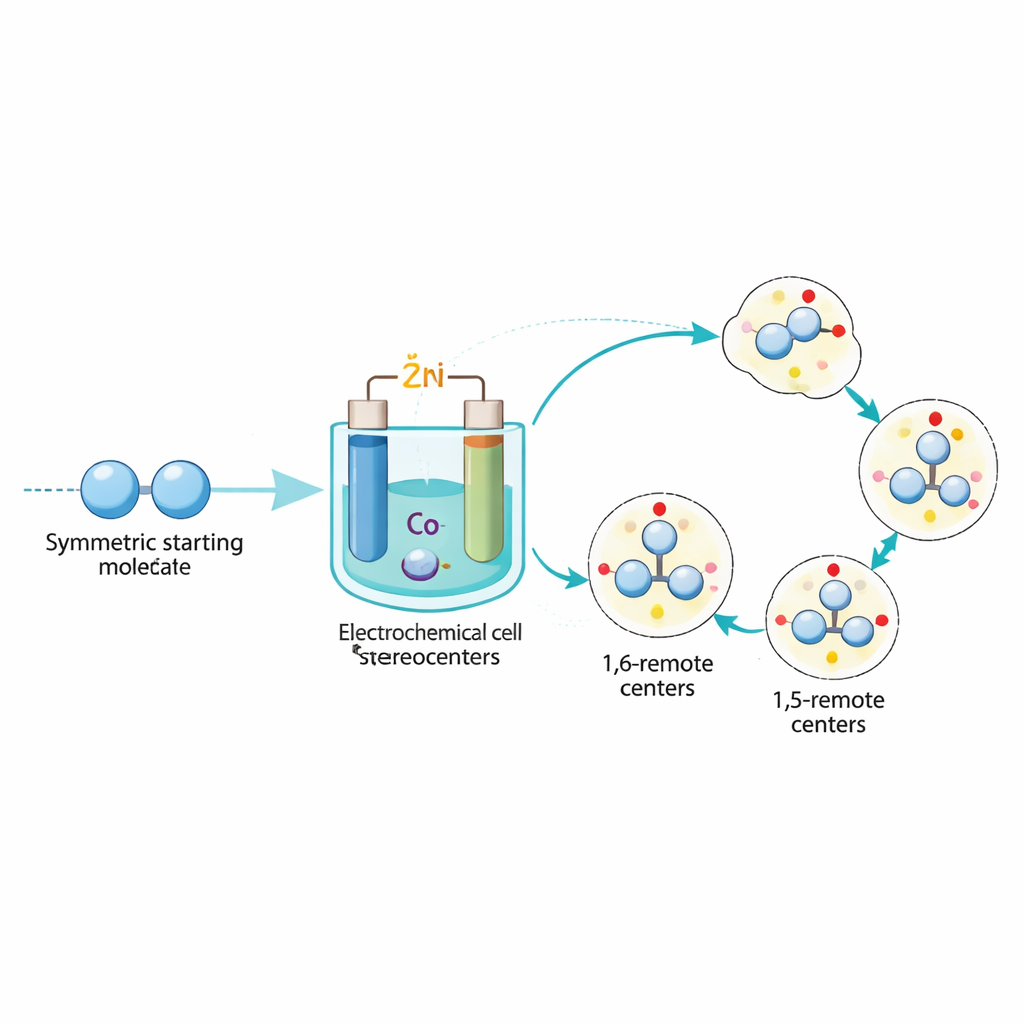
Von der Labormethode zu nützlichen molekularen Bausteinen
Anschaulich zeigt diese Arbeit, wie Elektrizität und ein einzelner Cobalt‑Katalysator sehr spezifische 3‑D‑Formen in ansonsten einfache und symmetrische Ausgangsmoleküle einprägen können. Anstatt für jede Art von chiralem Gerüst ein eigenes katalytisches System zu entwerfen, kann dieselbe elektrochemische Plattform mehrere Klassen chiraler Produkte mit zwei entfernten Steuerpunkten liefern. Da solche Strukturen in Top‑verkäufern und fortschrittlichen Katalysatoren häufig vorkommen, bietet diese Strategie Chemikern einen leistungsfähigen und flexiblen Weg, komplexe, formabhängige Moleküle direkter und effizienter zu bauen.
Zitation: Li, Y., Liu, S., Yuan, B. et al. Construction of remote dual stereocenters by electrochemical cobalt-catalyzed enantioselective desymmetrization. Nat Commun 17, 743 (2026). https://doi.org/10.1038/s41467-026-68437-w
Schlüsselwörter: asymmetrische Katalyse, Elektrochemie, Cobalt-Katalyse, chirale Moleküle, entfernte Stereozentren