Clear Sky Science · de
Verbesserter in vivo-Genskift mit hoher Spezifität durch multiplexe Cas12a-sgRNAs
Gene zuverlässiger bearbeiten
Genediting verspricht neue Wege, Biologie zu erforschen, Krankheiten zu behandeln und sogar Schädlinge zu kontrollieren, funktioniert in lebenden Tieren aber oft weniger sauber, als Schlagzeilen nahelegen. Viele Zellen entgehen der Bearbeitung oder werden nur teilweise verändert, was experimentelle Ergebnisse verwischen und die praktische Anwendung einschränken kann. Diese Arbeit beschreibt eine neue CRISPR-basierte Methode in Fruchtfliegen, die Genknockouts vollständiger und präziser macht und einen Leitfaden für verlässlichere Genomeditierung in komplexen Organismen liefert.
Warum Standard-CRISPR oft nicht ausreicht
Traditionelle CRISPR-Werkzeuge wie Cas9 schneiden DNA an einer gewählten Stelle mithilfe einer oder weniger Leit-RNAs. In lebenden Tieren stößt dieser Ansatz auf mehrere Hindernisse. Manche Guides funktionieren schlicht schlecht; manche Zielstellen sind für das Enzym schwer erreichbar; und die Reparaturmaschinerie der Zelle „repariert“ den Bruch häufig mit winzigen Veränderungen, die das Gen weiterhin funktionsfähig lassen. Das Ergebnis ist ein Mosaik: benachbarte Zellen desselben Gewebes können unterschiedliche Mutationen oder gar keine tragen. Diese Fleckenbildung erschwert es, nachzuvollziehen, was passiert, wenn ein Gen wirklich ausgeschaltet ist, und stellt eine Herausforderung für Anwendungen wie Gentherapie oder Gene Drives dar, die in den meisten Zellen wirksam sein müssen.
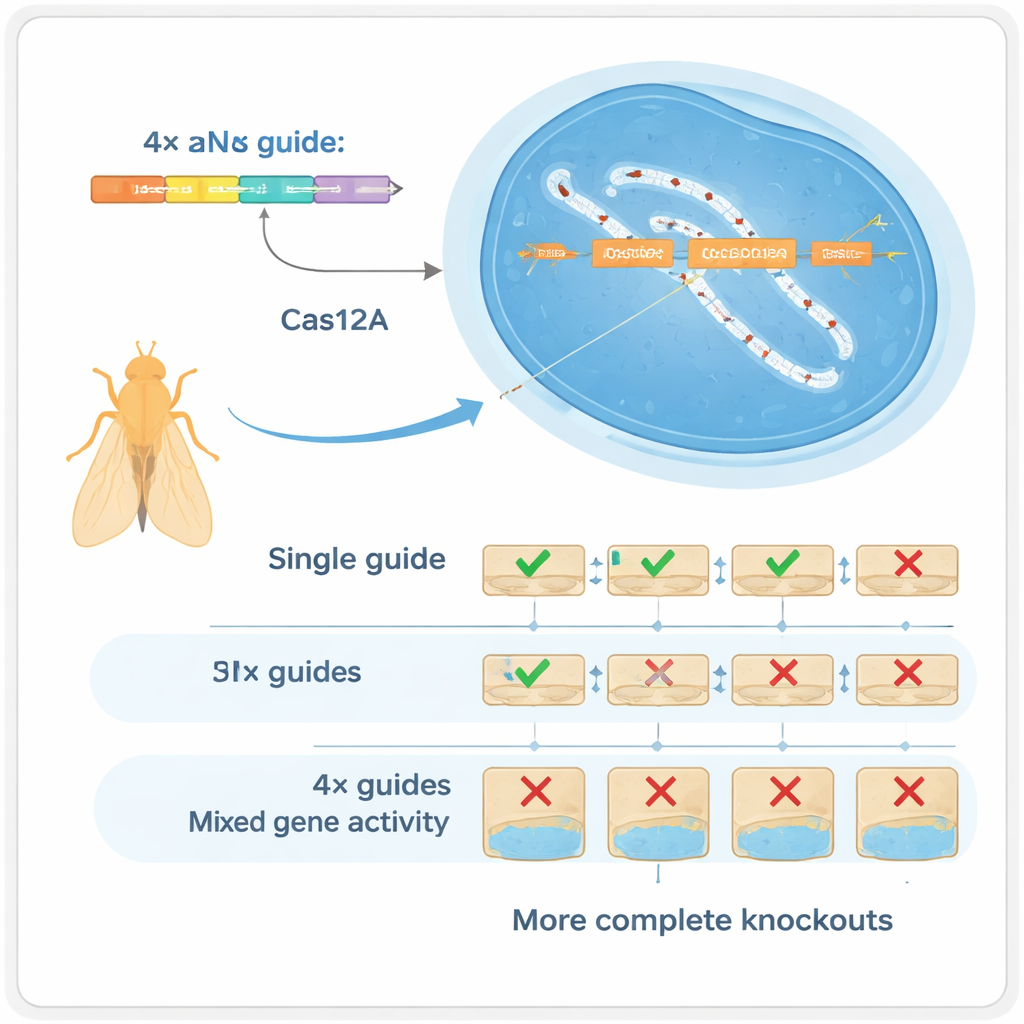
Vier Guides sind besser als einer
Die Autoren setzten ein anderes CRISPR-Enzym ein, Cas12a, das kompakte Arrays von Guides deutlich leichter verarbeiten kann als Cas9. Sie bauten ein Drosophila-Toolkit, in dem jedes Gen durch ein Array aus vier Leit-RNAs adressiert wird, die alle auf einem einzigen kleinen DNA-Fragment kodiert sind und massenproduziert werden können. In sorgfältig kontrollierten Tests zeigten sie, dass die Verwendung von vier Guides pro Gen die Art der erzeugten DNA-Veränderungen dramatisch verändert: Anstatt überwiegend winziger Einfügungen oder Deletionen an einer einzelnen Stelle erzeugt das System häufig größere Deletionen zwischen Schnittstellen, die fast immer die Genfunktion zerstören. Dieses „Multiplexing“ wirkt auf zwei Arten: Fällt ein Guide aus, können andere die Aufgabe übernehmen (Redundanz), und schneiden mehrere gleichzeitig, können sie größere Genabschnitte entfernen (Synergie).
Hohe Effizienz ohne zusätzliche Kollateralschäden
Mehr DNA-Brüche zu erzeugen wirft offensichtliche Sicherheitsfragen auf. Könnten mehrere Schnitte in einem Bereich versehentlich benachbarte Gene löschen? Könnten Guides anderswo im Genom häufiger fehlzielen? Um das zu prüfen, maßen die Forscher den Zelltod, untersuchten Auswirkungen auf benachbarte Gene und entwickelten einen raffinierten Test, um Chromosomenreparaturereignisse als Verlust der Heterozygosität über große DNA-Abschnitte sichtbar zu machen. Sie fanden heraus, dass das Bündeln von vier Schnitten innerhalb eines einzelnen Gens gut vertragen wurde: Es erhöhte den Zelltod nicht im Vergleich zu herkömmlichen Cas9-Ansätzen und störte nur selten benachbarte Gene, es sei denn, ein Guide landete extrem nah an einem regulatorischen Element. Groß angelegte Screens mit mehr als 2.000 Guides über ein Drittel des Fliegen-Genoms zeigten, dass über 99 % der Guide-Arrays an ihrem beabsichtigten Ziel aktiv waren, während reproduzierbare Off-Target-Aktivität unter 1 % lag — ein Hinweis auf sehr hohe Spezifität selbst in einem multiplexen Setup.
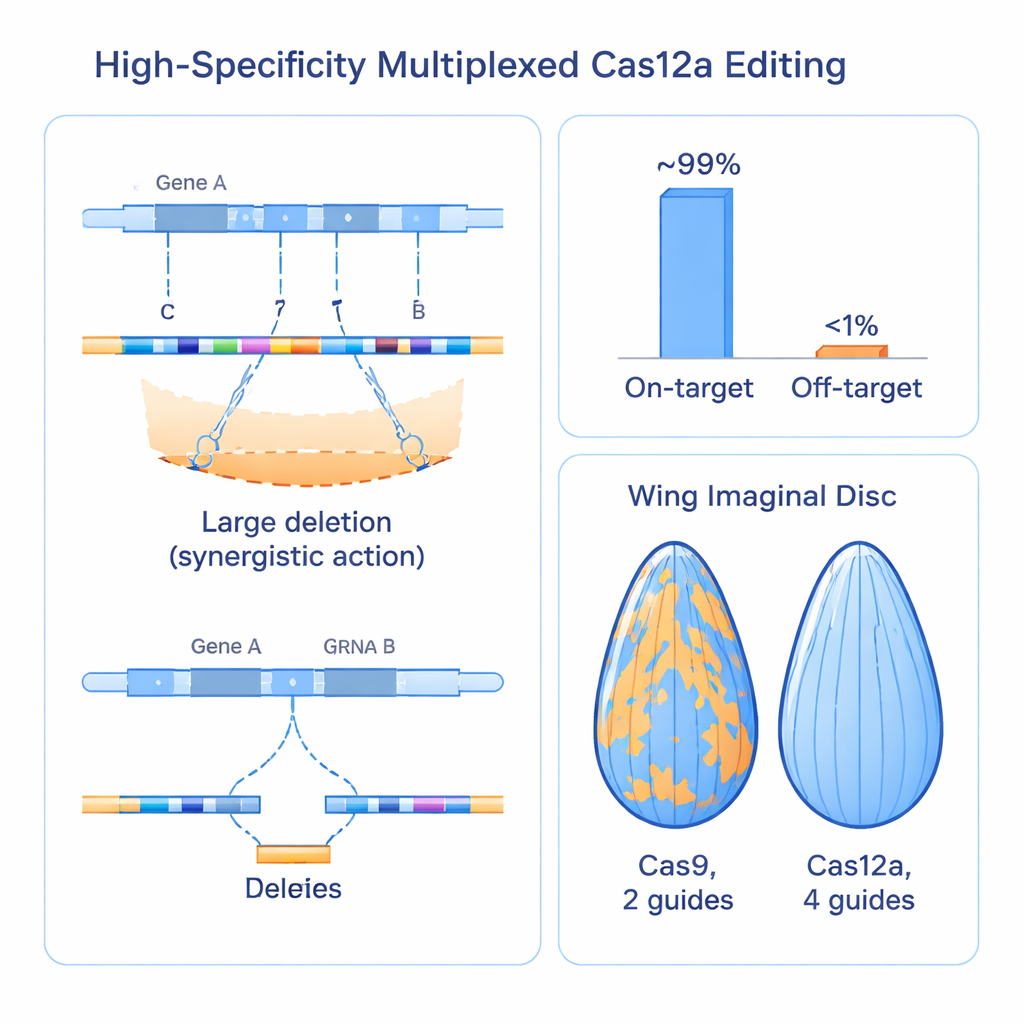
Übertrifft etablierte Cas9-Systeme in echten Geweben
Um zu prüfen, ob sich diese molekularen Verbesserungen in klarere biologische Ergebnisse übersetzen, verglich das Team ihr Cas12a–Vier-Guide-System direkt mit weit verbreiteten Cas9-basierten Ressourcen, die mehr als 100 Gene in der Fliege anvisierten. In Geweben wie dem Auge, dem Darm und dem sich entwickelnden Flügel erzeugte der Cas12a-Ansatz stärkere und gleichmäßigere Loss-of-Function-Effekte als Cas9, das oft offensichtliche Flecken uneditierter, normaler Gewebebereiche hinterließ. Als sie die Flügelgröße als quantitativen Messwert nutzten, erzeugte das neue System konsistent größere und reproduzierbarere Wachstumsdefekte für bekannte Regulatoren und zeigte, dass einige Gene, die zuvor als schwach oder nicht essentiell eingestuft wurden, tatsächlich übersehen worden waren, weil ältere Werkzeuge sie nicht gründlich genug inaktivierten. Die erhöhte Leistungsfähigkeit der Methode deckte sogar eine zuvor unbekannte, essentielle Rolle eines Gens namens trade embargo in der Flügelentwicklung und dem Überleben auf.
Was das für die Zukunft der Geneditierung bedeutet
Einfach gesagt zeigt diese Arbeit, wie man CRISPR von einem manchmal unordentlichen Skalpell in einen entschiedeneren Schalter verwandelt, um Gene in lebenden Tieren auszuschalten. Durch die Kombination von Cas12a mit vier Guides pro Gen erreichen die Autoren nahezu vollständige Knockouts bei sehr wenigen unbeabsichtigten Effekten, und das alles in einem Format, das praktikabel über Hunderte von Genen skaliert werden kann. Obwohl in Fruchtfliegen entwickelt, sind die zugrunde liegenden Prinzipien — die Nutzung mehrerer Guides für Redundanz und Synergie sowie das sorgfältige Prüfen chromosomaler Nebeneffekte — breit anwendbar. Diese Strategie könnte die Grundlagenforschung verbessern, genetische Screens schärfen und sicherere Entwürfe für zukünftige medizinische und ökologische Anwendungen der Geneditierung informieren.
Zitation: Port, F., Buhmann, M.A., Zhou, J. et al. Improved in vivo gene knockout with high specificity using multiplexed Cas12a sgRNAs. Nat Commun 17, 877 (2026). https://doi.org/10.1038/s41467-026-68434-z
Schlüsselwörter: CRISPR, Cas12a, Gendeletion, Drosophila, Spezifität der Genomeditierung