Clear Sky Science · de
Kontrolle der Rekrutierung von Telomerase und des Ends‑schutzes durch unabhängige Shelterin‑Komponenten
Wie Zellen ihre Chromosomenenden schützen
Jedes Mal, wenn sich eine Zelle teilt, werden die äußersten Enden ihrer Chromosomen — die Telomere — ein wenig verkürzt. Um den Verlust wichtiger genetischer Information zu vermeiden, nutzen Zellen ein spezielles Enzym, die Telomerase, sowie eine Gruppe schützender Proteine zur Erhaltung dieser Enden. Diese Studie untersucht, wie zwei dieser Proteine, TPP1 und POT1, das empfindliche Gleichgewicht zwischen dem Zulassen von Telomerase zum Wiederaufbau der Telomere und dem sicheren Verschließen der Chromosomenenden gegen Schäden steuern.
Das Problem alternder Chromosomenenden
Telomere wirken wie Kunststoffkappen an Schnürsenkeln und verhindern, dass Chromosomen ausfransen oder fälschlich als beschädigte DNA erkannt werden. Wenn die Zelle ein Chromosomenende als Schaden fehlinterpretiert, kann das Notfallreparatursystem aktiviert werden, das Chromosomen verklebt oder die Zellteilung stoppt. Gleichzeitig müssen Telomere gelegentlich geöffnet werden, damit Telomerase sie verlängern kann, besonders in Stammzellen, die sich häufig teilen. Biologen stellten sich lange vor, dass Telomere zwischen einem „geschlossenen“ geschützten Zustand und einem „offenen“ Zustand umschalten, der Telomerase Zugang gewährt, aber vorübergehend Schadenssignale zulassen kann. Ob diese beiden Zustände unterschiedliche physische Formen des Telomers widerspiegeln oder tatsächlich getrennte Kontrollmechanismen darstellen, blieb bislang ungeklärt.
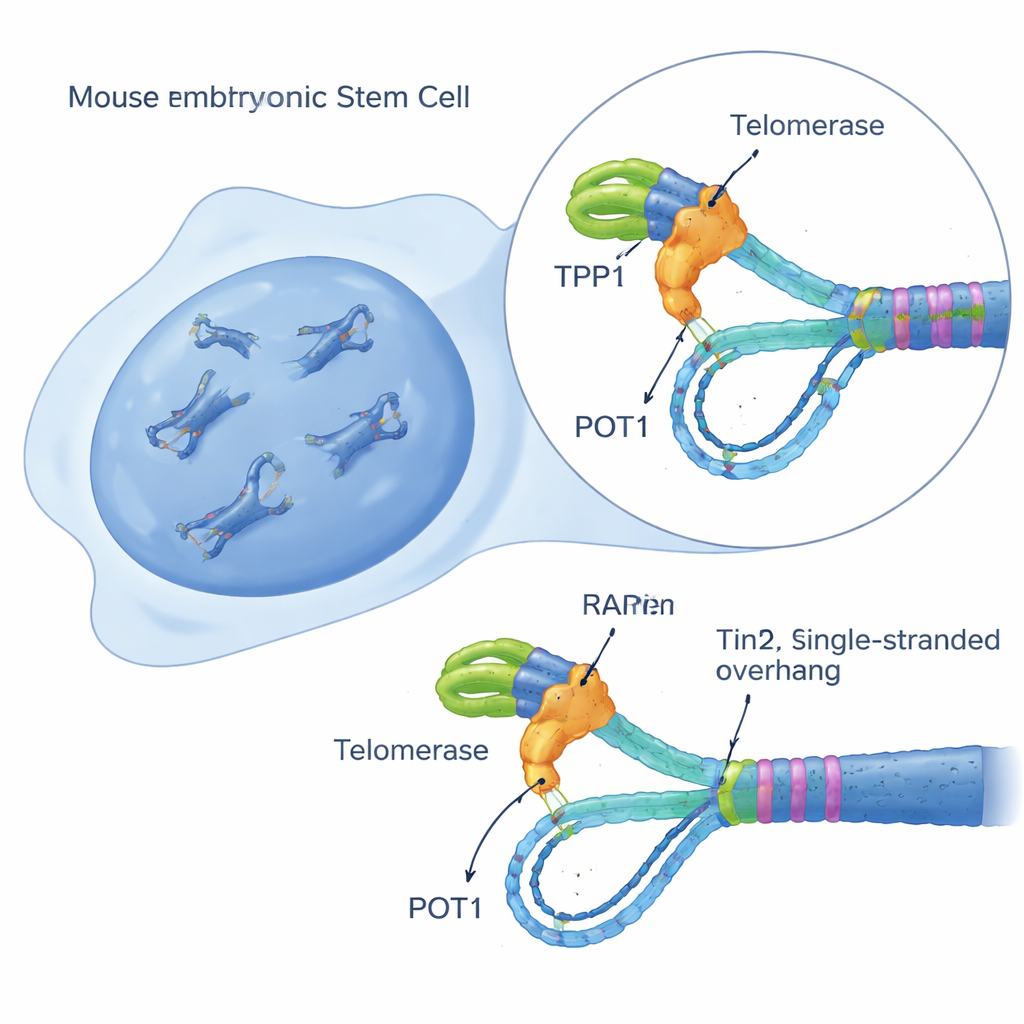
Aufbau eines Einzelzell‑Sensors für Telomeraseaktivität
Um dieses Rätsel zu lösen, entwickelten die Forschenden einen empfindlichen Live‑Zell‑Test namens iTAP (inducible Telomerase Activity Probing) in Maus‑embryonalen Stammzellen. Sie konstruierten Zellen so, dass diese nur nach Zugabe des Wirkstoffs Doxycyclin eine leicht veränderte Version der Telomerase‑RNA‑Vorlage herstellen. Diese „mutierte“ Vorlage bewirkt, dass Telomerase eine modifizierte DNA‑Sequenz an Telomeren anfügt, die sich visuell von normaler Telomer‑DNA unterscheiden lässt. Mit fluoreszierenden Sonden, DNA‑Blots und einer Methode zur Anreicherung von Telomerfragmenten durch Sequenzierung konnte das Team direkt, Zelle für Zelle, sehen, wann und wo Telomerase aktiv war. Wichtig war, dass dieses System das Zellwachstum nicht beeinträchtigte und selbst keine Schadensantwort auslöste, sodass saubere Messungen des Telomeraseverhaltens in ansonsten gesunden Zellen möglich waren.
TPP1 holt Telomerase heran, POT1 bremst sie
Mit iTAP prüften die Autorinnen und Autoren, wie zwei Schlüsselfaktoren am Telomer, TPP1 und POT1, zur Telomerase‑Aktivität beitragen. Beide gehören zu dem größeren Komplex Shelterin, der Telomere bedeckt. Entfernten sie TPP1 mittels Geneditierung, gingen die mutierten Telomersequenzen nahezu verloren, obwohl die mutierte Telomerase‑RNA weiterhin in normaler Menge produziert wurde. Weitere Experimente zeigten, dass TPP1 physisch mit einer anderen Shelterin‑Komponente, TIN2, verbunden sein muss, um Telomerase anzuwerben; die Störung der Verbindung zwischen TPP1 und TIN2 schaltete die Telomeraseaktivität aus. Überraschenderweise hatte das Aufbrechen der Wechselwirkung zwischen TPP1 und POT1 keinen solchen Effekt, und das Entfernen von POT1 selbst verringerte die Telomerasewirkung nicht. Tatsächlich zeigten Zellen ohne POT1 einen moderaten Anstieg der eingebrachten mutierten Sequenz, was nahelegt, dass POT1 üblicherweise als Bremse wirkt — es begrenzt, wie häufig Telomerase an Telomere bindet, anstatt sie zu fördern.
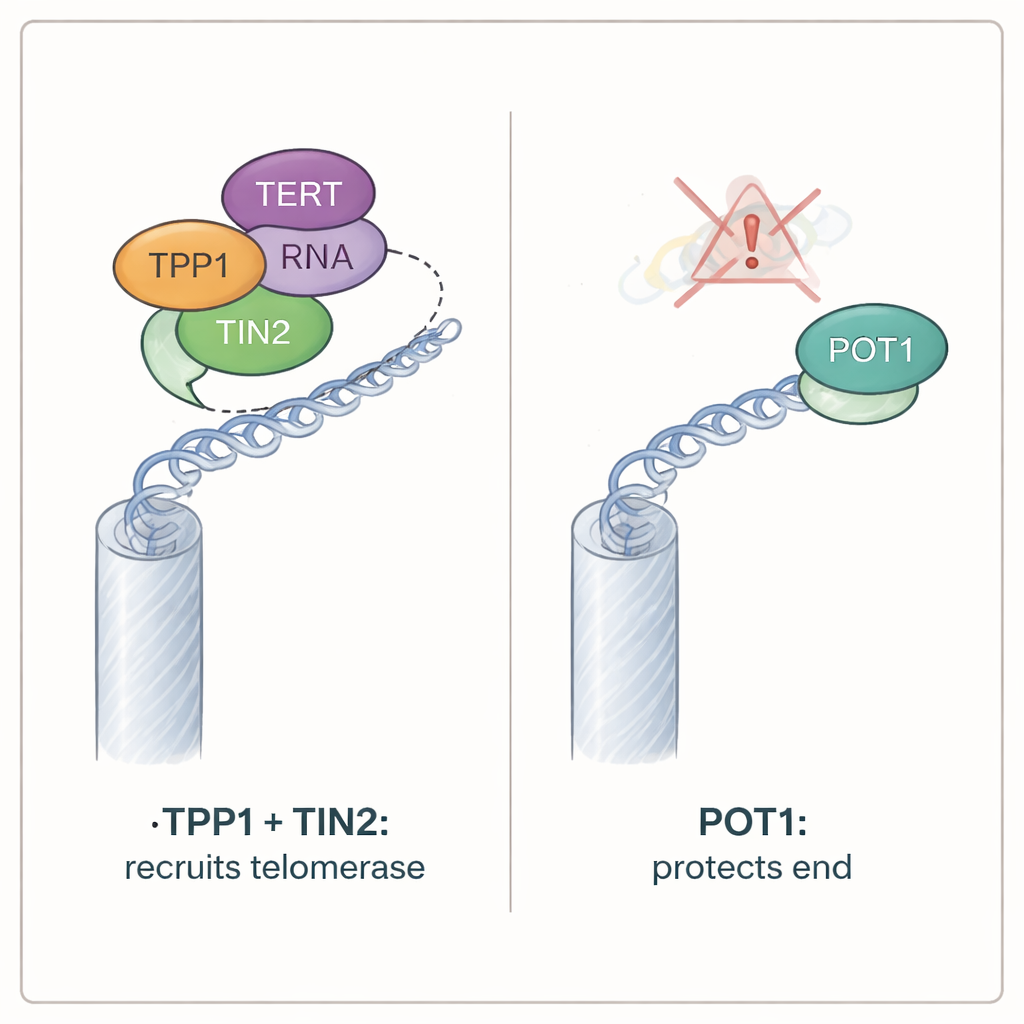
POT1 bewacht die Enden, während TPP1 entbehrlich sein kann
Obwohl POT1 für die Rekrutierung der Telomerase nicht erforderlich war, erwies es sich als essenziell für den Schutz der Chromosomenenden. Zellen, denen beide Varianten von POT1 in Mäusen fehlten, stellten rasch die Proliferation ein und zeigten alle Kennzeichen freiliegender Telomere: DNA‑Schadensmarker häuften sich an den Chromosomenenden, die damage‑sensitiven Kinase ATR wurde aktiviert und Chromosomenenden fusionierten. Im Gegensatz dazu teilten sich Zellen ohne TPP1 weiter und zeigten kaum Anzeichen von Telomerstress, obwohl sie die normale Telomeraseaktivität verloren hatten. Zusätzliche Tests zeigten, dass POT1s defensive Rolle von seiner Fähigkeit abhängt, an die einzelsträngige Überhängen der Telomere zu binden. Mutante POT1‑Proteine, die diese exponierte DNA nicht mehr greifen konnten, unterdrückten die Schadenssignale nicht, selbst wenn sie weiterhin mit TPP1 interagieren konnten. Umgekehrt schützten POT1‑Varianten, die den Überhang binden konnten, aber nicht mehr an TPP1 anhefteten, weiterhin die Chromosomenenden.
Eine neue, modulare Sicht auf die Telomer‑Kontrolle
Diese Ergebnisse widerlegen das einfache Bild, wonach Telomere zwischen einem einzigen „offenen“ Zustand für Telomerase und einem einzigen „geschlossenen“ Zustand für Schutz umschalten. Stattdessen zeigt die Studie, dass Rekrutierung der Telomerase und Ends‑schutz durch trennbare molekulare Schaltkreise gesteuert werden. TPP1 wirkt über TIN2 als Haupttor, das Telomerase an Telomere bringt, während POT1 unabhängig das einzelsträngige DNA‑Überhang am Chromosomenende bewacht und Schadensantworten in Schach hält. Für Laien zusammengefasst heißt das: Zellen verlassen sich nicht auf einen universellen Schalter an den Chromosomenenden. Vielmehr nutzen sie getrennte, aber koordinierte Regler — einen, um Telomerase hereinzulassen, und einen anderen, um die Enden sicher zu halten — um die Genomstabilität ein Leben lang zu erhalten.
Zitation: Sandhu, R., Tricola, G.M., Lee, S.Y. et al. Control of telomerase recruitment and end protection by independent shelterin components. Nat Commun 17, 1733 (2026). https://doi.org/10.1038/s41467-026-68433-0
Schlüsselwörter: Telomere, Telomerase, Stammzellen, DNA‑Schäden, Chromosomenschutz