Clear Sky Science · de
Dynamische Allelnutzung X‑gebundener Gene mildert phänotypische Merkmale neuroentwicklungsbedingter Erkrankungen in Gehirn‑Organoiden
Wie das „stille“ X‑Chromosom das Gehirn schützt
Jede Zelle einer Frau trägt zwei X‑Chromosomen, doch in Lehrbüchern hieß es jahrzehntelang, eines davon sei weitgehend abgeschaltet—wie ein Ersatzbuch, das geschlossen im Regal liegt. Diese Studie zeigt, dass dieses „stille“ X, besonders im sich entwickelnden Gehirn, eher einer dynamischen Backup‑Bibliothek gleicht. Es kann bei Bedarf angezapft werden, und diese zusätzliche Flexibilität könnte erklären, warum viele Störungen der Gehirnentwicklung Männer stärker treffen als Frauen.
Ein verborgenes Backup‑System auf dem X‑Chromosom
Bei weiblichen Säugetieren wird in jeder Zelle früh in der Entwicklung ein X‑Chromosom abgeschaltet, um eine doppelte Dosis X‑gebundener Gene zu vermeiden. Allerdings ist seit langem bekannt, dass einige Gene dieser Abschaltung entkommen können. Die neue Arbeit geht einer tieferen Frage nach: Ist dieses Entkommen festgelegt, oder kann es sich mit der Entwicklung der Zellen verändern? Mithilfe menschlicher Stammzellen und Mini‑Gehirn‑Gewebe, so genannter Organoide, verfolgten die Forschenden, welche Kopie jedes X‑gebundenen Gens—mütterlich oder väterlich—genutzt wurde, während sich Zellen von Stammzellen zu Nervenzellen entwickelten. Sie fanden heraus, dass viele Gene auf dem vermeintlich inaktiven X phasen‑ und zelltypspezifisch ein‑ und ausgeschaltet werden, anstatt einer einfachen Ein/Aus‑Regel zu folgen.
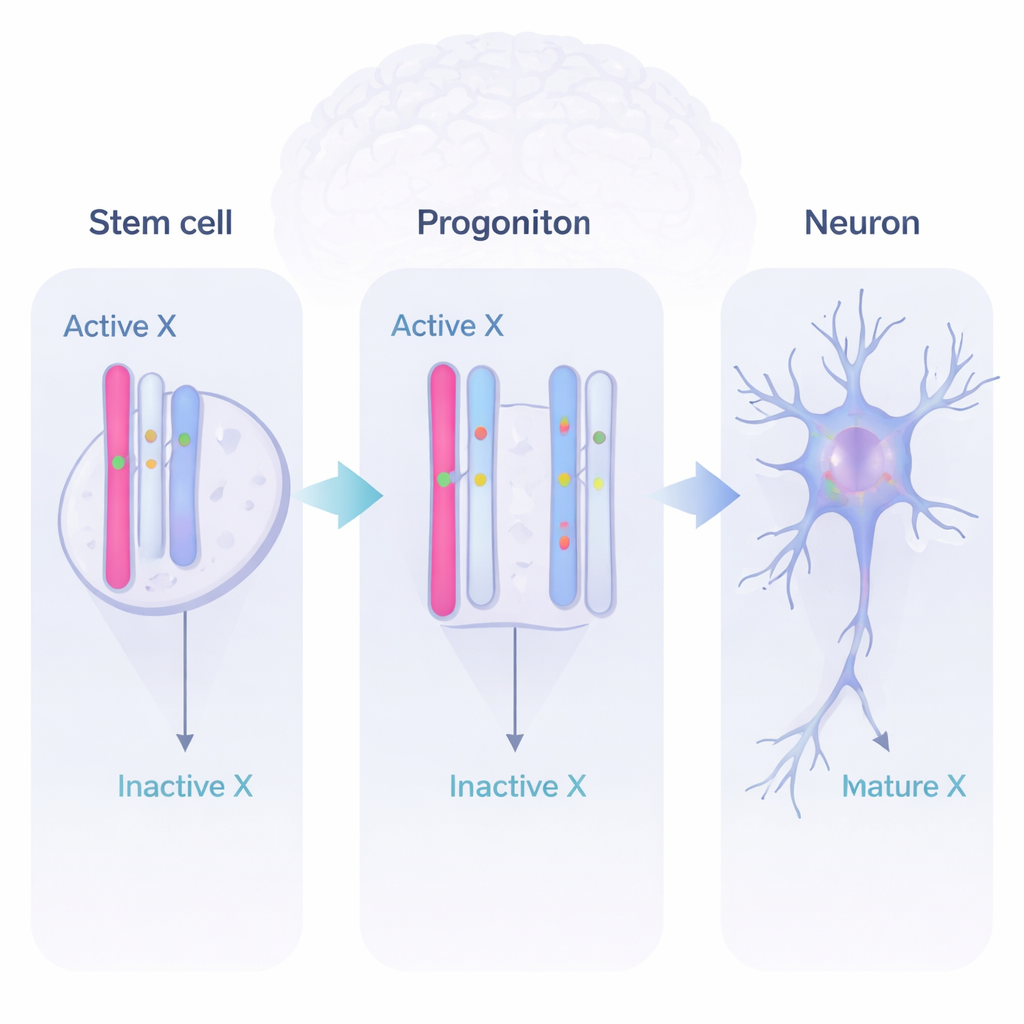
Dynamische Genutzung während der Gehirnentwicklung
Durch das Lesen von RNA (den von Genen erzeugten Botschaften) und die Unterscheidung zwischen den beiden elterlichen Kopien entdeckte das Team drei Hauptverhaltensweisen. Einige Gene blieben auf dem inaktiven X größtenteils ausgeschaltet, wie erwartet. Andere waren „vollständige Entkletterer“ und von beiden X‑Kopien in allen Stadien aktiv. Am interessantesten war eine beträchtliche Gruppe dynamischer Gene. Diese Gene waren in Stammzellen auf dem inaktiven X still, wurden in neuralen Vorläuferzellen und frühen Neuronen von beiden X‑Chromosomen aktiviert und schalteten sich später bei einigen wieder ab. Das zeigt, dass das inaktive X kein statischer Friedhof für Gene ist, sondern ein flexibler Vorrat, auf den das sich entwickelnde Gehirn zurückgreifen kann, wenn zusätzliche Genaktivität nützlich ist.
Konservierte Muster und Verbindungen zu Hirnerkrankungen
Verglichen mit Mausstudien und chemischen Markierungen auf der DNA aus fetalem Hirngewebe fanden die Forschenden, dass dieses dynamische Entkommen der X‑Inaktivierung auch bei anderen Säugetieren vorkommt und mit Chromatin‑Zuständen verknüpft ist—Eigenschaften der DNA‑Verpackung, die steuern, wie leicht Gene eingeschaltet werden können. Die reaktivierenden Gene neigten dazu, in bestimmten Regionen des X‑Chromosoms zu clustern und trugen epigenetische Signaturen aktiver DNA, speziell im weiblichen Gehirngewebe. Wichtigerweise waren diese dynamisch reaktivierten Gene ungewöhnlich reich an bekannten Risikogenen für neuroentwicklungsstörungen wie geistige Behinderung und Autismus‑Spektrum‑Störungen, was nahelegt, dass diese Flexibilität sich als Schutzmechanismus entwickelt hat.
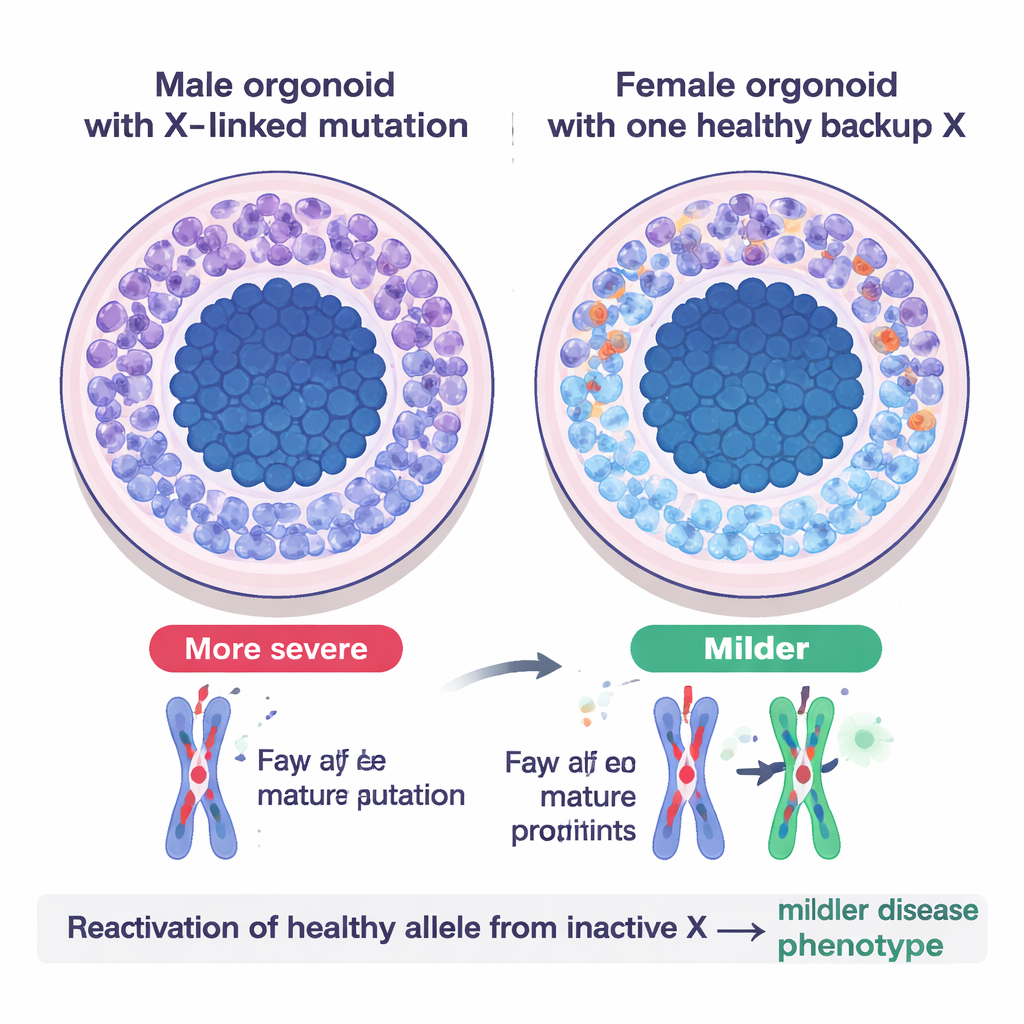
Ein realistischer Test: Opitz BBB/G‑Syndrom
Um zu untersuchen, wie dieses Backup‑System in der Krankheit wirkt, modellierte das Team das Opitz BBB/G‑Syndrom, eine seltene X‑gebundene Erkrankung, die die Mittellinienstruktur des Gehirns betrifft und häufig Entwicklungsverzögerungen verursacht. Die Störung wird durch schädigende Mutationen in einem Gen namens MID1 auf dem X‑Chromosom ausgelöst. In aus männlichen Patientenzellen gezüchteten Gehirn‑Organoiden—wo nur eine X‑Kopie vorliegt—waren Neuronen rar und neuralen Stammzellen verharrten zu lange im teilenden Zustand, was dem bei Patienten beobachteten Minderwachstum des Gehirns entspricht. Weibliche Organoide mit derselben Mutation auf ihrem aktiven X, aber einer gesunden Kopie auf dem inaktiven X, wirkten merklich gesünder: Sie produzierten mehr Neuronen und zeigten mildere Defekte. Als Wissenschaftler weibliche Linien so konstruierten, dass beide X‑Kopien die Mutation trugen, entwickelten die Organoide schwere, männliche Probleme—ein Beleg dafür, dass das zuvor inaktive gesunde Allel reaktiviert worden war und zur Kompensation beitrug.
Was das für geschlechtsspezifische Unterschiede bei Hirnerkrankungen bedeutet
Die Studie zeigt, dass das zweite, „stille“ X‑Chromosom bei Frauen nicht nur genetisches Ballast ist. Während wichtiger Zeitfenster der Gehirnentwicklung schalten ausgewählte Gene auf diesem inaktiven X in spezifischen Zelltypen an und vergrößern so den Pool funktionierender Genkopien. Für Gene wie MID1, die für den Aufbau des Gehirns entscheidend sind, kann diese dynamische Reaktivierung die Auswirkungen schädlicher Mutationen abschwächen und zu milderen, variableren Symptomen bei Frauen führen. Anders ausgedrückt: Das weibliche Gehirn verfügt über ein internes Backup‑System, das im Laufe der Zeit hoch‑ oder heruntergeregelt werden kann und so hilft zu erklären, warum viele X‑gebundene neuroentwicklungsbedingte Erkrankungen bei Mädchen seltener oder weniger schwer verlaufen als bei Jungen.
Zitation: Bertin, M., Todorov, H., Frank, S. et al. Dynamic allele usage of X-linked genes ameliorates neurodevelopmental disease phenotypes in brain organoids. Nat Commun 17, 599 (2026). https://doi.org/10.1038/s41467-026-68428-x
Schlüsselwörter: Inaktivierung des X‑Chromosoms, Gehirn‑Organoide, neuroentwicklungsstörungen, Gen‑Dosierung, geschlechtsspezifische Unterschiede bei Krankheiten