Clear Sky Science · de
Shigella flexneri entgeht septinvermittelter zellautonomer Immunität durch Protein-ADP‑Riboxanierung
Wie manche Darmbakterien an unserer inneren Sicherheitsabwehr vorbeischlüpfen
Schwere Durchfallerkrankungen durch Shigella-Bakterien sind weltweit nach wie vor ein großes Problem, vor allem bei Kleinkindern. Unsere Zellen sind nicht wehrlos: sie verfügen über eingebaute Mechanismen, die eindringende Mikroben fangen und zerstören können. Diese Studie zeigt, wie Shigella flexneri, eine führende Ursache von Ruhr, raffinierte molekulare Tricks einsetzt, um eines dieser Abwehrsysteme zu demontieren und so das Ausbreiten von Zelle zu Zelle im Darm zu ermöglichen.
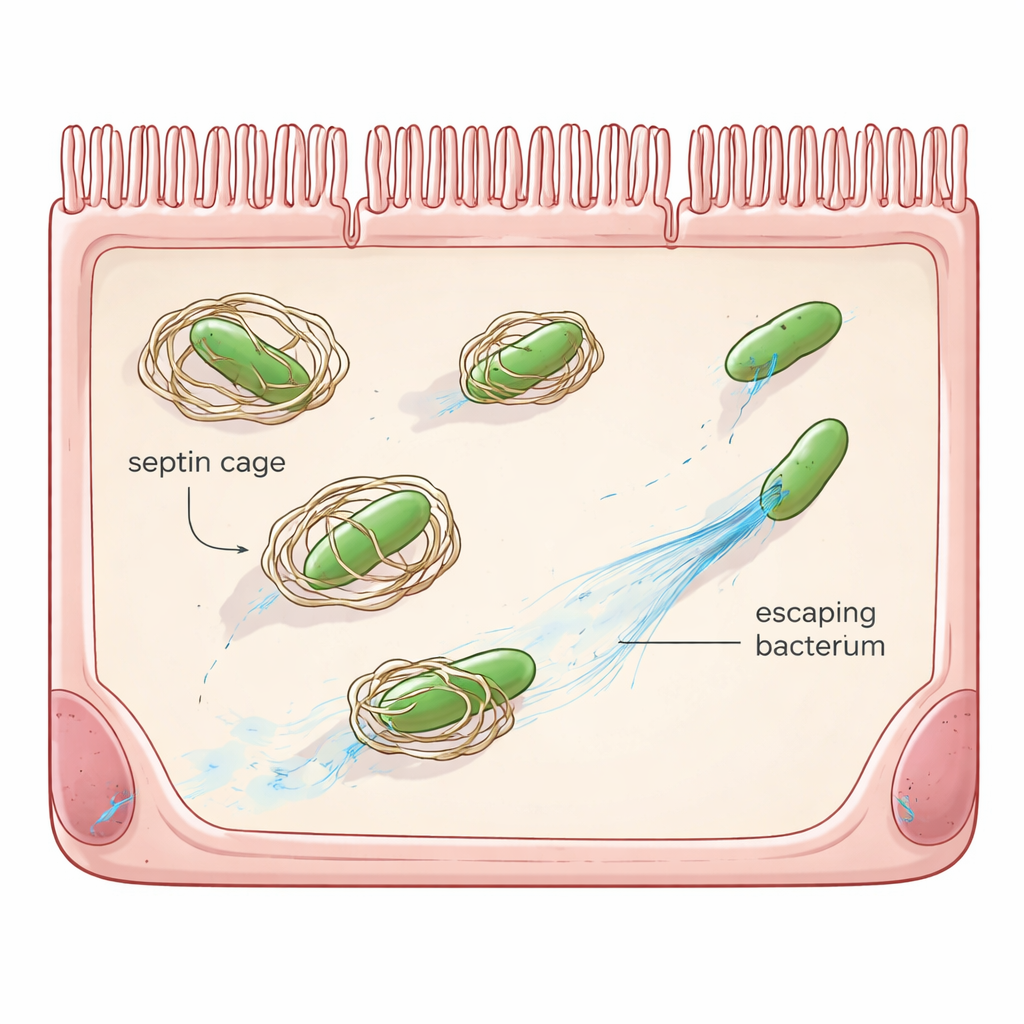
Die „Do-it-yourself“-Verteidigung der Zelle
Abgesehen von weißen Blutkörperchen und Antikörpern verfügen viele gewöhnliche Zellen über eigene Notfall-Sicherheitssysteme, die man als zellautonome Immunität bezeichnet. Ein solches System beruht auf Septinen, einer Familie von Gerüstproteinen, die Ringe und käfigartige Strukturen bilden. Wenn Shigella in eine Zelle eindringt und in das gelartige Zellinnere entkommt, können sich Septine um das Bakterium herum anordnen, seine Bewegungsfähigkeit blockieren und es für den Abbau durch zelluläre Recycling‑Wege markieren. Frühere Arbeiten zeigten, dass Shigella bereits eine Gegenmaßnahme besitzt, ein Protein namens OspG, das Septine für den Abbau markiert. Doch selbst wenn OspG fehlt, entgehen die meisten Bakterien weiterhin dem Gitter, was nahelegt, dass Shigella zusätzliche Tricks hat.
Aufspüren eines zweiten bakteriellen Saboteurs
Die Autorinnen und Autoren richteten ihre Aufmerksamkeit auf eine weitere Gruppe von Shigella‑Proteinen, die als OspC‑Familie bekannt sind. Mit einem globalen Protein‑Kartierungsansatz in menschlichen Zellen suchten sie nach Wirtsproteinen, die chemisch verändert wurden, wenn OspC‑Proteine vorhanden waren. Neben bekannten Zielmolekülen der Proteinsynthese fanden sie, dass mehrere Septine, besonders eines namens SEPT9, konsistent markiert wurden. Detaillierte biochemische Tests zeigten, dass drei OspC‑Proteine direkt einen kleinen, energiehaltigen Anhängsel aus dem Molekül NAD an vielen Stellen in Septinen anbringen können. Diese chemische Modifikation, ADP‑Riboxanation genannt, ist eine spezielle, irreversible Variante einer verbreiteten Proteinveränderung.
Das Gerüst von innen heraus sprengen
Um zu verstehen, wie dieser chemische Anhängsel die zelluläre Abwehr schwächt, fokussierte das Team auf SEPT9. Septine bilden typischerweise geordnete Ketten aus acht Einheiten, die sich zu Filamenten und schließlich zu vollständigen Käfigen um Bakterien anordnen. Die Forschenden entdeckten, dass eine bestimmte Position in SEPT9, die Aminosäure Arginin 561, die Hauptstelle für ADP‑Riboxanation während einer Infektion ist. Strukturelle Untersuchungen und Rekonstitutionsversuche mit gereinigten Proteinen zeigten, dass sich diese Stelle an einer kritischen Kontaktfläche befindet, an der zwei SEPT9‑Einheiten miteinander verriegeln. Wenn dieses Arginin chemisch modifiziert wird — oder durch eine Aminosäure ersetzt wird, die die hinzugefügte negative Ladung imitiert —, lösen sich die oktamerischen Ketten in kleinere Teile auf und können keine stabilen Filamente mehr bilden.
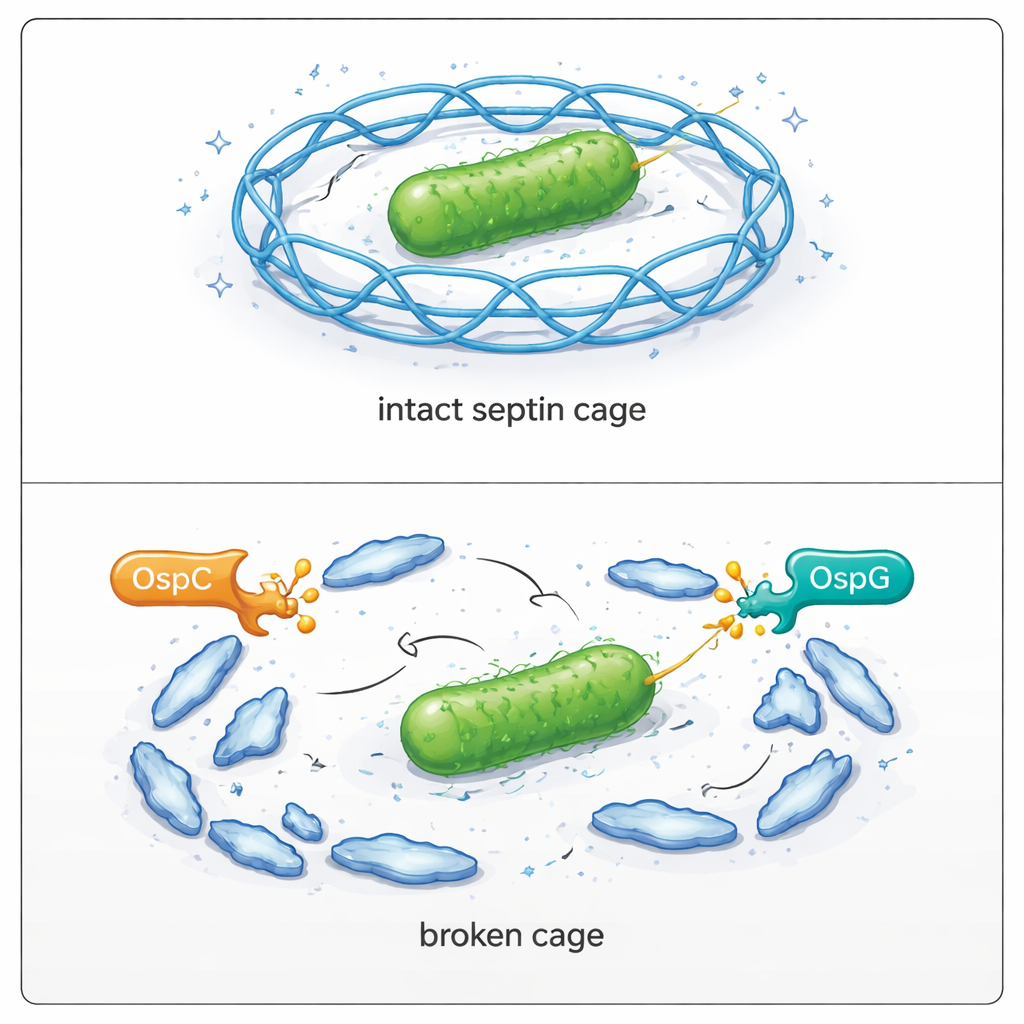
Beobachtung, wie Käfige in infizierten Zellen versagen
Anschließend untersuchten die Forschenden lebende Zellen, um die Folgen zu sehen. In menschlichen Zellen, die mit normaler Shigella infiziert waren, landete nur eine Minderheit der Bakterien in Septin‑Gittern. Als alle OspC‑Proteine genetisch entfernt wurden, verdoppelte sich nahezu der Anteil der eingesperrten Bakterien. Das Entfernen von OspG hatte einen ähnlichen Effekt; wurden sowohl OspC als auch OspG gemeinsam deletiert, erhöhte sich die Käfigbildung noch weiter und die Fähigkeit der Bakterien, sich über eine Zellschicht auszubreiten, war stark beeinträchtigt. Die Wiedereinführung aktiver OspC‑Proteine in die Mutantenstämme stellte deren Entkommen aus den Käfigen sowie ihre Replikations‑ und Plaquebildungsfähigkeit wieder her. Die Mikroskopie bestätigte, dass SEPT9, wenn es an Arginin 561 nicht modifiziert werden kann, effizient an Käfigen teilnimmt; wird es jedoch durch OspC verändert, sinkt die Käfigbildung um einen deutlichen Betrag.
Was das für die Bekämpfung von Shigella bedeutet
Vereinfacht gesagt zeigt diese Arbeit, dass Shigella ein passgenaues Paar molekularer Werkzeuge mitführt, das dazu dient, die Stäbe eines intrazellulären „Gefängnisses“ aufzubrechen. OspC schwächt direkt die Proteinbausteine, die zum Aufbau von Septin‑Gittern nötig sind, während OspG deren Entsorgung über einen anderen chemischen Weg fördert. Zusammen erlauben diese Strategien den Bakterien, sich zu befreien, sich innerhalb von Zellen zu bewegen und benachbarte Zellen zu befallen. Das Verständnis dieser genauen Fluchtmechanismen vertieft nicht nur unser Bild davon, wie zell‑intrinsische Immunität funktioniert, sondern weist auch auf neue therapeutische Ansatzpunkte hin: Wirkstoffe, die OspC blockieren oder kritische Septin‑Kontaktstellen schützen, könnten helfen, die natürliche Fähigkeit der Zelle wiederherzustellen, diesen gefährlichen Erreger einzufangen und zu beseitigen.
Zitation: Tang, Z., Xian, W., Özbaykal Güler, G. et al. Shigella flexneri evades septin-mediated cell-autonomous immunity via protein ADP-riboxanation. Nat Commun 17, 1727 (2026). https://doi.org/10.1038/s41467-026-68425-0
Schlüsselwörter: Shigella, Septin-Gitter, zellautonome Immunität, bakterielle Virulenzfaktoren, ADP‑Ribosylierung