Clear Sky Science · de
Peptid-Naturstoffe, die ClpC1 anvisieren, stören unterschiedlich das Proteom von Mycobacterium tuberculosis
Warum es wichtig ist, bakterielle Aufräumtruppen zu stören
Tuberkulose bleibt eine der tödlichsten Infektionskrankheiten weltweit, und medikamentenresistente Stämme von Mycobacterium tuberculosis erschweren die Behandlung. Die meisten vorhandenen Antibiotika greifen die Zellwand der Bakterien an oder stören ihre Fähigkeit, Energie zu erzeugen und genetisches Material zu kopieren. Diese Studie untersucht eine ganz andere Schwachstelle: das interne „Aufräumteam“ der Zelle, das die Proteingesundheit bewahrt. Indem man versteht, wie neue, auf natürlichen Produkten basierende Moleküle dieses Aufräumsystem stören, hoffen Wissenschaftler, künftige Wirkstoffe zu entwerfen, die TB‑Bakterien auf neue und nachhaltigere Weise abtöten können.
Das proteinpflegerische Zentrum der Zelle
Wie alle lebenden Zellen baut der TB‑Erreger kontinuierlich Proteine auf, faltet, repariert und recycelt sie. Ein zentraler Akteur in diesem Netzwerk ist eine große Maschine namens ClpC1–ClpP1P2‑Komplex. Ein Teil (ClpC1) fungiert als Chaperon, erkennt und zieht beschädigte oder überflüssige Proteine hinein, während der andere Teil (ClpP1P2) sie in Stücke zerschneidet, um sie zu recyceln. Dieses System ist für das Überleben des Bakteriums unerlässlich, insbesondere unter Stress wie Hitze oder Antibiotikabehandlung. Mehrere natürliche Peptidverbindungen — Ecumicin, Ilamycine (Rufomycine) und Cyclomarine — sind bereits dafür bekannt, an ClpC1 zu binden und starke TB‑tötende Aktivität zu zeigen, was darauf hindeutet, dass dieser Komplex ein vielversprechendes Wirkziel sein könnte. 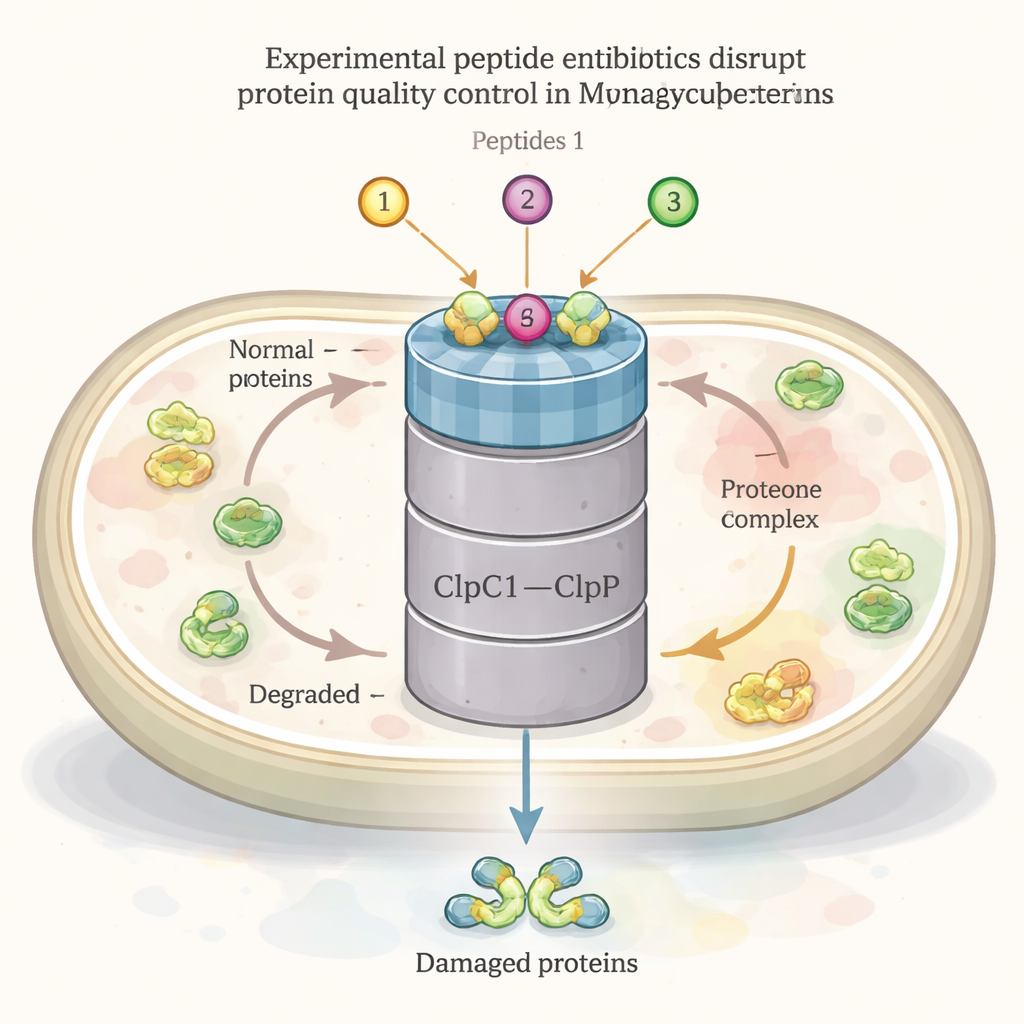
Drei verwandte Wirkstoffe, drei unterschiedliche Auswirkungen
Die Forscher untersuchten je einen Vertreter aus den drei Peptidfamilien: ein Ecumicin‑Analogon (Ecu*), Ilamycin E (IlaE) und ein Cyclomarin‑Derivat (Desoxycyclomarin, dCym). Obwohl alle drei an dieselbe Region von ClpC1 andocken, verhalten sie sich innerhalb der Zelle nicht gleich. Mit quantitativer Proteomik — einer Methode, die tausende Proteine gleichzeitig misst — stellten sie fest, dass Ecu* die breiteste Störung verursachte und die Mengen von fast 17 % aller bakteriellen Proteine signifikant veränderte. IlaE veränderte etwa 12 % und dCym etwa 7 %. Nur 72 Proteine wurden von allen drei Verbindungen konsistent beeinflusst, und die meisten davon nahmen ab. Das zeigt, dass jedes Molekül die ClpC1‑Maschine in eine andere Richtung drängt und die Proteinlandschaft der Zelle auf unterschiedliche Weise umgestaltet, anstatt die Maschine einfach „abzuschalten“.
Den Schredder verstopfen versus die Energie abschalten
Um diese Effekte einzuordnen, verglich das Team die Peptide mit Bortezomib, einem Krebsmedikament, das Proteine abbauende Enzyme allgemein blockiert. In TB‑Bakterien verursachte Bortezomib wie erwartet eine allgemeine Anhäufung vieler Proteine, wenn die Schredder ausgeschaltet sind. Im Gegensatz dazu erzeugten die Peptide selektivere Muster: Einige bekannte ClpC1‑Ziele häuften sich an, andere gingen zurück, und eine globale Hemmung des gesamten Proteinabbaus wurde nicht beobachtet. Detaillierte Labortests mit gereinigten Komponenten zeigten, dass jedes Peptid veränderte, wie bestimmte Substrate gehandhabt werden. Beispielsweise beeinträchtigten alle drei die Zerstörung eines regulatorischen Proteins (PanD), aber nur Ecu* blockierte den Abbau eines modellhaften ungeordneten Proteins, und nur dCym behinderte den Abbau des stressschützenden Proteins Hsp20. Diese Unterschiede deuten darauf hin, dass die Gesamtgestalt und Flexibilität jedes Zielproteins beeinflussen, wie es betroffen ist, wenn ClpC1 durch ein bestimmtes Mittel „fehlgestimmt“ wird. 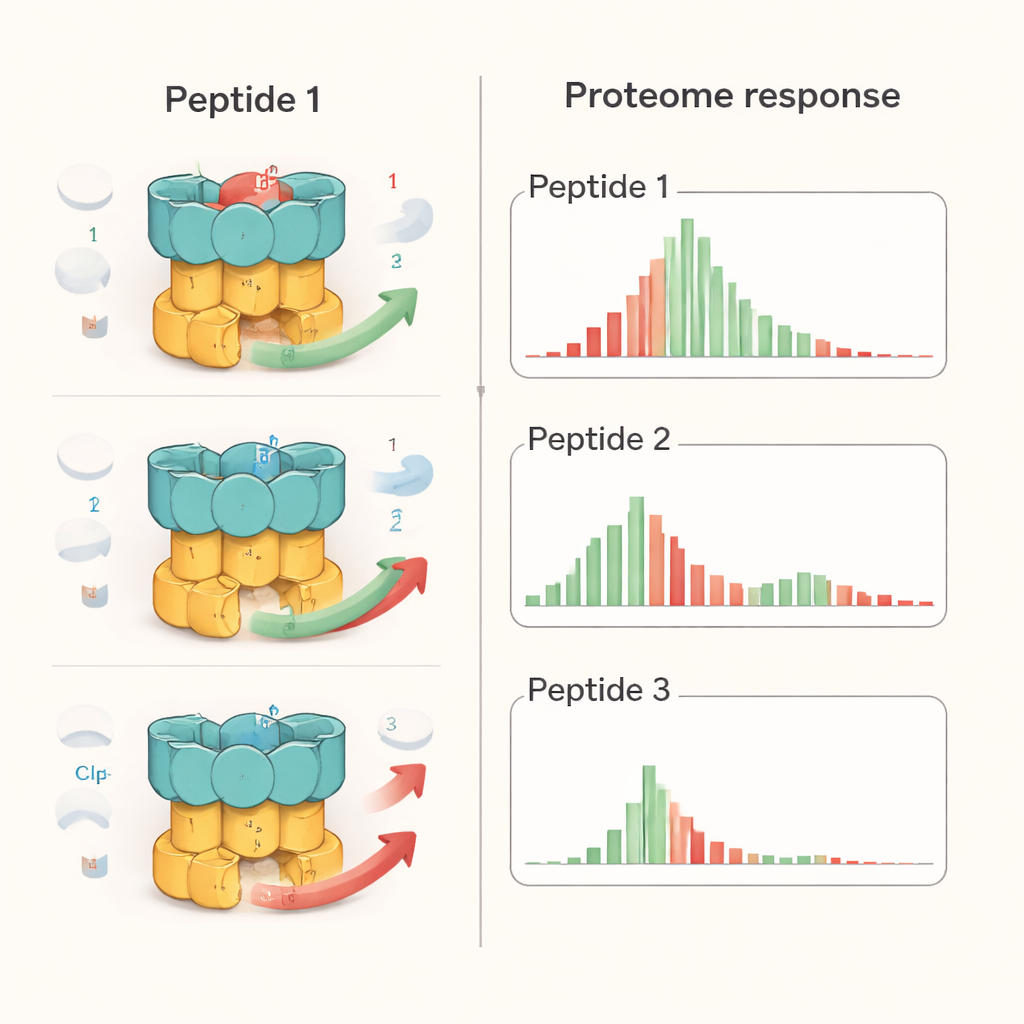
Stressantworten und bakterielle Selbstrettung
Der TB‑Erreger verfügt über Backup‑Systeme, um zurechtzukommen, wenn Proteinschäden die Hauptaufräummechanik überfordern. Ein solches System umfasst ein weiteres Chaperon, ClpC2, das cyclomarinähnliche Moleküle binden und deren Wirkung auf ClpC1 abschwächen kann. Diese Studie fand heraus, dass zwar alle drei Peptide im Reagenzglas an ClpC2 binden können, aber nur das Cyclomarin‑Derivat (dCym) tatsächlich in lebenden Bakterien erhöhte ClpC2‑Spiegel auslöste und bei experimenteller Reduktion von ClpC2 stärker wirksam wurde. Im Gegensatz dazu blieben Ecu* und IlaE wirksam, selbst wenn ClpC2 eingedämmt wurde, was darauf hindeutet, dass sie diese Selbstrettungsroute größtenteils umgehen. Das Team entdeckte außerdem eine starke, verbindungsspezifische Beziehung zu Hsp20, einem kleinen Protein, das schädliche Aggregate verhindert: Ecu* (und in geringerem Maß IlaE) führte zu dramatischen Anstiegen der Hsp20‑Spiegel, und Ecu* band Hsp20 direkt, wodurch eine neue Verbindung zwischen diesen Wirkstoffkandidaten und dem Stress‑Antwortnetzwerk der Zelle aufgedeckt wurde.
Stress in einen therapeutischen Vorteil verwandeln
Da das ClpC1‑System besonders unter widrigen Bedingungen wichtig ist, testeten die Forscher die Wirkstoffe, während die Bakterien mildem Hitzestress ausgesetzt waren, der die Last fehlgefalteter Proteine erhöht. Unter diesen Bedingungen wurden sowohl Ecu* als auch dCym deutlich tödlicher und erreichten eine Toxizität, die mit der von Bortezomib vergleichbar ist, obwohl sie selektiver wirken. Das zeigt, dass eine gezielte Beeinflussung der Protein‑Qualitätskontrolle genauso effektiv sein kann wie das Abschalten aller wichtigen Proteasen, jedoch mit potenziell präziserer Kontrolle. Die Arbeit zeigte außerdem, dass viele der durch Ecu* verursachten Veränderungen der Proteinmengen nicht einfach die Genaktivität widerspiegelten, was unterstreicht, dass die Störung von ClpC1 hauptsächlich nach der Proteinbiosynthese die Regulation beeinträchtigt.
Was das für zukünftige TB‑Behandlungen bedeutet
Für Nicht‑Fachleute ist die Kernbotschaft, dass TB‑Bakterien auf ein fein austariertes internes Aufräum‑ und Stressantwortsystem angewiesen sind, um zu überleben. Die drei hier getesteten, aus natürlichen Produkten abgeleiteten Peptide greifen alle dieselbe zentrale Maschine an, versetzen sie aber in unterschiedliche Modi, was zu vielfältigen und hochspezifischen Verzerrungen in der Proteinzusammensetzung des Bakteriums führt. Wichtig ist, dass Ecumicin‑ähnliche und Ilamycin‑ähnliche Verbindungen einen eingebauten bakteriellen Rettungsmechanismus umgehen, der die Wirkung von Cyclomarin abschwächen kann, und dennoch den Erreger unter Stress lähmen. Diese Eigenschaften machen sie zu vielversprechenden Gerüsten für zukünftige Tuberkulosemedikamente, einschließlich maßgeschneiderter Moleküle, die TB‑Zellen dazu zwingen könnten, selektiv ihre eigenen lebenswichtigen Proteine zu zerstören, oder die in „protein‑zielgerichtete Chimären“ eingebaut werden könnten, um bakterielle Selbstverdauung präzise zu lenken.
Zitation: Barter, I.K., Bedding, M.J., Leodolter, J. et al. ClpC1-targeting peptide natural products differentially dysregulate the proteome of Mycobacterium tuberculosis. Nat Commun 17, 1725 (2026). https://doi.org/10.1038/s41467-026-68423-2
Schlüsselwörter: Tuberkulose, Protein‑Qualitätskontrolle, ClpC1, Antibiotikaresistenz, natürliche Produktantibiotika