Clear Sky Science · de
Wächter-Ubiquitin-E3-Ligasen zielen auf krebsspezifische APOBEC3-Deaminasen zur Degradation ab, um die Integrität des menschlichen Genoms zu fördern
Unser Erbgut vor Kollateralschäden schützen
Unsere Zellen setzen potente Enzyme ein, um virale DNA zu beschädigen und so Infektionen abzuwehren. Einige dieser Enzyme können jedoch, wenn sie nicht kontrolliert werden, versehentlich unser eigenes Genom verletzen und zur Krebsentstehung beitragen. Diese Studie zeigt, wie menschliche Zellen diese riskanten Enzyme überwachen und enthüllt ein eingebautes „Qualitätskontroll“-System, das gefährliche Varianten markiert und zur Vernichtung freigibt, bevor sie unsere DNA umschreiben können.
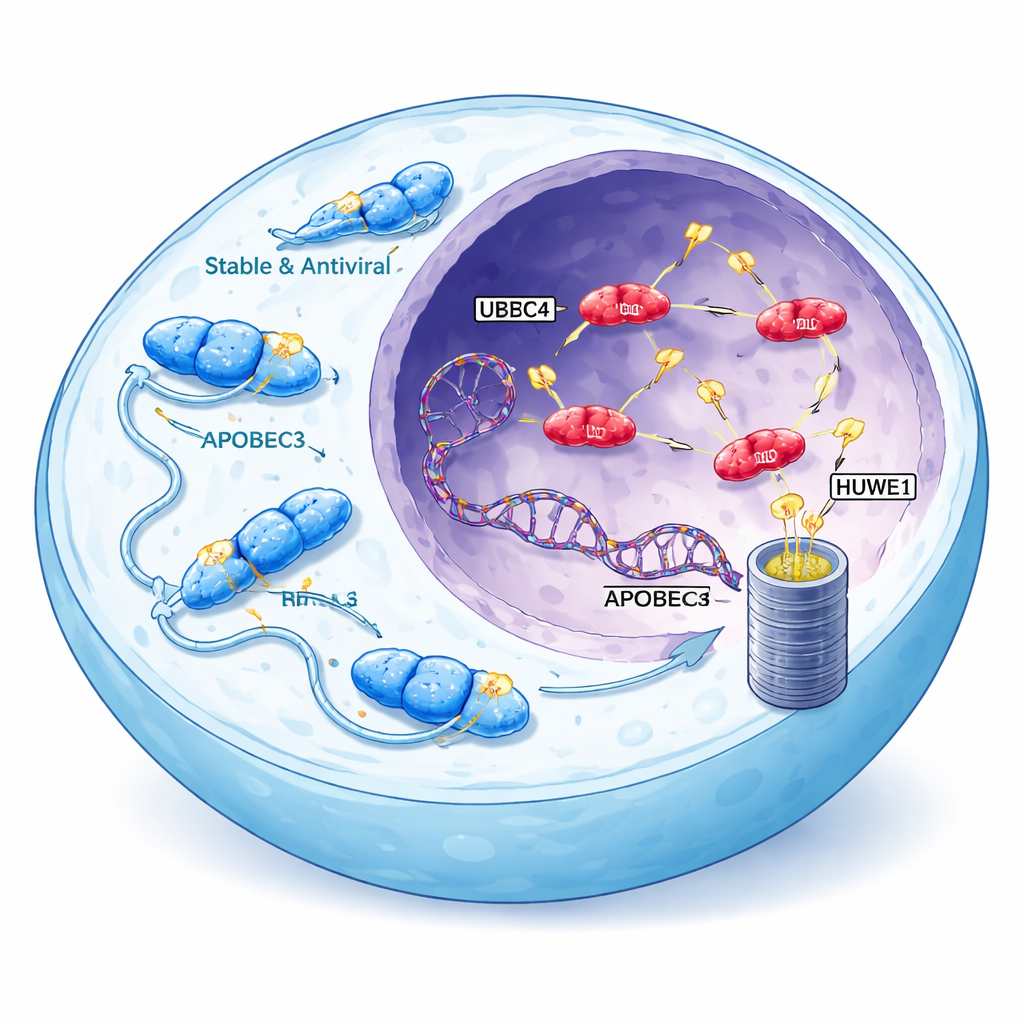
Virenkämpfer, die gegen uns selbst arbeiten können
Die APOBEC3-Familie von Enzymen hilft normalerweise, gegen Viren wie HIV vorzugehen, indem sie virale DNA chemisch verändert und so tödliche Fehler auslöst. Menschen tragen sieben APOBEC3-Varianten; drei von ihnen – A3A, A3B und eine Form von A3H, genannt Haplotyp I (A3H-I) – stehen in starkem Zusammenhang mit Mutationsmustern, die in vielen Krebsarten beobachtet werden. Diese speziellen Enzyme können in den Zellkern gelangen, wo unsere Chromosomen liegen, und charakteristische Cluster von Mutationen im Genom erzeugen. APOBEC-verbundene Signaturen treten in über der Hälfte aller menschlichen Tumoren auf, besonders bei Brust-, Lungen- und Blasentumoren, wo sie den Pool an genetischen Veränderungen vergrößern, auf die Tumoren zur Anpassung und Therapieflucht zurückgreifen können.
Warum die gefährlichsten Formen seltsam instabil sind
Interessanterweise sind die APOBEC3-Enzyme, die am stärksten mit Krebs assoziiert werden, zugleich am wenigsten stabil. Im Gegensatz zu ihren zytoplasmatischen Verwandten, die sich in hohen Mengen ansammeln und Viren effektiv blockieren, werden A3A, A3B und A3H-I schnell abgebaut und liegen im Kern meist in niedrigen Konzentrationen vor. Die Forscher vermuteten, dass diese Instabilität absichtlich ist: Wenn Zellen die Menge nuklearer APOBEC3-Proteine aktiv begrenzen, könnte ein Ausfall dieser Kontrolle bursts von Mutagenese freisetzen. Anhand von A3H-I als Modell zeigten sie, dass krebsspezifische APOBEC3s hauptsächlich vom Proteasom, dem Proteinzerkleinerer der Zelle, abgebaut werden, nachdem sie an mehreren Aminosäurestellen mit kleinen molekularen „Flaggen“ namens Ubiquitin markiert wurden.
Die zellulären Wächter finden
Um die Maschinerie zu identifizieren, die A3H-I und A3B markiert, kombinierten die Forscher CRISPR-Screening mit Protein-Näherungs-Kartierung. Sie konstruierten Zellen, die je nach Stabilität von A3H-I und seiner harmlosen Variante A3H-II unterschiedlich leuchten, und schalteten systematisch Gene aus, die am Proteinabbau beteiligt sind. Drei Ubiquitin-Ligasen – UBR4, UBR5 und HUWE1 – hoben sich hervor. Das Entfernen jeder einzelnen dieser Ligasen erhöhte selektiv die Menge des instabilen, nukleären A3H-I, ohne das stabile, zytoplasmatische A3H-II zu beeinflussen. Dieselben Ligasen steigerten unabhängig voneinander auch die Mengen des endogenen A3B in Darm- und Immunzelllinien, und die gleichzeitige Deletion aller drei führte zu einer additiven Zunahme von A3B. Biochemische Experimente zeigten weiter, dass UBR5 und HUWE1 physisch an A3B und A3H-I binden und unmittelbar Ubiquitin-Ketten anhängen, während UBR4 offenbar darauf spezialisiert ist, diese Ketten zu verlängern, damit die Proteine effizienter abgebaut werden können.
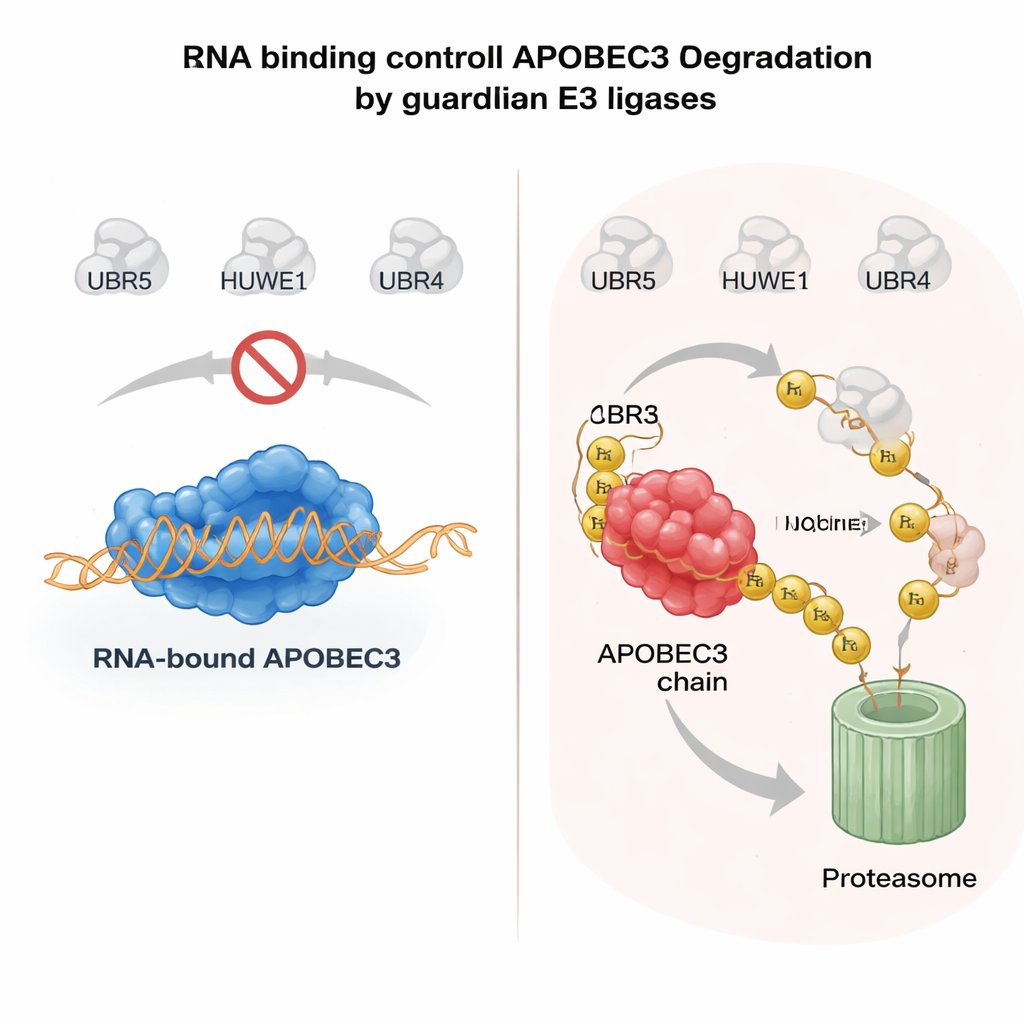
RNA als Sicherheitsgurt für riskante Enzyme
Was bestimmt, ob ein APOBEC3-Enzym verschont oder zerstört wird? Ein wichtiger Hinweis ergab sich aus der Art und Weise, wie APOBEC3-Proteine an RNA-Moleküle im Zytoplasma binden. Wenn A3H oder ein anderes Familienmitglied, A3G, RNA bindet, verbleiben sie tendenziell in großen Komplexen im Zytosol und sind relativ stabil. Mutationen, die die RNABindung schwächen, führen dazu, dass diese Enzyme in den Kern abwandern, ihre schützenden Partner verlieren und hochgradig instabil werden. Die Autoren zeigten, dass, wenn APOBEC3-Proteine nicht an RNA gebunden sind, UBR5 und HUWE1 freiliegende Oberflächen des Enzyms erkennen, sie mit Ubiquitin versehen und für den nuklearen Abbau markieren. In gereinigten Systemen verstärkte das Zugaben von RNase, das die RNA entfernt, deutlich die Fähigkeit dieser Ligasen, an APOBEC3 zu binden und es zu ubiquitinieren, was bestätigt, dass die RNABindung als molekularer Schild wirkt. Dieser Mechanismus erlaubt es den Zellen, antivirale APOBEC3s im Zytoplasma aktiv zu halten und gleichzeitig ungebundene, genome-bedrohende Pools im Kern rasch zu beseitigen.
Wenn die Wächter versagen: Verbindungen zu Krebsmutationen
Wenn UBR4, UBR5 und HUWE1 als Wächter fungieren, sollte ihr Verlust die Mutationsrate erhöhen. Die Forscher prüften dies, indem sie jede Ligase in Darmkrebszellen deaktivierten und DNA-Veränderungen im Zeitverlauf mit einer sensitiven Sequenziermethode verfolgten, die mutationale „Signaturen“ liest. Das Entfernen dieser Ligasen, insbesondere in Zellen, die A3H-I exprimieren, verstärkte APOBEC-spezifische Mutationsmuster – genau die Art, die in menschlichen Tumoren gefunden wird. In Patientendaten analysierten sie Tausende von Krebsgenomen und fanden, dass Tumoren mit Mutationen in UBR5 oder HUWE1 einen signifikant höheren Anteil an APOBEC-verbundenen Mutationssignaturen aufwiesen als Tumoren mit intakten Ligasen, selbst nach Kontrolle der gesamten Mutationslast. Das deutet darauf hin, dass defekte Wächter-Ligasen bei Patienten krebsspezifische APOBEC3-Enzyme enthemmen und das Tumorgenom umgestalten können.
Was das für die künftige Krebsversorgung bedeutet
Für Nichtfachleute lässt sich festhalten: Unsere Zellen verfügen über ein ausgeklügeltes Überwachungssystem, um zu verhindern, dass hilfreiche antivirale Enzyme unser eigenes Erbgut sabotieren. UBR4, UBR5 und HUWE1 fungieren als Wächter, die erkennen, wenn APOBEC3-Enzyme nicht mehr sicher an RNA gebunden sind, und insbesondere im Kern die Proteine zum zellulären Schredder schicken. Wenn dieses Kontrollsystem geschwächt ist – durch Mutationen in den Ligasen oder durch Medikamente, die den Proteinabbau blockieren – kann APOBEC3-Aktivität das genetische Chaos befeuern, das Krebsentwicklung und Therapieresistenz vorantreibt. Das Verständnis dieses Wächternetzwerks eröffnet Wege zu neuen diagnostischen Markern, wie Ligase-Mutationen oder APOBEC-Proteinspiegeln, und deutet darauf hin, dass eine gezielte Modulation dieses Pfads eines Tages helfen könnte, schädliche Mutationsausbrüche in Tumoren zu begrenzen, ohne unsere antiviralen Abwehrmechanismen zu gefährden.
Zitation: Schwartz, I., Budroni, V., Meyenberg, M. et al. Guardian ubiquitin E3 ligases target cancer-associated APOBEC3 deaminases for degradation to promote human genome integrity. Nat Commun 17, 1723 (2026). https://doi.org/10.1038/s41467-026-68420-5
Schlüsselwörter: APOBEC3, Genomstabilität, Ubiquitin-Ligase, Krebsmutagenese, Proteinabbau