Clear Sky Science · de
Räumliche Musterbildung der Kontraktilität durch einen selbstorganisierten Mechanogen-Aktivitätsgradienten liegt der Gastrulation von Drosophila zugrunde
Wie Gewebe sich selbst formen
Frühe Embryonen verwandeln auf ungeklärte Weise einfache Zellschichten in komplexe dreidimensionale Formen. Diese Studie stellt eine grundlegende Frage hinter diesem Kunststück: Wie koordinieren Zellen, wo sie zusammenziehen und sich biegen müssen, damit ein Gewebe an der richtigen Stelle und in die richtige Richtung faltet? Durch hochauflösende Beobachtungen von Fliegenembryonen identifizieren die Autoren ein chemisches Signal, das wie ein „mechanischer Morphogen“ wirkt und direkt vorgibt, wo Zellen an sich selbst ziehen, um ein entscheidendes Faltungsereignis in der Entwicklung anzutreiben.
Eine Welle, die den Embryo faltet
Beim Fruchtfliegen-Genus Drosophila ist ein wichtiger Schritt der frühen Entwicklung die Gastrulation, bei der eine flache Zellschicht nach innen knickt und damit beginnt, den Darm zu bilden. Im Hinterteil des Embryos startet ein Zellfeld, das als posteriorer Endoderm-Primordium bezeichnet wird, diesen Prozess durch Kontraktion an ihrer oberen (apikalen) Seite. Diese anfängliche Biegung löst eine fortschreitende Welle der Gewebeinvagination aus, die sich über benachbarte Zellen nach vorn ausbreitet. Die Autoren zeigen, dass diese Welle von einem Signal namens Fog abhängt, einem sezernierten Molekül, das eine Familie von Rezeptoren aktiviert, die als GPCRs bekannt sind; diese schalten wiederum die kontraktile Maschinerie der Zelle auf Basis des Motorproteins Myosin-II ein.
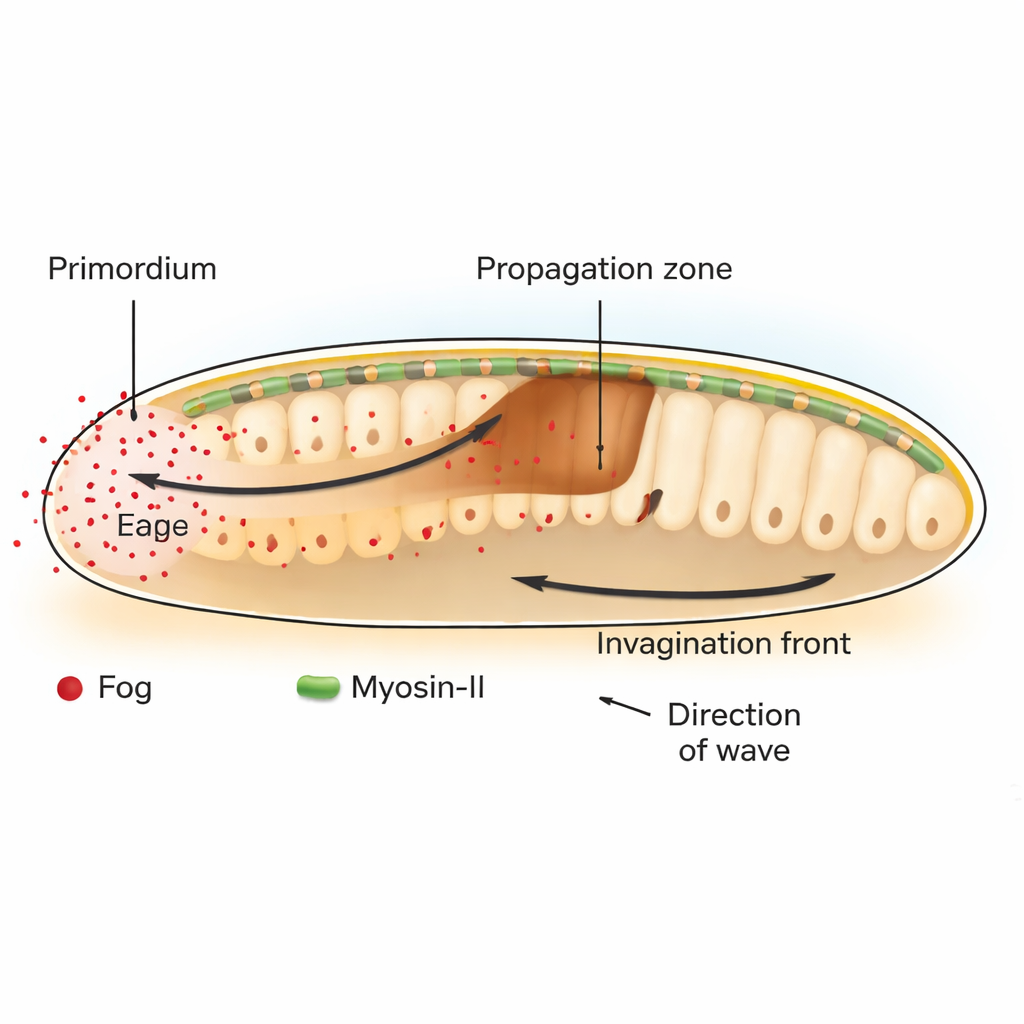
Ein Chemischer, der Kraft statt Schicksal gestaltet
Klassischerweise konzentrieren sich Entwicklungsbiologinnen und -biologen auf „Morphogene“, diffundierende Moleküle, deren Konzentrationsgradienten Zellen sagen, welche Identität sie annehmen sollen. Hier verhält sich Fog anders. Statt zu bestimmen, welcher Zelltyp ein Gebiet wird, reguliert Fog direkt, wie stark Zellen kontrahieren. Indem die Forschenden Fog und seinen nachgeschalteten Boten Gα selektiv in bestimmten Regionen wiederherstellen oder blockieren, zeigen sie, dass das im Primordium produzierte Fog sowohl notwendig als auch ausreichend ist, um Myosin-II-Aktivierung und Gewebefaltung in der angrenzenden Propagationszone auszulösen. Wenn Fog so verankert wird, dass es sich nicht verbreiten kann, kontrahieren nur die produzierenden Zellen und die Invaginationswelle stockt bereits nach ein oder zwei Zellreihen.
Ein verborgener Gradient an der Zelloberfläche
Eine naheliegende Idee ist, dass Fog einen klassischen Konzentrationsgradienten außerhalb der Zellen bildet. Mit einer fluoreszenzmarkierten Fog-Variante und empfindlichen Fluoreszenzmessungen stellt das Team jedoch das Gegenteil fest: in der dünnen Flüssigkeitsschicht zwischen dem Gewebe und seiner umschließenden Hülle (der Vitellinmembran) ist Fog bemerkenswert gleichmäßig verteilt. Dennoch bildet Myosin-II-Aktivität klar einen steilen, wandernden Gradient, der direkt vor der voranschreitenden Falte am stärksten ist und nach einigen Zell-Durchmessern abnimmt. Der fehlende Baustein ist, dass Fog nicht als einfacher Bulk-Konzentrationshinweis wirkt; stattdessen wird ein kleiner Anteil von Fog kurzzeitig an der Zelloberfläche gebunden, heftet sich an GPCR-Rezeptoren und bildet so einen oberflächengebundenen Aktivitätsgradienten, obwohl die freien Fog-Moleküle im Fluid gleichmäßig verteilt bleiben.
Rezeptoren, Endozytose und Adhäsion formen die Welle
Die Autoren zeigen, dass dieses oberflächengebundene Fog zusammen mit seinen Rezeptoren ein Muster selbst organisiert. Dort, wo Fog wiederholt auf Rezeptoren trifft, fördert es Rezeptor-Clusterbildung und -aktivierung, was mehr Myosin-II rekrutiert. Ein zellulärer „Aufräum“-Prozess — die GPCR-Endozytose — entfernt anschließend aktive Komplexe, verhindert unkontrollierte Aktivierung und hilft, die Ausbreitungsdistanz des Signals zu justieren. Wird diese Endozytose genetisch verlangsamt, wird der Myosin-II-Gradient höher und breiter. Ein zweiter wichtiger Akteur sind Integrine, eine Klasse von Adhäsionsmolekülen. Wenn sich das Gewebe biegt, drücken die Zellen vor der Falte gegen die Vitellinmembran; dieser Kontakt aktiviert lokal Integrine, die wiederum die Wirksamkeit der Fog–GPCR-Signalgebung verstärken. Das Gebiet starker Integrin-Engagements stimmt mit dem Ausmaß des Myosin-II-Gradienten überein, und ohne Integrine wird die Welle schwach und kurzreichweitig, selbst wenn die Fog-Signalgebung sonst verstärkt ist.
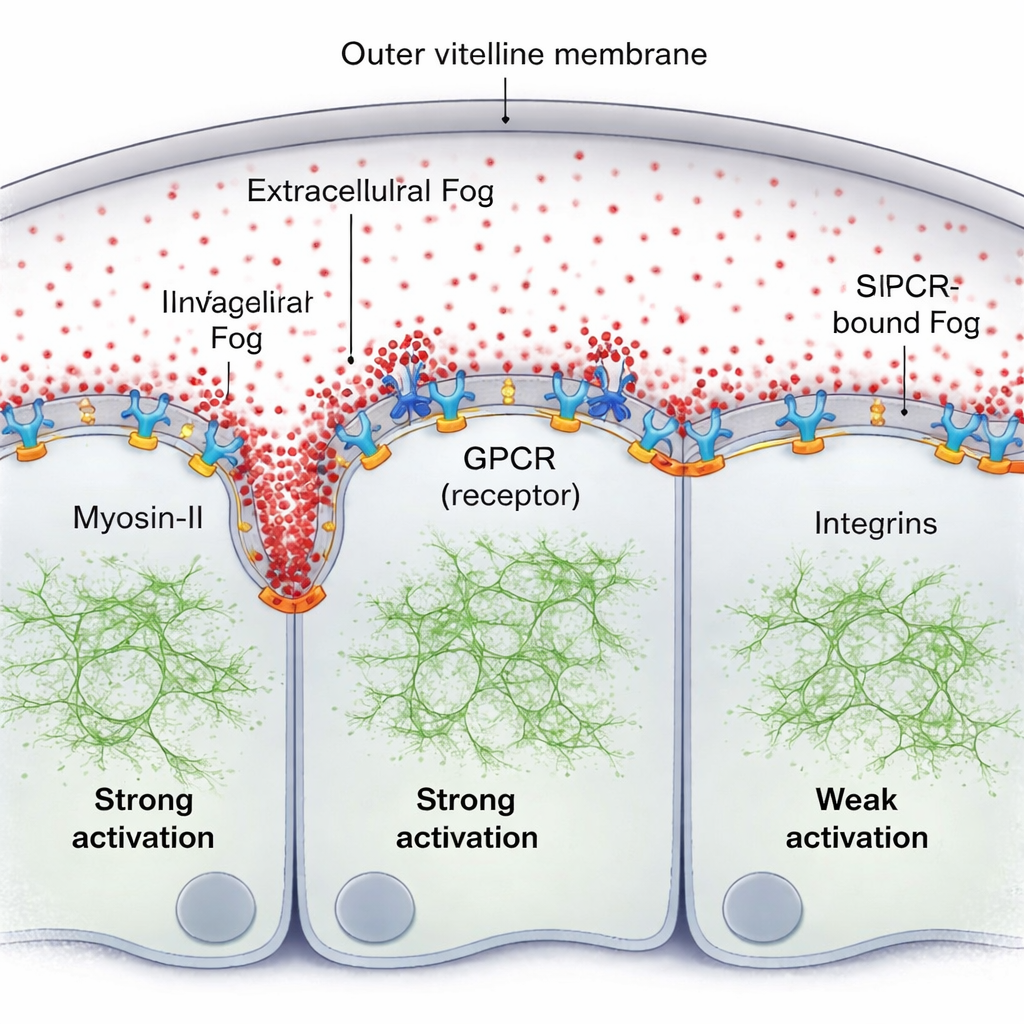
Ein sich selbst erneuerndes mechanisches Muster
Für einen Nichtfachmann ist die Hauptbotschaft, dass der Embryo sich nicht ausschließlich auf vorgezeichnete chemische Karten verlässt, um zu entscheiden, wo er faltet. Stattdessen baut er ein bewegtes Muster mechanischer Aktivität „on the fly“ auf. Fog verbreitet sich einheitlich, doch seine effektive Wirkung wird an der Zelloberfläche durch Rezeptor-Clusterbildung, Rezeptorentfernung und veränderliche Geometrie des Gewebes beim Andrücken an die Umgebung geformt. Das erzeugt einen selbstorganisierten, wandernden Gradient kontraktiler Kräfte, der das Gewebe in einer koordinierten Welle nach innen zieht. Die Arbeit liefert ein konkretes Beispiel für einen seit Langem theoretisch diskutierten „Mechanogen“: ein diffundierendes Molekül, das direkt die physikalischen Kräfte in einem Gewebe mustert und so hilft zu erklären, wie lebende Formen sich während der Entwicklung so zuverlässig formen.
Zitation: Mundhe, G., Dunsing-Eichenauer, V., Philippe, JM. et al. Spatial patterning of contractility by a self-organized mechanogen activity gradient underlies Drosophila gastrulation. Nat Commun 17, 1721 (2026). https://doi.org/10.1038/s41467-026-68418-z
Schlüsselwörter: Gastrulation, Mechanogen, Drosophila-Embryo, Gewebe-Mechanik, Fog-Signalgebung