Clear Sky Science · de
Konfigurationen von DNA-Enden bestimmen die Bildung synaptischer Komplexe während der NHEJ-vermittelten End‑Brückenbildung
Wenn DNA bricht, müssen Zellen schnell handeln
Tagtäglich wird die DNA in unseren Zellen durch normalen Stoffwechsel und Umweltstress angeschlagen, eingeschnitten und beschädigt. Zu den gefährlichsten Verletzungen zählen Doppelstrangbrüche, bei denen beide Stränge der DNA-Helix durchtrennt werden. Werden diese Brüche nicht schnell und korrekt repariert, können Zellen absterben oder — schlimmer noch — auf einen krebsigen Pfad geraten. Diese Studie untersucht, wie die exakte Form und Chemie der gebrochenen DNA‑Enden beeinflusst, ob ein wichtiger Reparaturweg, die nicht-homologe Endverknüpfung (NHEJ), diese Enden effizient und mit möglichst wenigen Fehlern zusammenführt.
Zwei Wege, gebrochene DNA zusammenzubringen
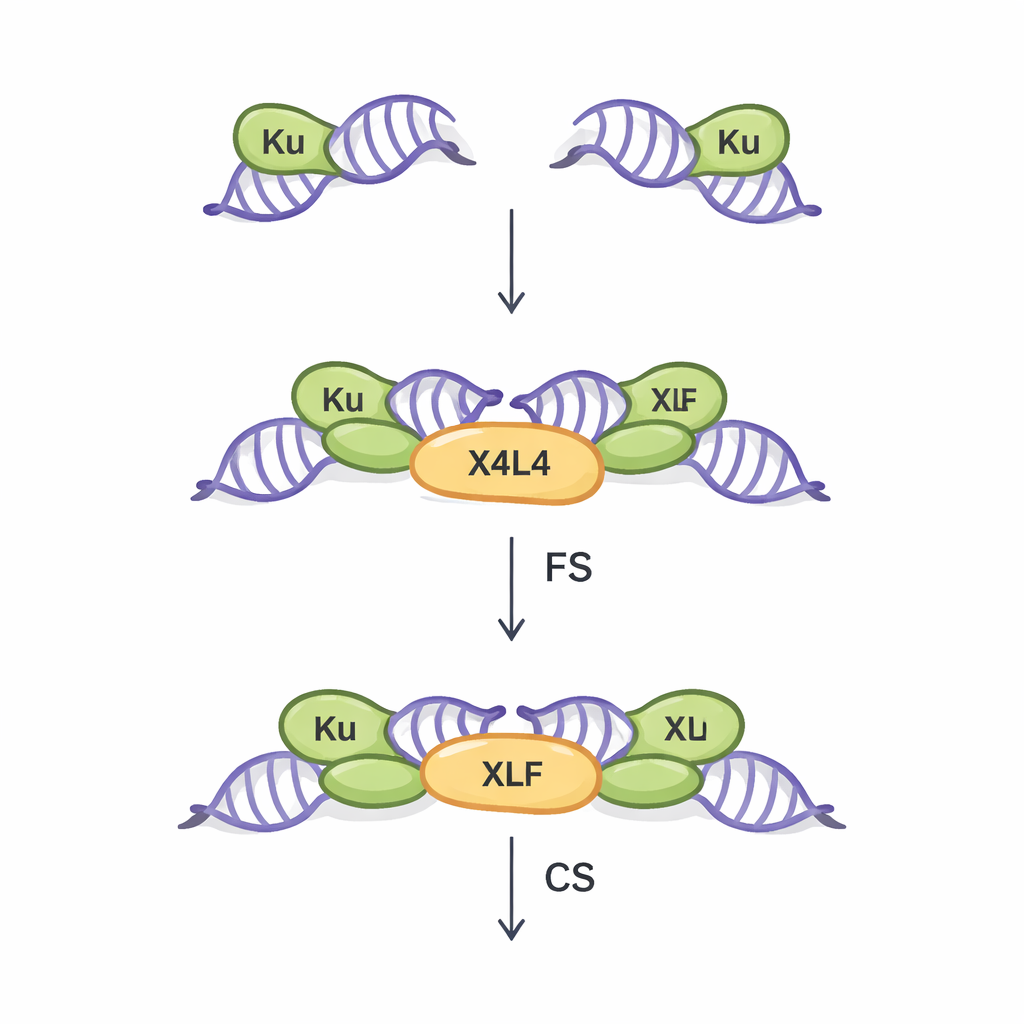
NHEJ ist der wichtigste Reparaturweg für Doppelstrangbrüche in den meisten Körperzellen. Er funktioniert ohne eine passende DNA‑Vorlage, wodurch er schnell, aber etwas fehleranfällig ist. Der erste entscheidende Schritt dieses Wegs wird Synapsis genannt: das physikalische Überbrücken der beiden gebrochenen DNA‑Enden, damit sie später verbunden werden können. Frühere Arbeiten, meist mit idealisierten stumpfen DNA‑Enden, zeigten zwei Arten synaptischer Anordnungen. Im „flexiblen synaptischen“ (FS) Zustand werden die Enden nahe beieinander gehalten und können sich bewegen, um Paarungsmöglichkeiten auszuloten. Im „nahen synaptischen“ (CS) Zustand liegen die Enden Ende an Ende und sind bereit für das Verschließen durch ein Ligasen‑Enzym. Drei Kernproteine — Ku, XRCC4–Ligase IV (zusammen X4L4 genannt) und XLF — sind bekannt dafür, diesen Prozess zu koordinieren, doch wie realistische, unregelmäßige DNA‑Enden beeinflussen, welcher synaptische Zustand entsteht, war lange unklar.
Endform und kurze Übereinstimmungen steuern den Reparaturweg
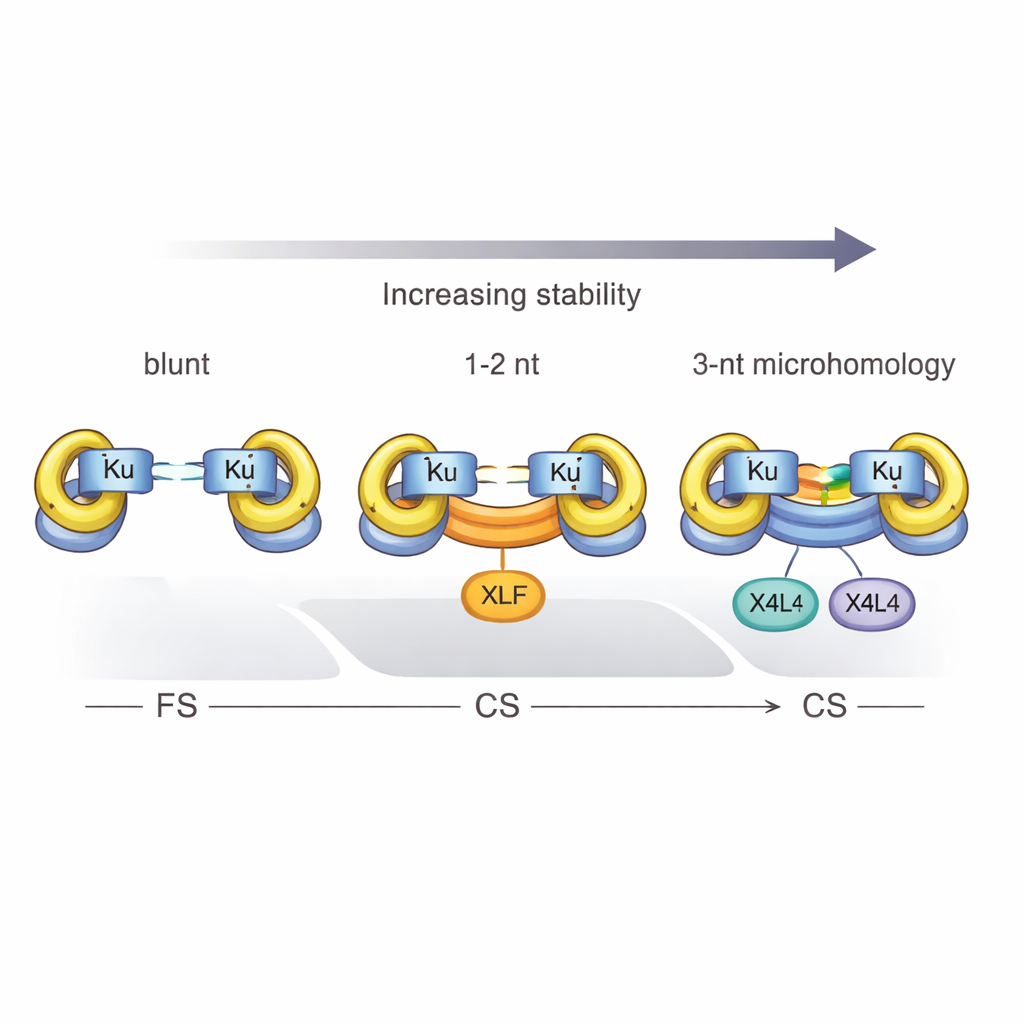
Die Forscher verwendeten Einzelmolekül‑FRET, eine fluoreszenzbasierte Technik, die Abstände im Nanometerbereich verfolgt, um einzelne DNA‑Moleküle zu beobachten, während sie von NHEJ‑Proteinen zusammengebracht wurden. Sie verglichen einfache stumpfe Enden mit realistischeren Enden, die kurze Überhänge tragen — kleine einzelsträngige Schwänze, die sich potenziell paaren können. Sie stellten fest, dass komplementäre Überhänge, selbst wenn sie nur wenige Basen umfassen, die Wahrscheinlichkeit für die Bildung eines nahen synaptischen Komplexes dramatisch erhöhen. Tatsächlich reichten schon drei passende Basen der sogenannten „Mikrohomologie“ an der Bruchstelle aus, damit Ku und X4L4 allein einen stabilen CS‑Komplex bilden konnten, ohne XLF. Das zeigt, dass die DNA selbst einen Teil der Energie und Orientierung liefern kann, die sonst von Helferproteinen bereitgestellt werden.
Wie winzige DNA‑Lappen die Brücke stabilisieren
Durch die Analyse unterschiedlicher FRET‑Signaturen entdeckte das Team mindestens zwei strukturelle Varianten des nahen synaptischen Zustands bei überhängenden Enden. In der einen paaren sich die very Spitzen der Überhänge miteinander und erzeugen eine eingeschnittene oder gapped Verbindung. In der anderen pressen die Übergangsstellen, an denen doppelsträngige DNA auf einzelsträngige Überhänge treffen, inline gegeneinander, während die Überhänge wie kleine Lappen nach außen klappen. Diese Lappen erlauben weiterhin Basenpaarung und halten die Enden sehr dicht beieinander, was wahrscheinlich den Komplex stabilisiert und den Enzymen Raum gibt, die DNA bei Bedarf zu kürzen oder zu verlängern, bevor das finale Verschließen erfolgt. Interessanterweise beeinflusste häufige oxidative Schädigung in den Überhängen, etwa 8‑Oxoguanin, diesen Prozess nur mäßig — ein Hinweis darauf, wie robust NHEJ gegenüber bestimmten Schadensformen ist.
Proteine, Phosphate und die Kraft der Drei
Die Studie definierte außerdem eine klare Schwelle: Mindestens drei komplementäre Basenpaare sind erforderlich, damit Ku und X4L4 verlässlich einen flexiblen Komplex in einen nahen umwandeln. Bei nur einem oder zwei Übereinstimmungen bleibt das System meist im flexiblen Zustand stecken, es sei denn, XLF greift ein und hilft, die Enden zusammenzuklemmen. Auch chemische Details spielen eine Rolle. Trägt die gebrochene DNA eine 5′‑Phosphatgruppe — ein normales Merkmal vieler physiologischer Brüche — wird die Synapsis effizienter, und nahe Komplexe werden eher auch wirklich ligiert, wodurch eine temporäre Brücke in eine dauerhafte Reparatur überführt wird. Dieser Phosphat‑Effekt kann die stabilisierende Wirkung von Basenpaarung an der Bruchstelle jedoch nicht vollständig ersetzen.
Warum das für Gesundheit und Genomeditierung wichtig ist
Einfach formuliert zeigt diese Arbeit, dass gebrochene DNA‑Enden keine passiven Opfer sind, die auf Reparatur warten. Ihre genaue Form, winzige Patches übereinstimmender Sequenz und chemische Markierungen lenken aktiv, wie Reparaturproteine sie fassen, ausrichten und wieder verbinden. Sind drei oder mehr passende Basen vorhanden, helfen die DNA‑Enden selbst mit, den Bruch in eine reparaturbereite Konfiguration zu verriegeln und machen manche Helferproteine optional. Fehlen solche Übereinstimmungen, werden zusätzliche Proteinfaktoren zwingend erforderlich. Diese Erkenntnisse erklären, warum manche Brüche sauber verheilen, während andere zu kleinen Mutationen oder Umlagerungen führen. Sie liefern zudem Hinweise zur Verbesserung von Genome‑Editing‑Werkzeugen wie CRISPR, bei denen gezielt erzeugte DNA‑Brüche durch dieselbe NHEJ‑Maschinerie repariert werden. Durch Feinabstimmung der Bruchenden könnten Forschende besser steuern, wie das Genom umgestaltet wird.
Zitation: Zhang, C., Jin, W., Jiang, Y. et al. DNA end configurations dictate synaptic complex formation during NHEJ-mediated end bridging. Nat Commun 17, 1720 (2026). https://doi.org/10.1038/s41467-026-68417-0
Schlüsselwörter: Reparatur von Doppelstrangbrüchen in der DNA, nicht-homologe Endverknüpfung, DNA-Synapse, Mikrohomologie, Genomstabilität