Clear Sky Science · de
Ein einzelner Valin‑zu‑Leucin‑Tausch stört die DNA‑Bindung von Plasmodium falciparum AP2‑G und enthüllt GDV1s Rolle bei der Aktivierung von ap2‑g
Wie Malariaparasiten eine lebenswichtige Entscheidungsfrage treffen
Malariaparasiten im Blut stehen ständig vor einer folgenreichen Wahl: weiter im Wirt zu vermehren oder in eine Form umzuschalten, die durch einen Mückenstich zum nächsten Wirt springen kann. Diese Studie zeigt, wie eine einzige winzige Änderung in einem Parasitenprotein die infektiöse, mückenfähige Phase vollständig ausschalten kann und damit neue Ansatzpunkte zum Blockieren der Malariübertragung eröffnet.
Die Weggabelung des Parasiten
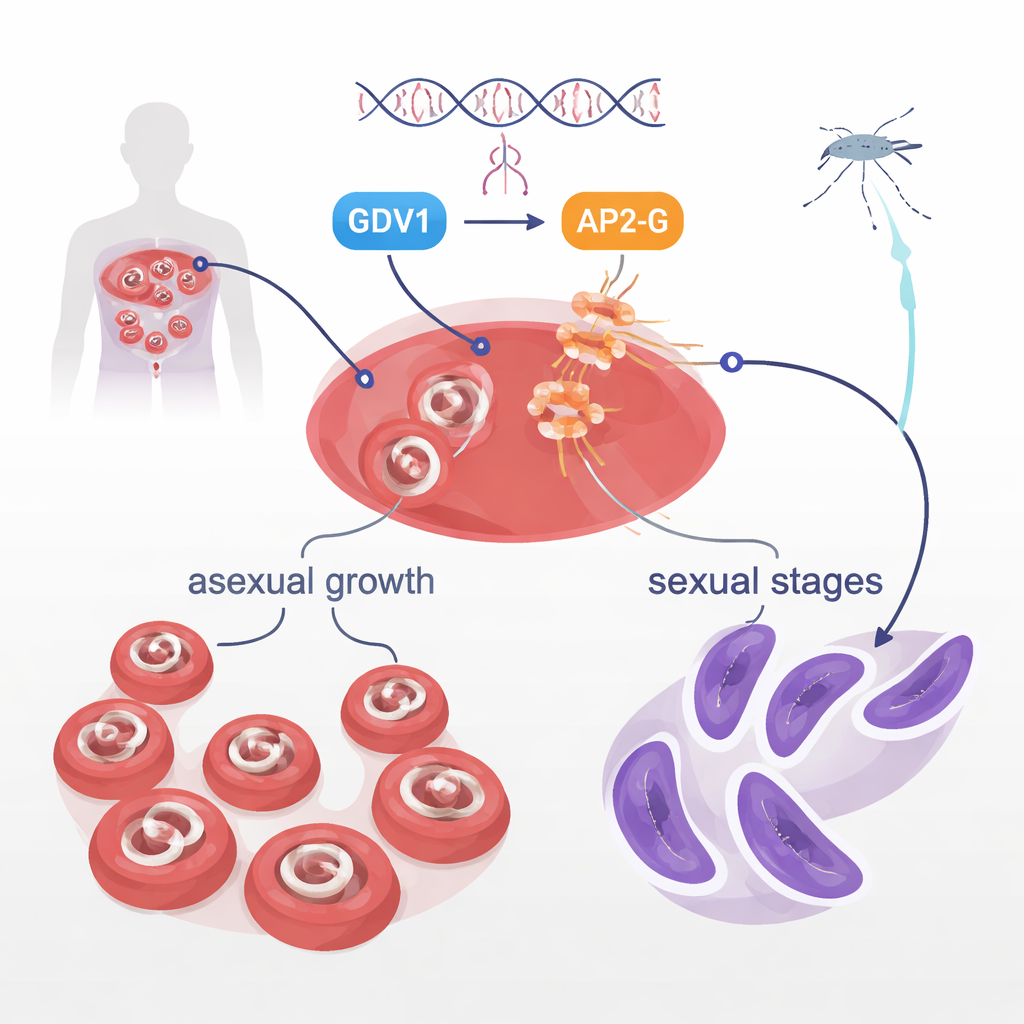
Im Blut konzentrieren sich Plasmodium falciparum‑Parasiten überwiegend auf schnelles Wachstum, was Krankheit verursacht. Eine kleine Minderheit wandelt sich jedoch in sexuelle Formen, die Gametozyten genannt werden und die einzigen Stadien sind, die Mücken aufnehmen und weitergeben können. Warum nur einige Parasiten in einer Population diesen Umschlag vollziehen, war lange rätselhaft. Frühere Arbeiten zeigten, dass zwei Parasitenproteine, GDV1 und ein DNA‑bindendes Protein namens AP2‑G, im Zentrum dieser Entscheidung stehen. GDV1 hilft, das normalerweise stille ap2‑g‑Gen zu wecken, und AP2‑G schaltet daraufhin ein Programm von Genen ein, das die sexuelle Entwicklung antreibt. Die vorliegende Studie wollte ursprünglich ein weiteres Protein, eine Kinas e namens STK2, untersuchen, stieß aber stattdessen auf eine weit dramatischere Entdeckung im AP2‑G selbst.
Eine einzelne Aminosäure, die die Übertragung stoppt
Beim Entfernen des stk2‑Gens in einem Laborstamm stellten die Forschenden fest, dass diese Parasiten völlig die Fähigkeit verloren, Gametozyten zu produzieren, während ihr asexuelles Wachstum unbeeinträchtigt blieb. Überraschenderweise bildeten in einem anderen Stamm ähnliche Manipulationen normale Gametozyten. Die Analyse der gesamten Genome enthüllte den versteckten Schuldigen: eine einzelne „Buchstaben“änderung im ap2‑g‑Gen, die eine Aminosäure—Valin—durch eine sehr ähnliche, Leucin, an Position 2163 ersetzt. Diese Position liegt ganz am Beginn der DNA‑Bindedomäne von AP2‑G, dem Bereich, der spezifische DNA‑Motifs physikalisch greift, um Gene zu aktivieren. Dieser winzige Valin‑zu‑Leucin‑Tausch allein reichte aus, die Gametozytenbildung zu verhindern. Als die Forscher diese Mutation in ansonsten normalen Parasiten einbauten, verschwanden die Gametozyten; bei Rückkehr zur Valin‑Variante wurde die sexuelle Entwicklung vollständig wiederhergestellt.
Wie der Tausch das molekulare Schloss zerstört
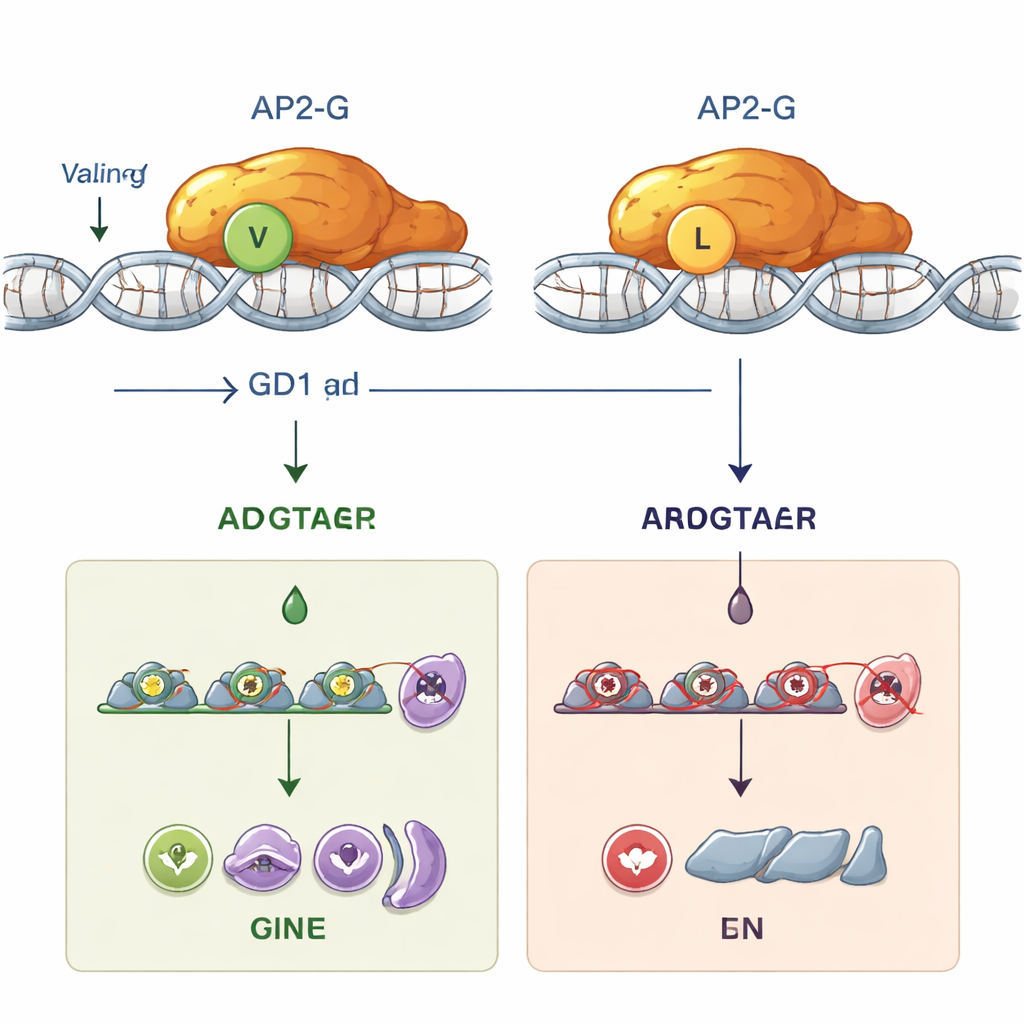
Um zu verstehen, warum diese subtile Änderung so verheerend ist, kombinierten die Forschenden Computermodellierung mit Laborversuchen. Strukturvorhersagen deuteten darauf hin, dass der Austausch von Valin gegen Leucin die genaue Form der AP2‑DNA‑Bindedomäne verschiebt und destabilisiert. In Reagenzglas‑Assays mit gereinigten Proteinen band normales AP2‑G stark an seine bevorzugte DNA‑Sequenz, einen kurzen Code mit dem Motiv „GnGTAC“. Im Gegensatz dazu konnte das mutierte AP2‑G mit Leucin an Position 2163 diese Sequenz überhaupt nicht binden. Ohne stabile DNA‑Bindung konnte AP2‑G sein eigenes Gen (eine positive Rückkopplung, bekannt als Autoregulation) nicht einschalten und auch dutzende nachgeschaltete Gene nicht aktivieren, die nötig sind, um Parasiten in den sexuellen Weg zu treiben. Funktionell wurden die mutierten Parasiten „steril“: Sie konnten die für Mücken infektiösen Formen nicht bilden, obwohl sie in den roten Blutkörperchen weiterhin gediehen.
GDV1s verborgene Rolle bevor AP2‑G übernimmt
Die Mutation lieferte den Forschenden auch ein einzigartiges Werkzeug: Parasiten, bei denen das ap2‑g‑Gen zwar angeschaltet werden kann, AP2‑G aber nicht an DNA binden kann. Mithilfe fluoreszierender und lichtemittierender Reporter verfolgten sie, wann verschiedene Akteure im 48‑Stunden‑Zyklus des Parasiten in roten Blutkörperchen aktiv werden. Sie fanden heraus, dass das GDV1‑Protein zuerst erscheint, früh in einer Phase namens Schizogonie, und unerlässlich ist, um das stillgelegte ap2‑g‑Gen zu starten. Diese frühe Aktivierung geschah unabhängig davon, ob ap2‑g normales oder mutiertes AP2‑G kodierte. Erst später, sobald sich genügend normales AP2‑G aufgebaut hatte, setzte die starke Selbstverstärkung und die Aktivierung weiterer „sexueller“ Gene ein. Ein wichtiger Marker, ein Protein namens MSRP1, leuchtete nur in Parasiten mit funktionalem AP2‑G und ermöglichte so eine einfache Unterscheidung zwischen früh und spät sexuell verpflichteten Parasiten. In den mutierten Linien mit dem Leucin‑Tausch konnte GDV1 ap2‑g zwar weiterhin wecken, aber das defekte AP2‑G‑Protein konnte den Prozess nicht weiter vorantreiben, sodass die sexuelle Entwicklung ins Stocken geriet.
Folgen für das Stoppen der Malariaverbreitung
Für eine allgemeine Leserschaft ist die Quintessenz einfach: Malariaparasiten verlassen sich auf ein extrem sensibles molekulares Schloss, um zu entscheiden, ob sie übertragbar werden. Diese Studie zeigt, dass das Austauschen nur eines „Zahns“ in diesem Schloss—eines einzelnen Valins in der DNA‑greifenden Region von AP2‑G—den Parasiten daran hindert, je mückeninfektiöse Stadien zu produzieren. Gleichzeitig klärt sie, dass ein anderes Protein, GDV1, früher als Schlüssel wirkt, um zunächst das stille ap2‑g‑Gen zu öffnen, bevor AP2‑G seine eigene Produktion verstärkt und ein breiteres sexuelles Programm einschaltet. Durch die Kartierung dieser Abfolge von Ereignissen und die Erstellung von Reporter‑Parasitenlinien, die bei jedem Schritt aufleuchten, liefert die Arbeit mächtige Werkzeuge, um Wirkstoffe oder menschliche Faktoren zu screenen, die die sexuelle Verpflichtung stören. Langfristig könnte die gezielte Beeinflussung der DNA‑Bindedomäne von AP2‑G oder des GDV1‑getriebenen Aktivierungsschritts die Basis neuer Strategien bilden, die nicht nur Malaria bei einem Patienten heilen, sondern die Übertragungskette insgesamt durchbrechen.
Zitation: Prajapati, S.K., Dong, J.X., Morahan, B.J. et al. A single valine to leucine switch disrupts Plasmodium falciparum AP2-G DNA binding and reveals GDV1’s role in ap2-g activation. Nat Commun 17, 1719 (2026). https://doi.org/10.1038/s41467-026-68416-1
Schlüsselwörter: Malariatransmission, Plasmodium falciparum, Gametocytentwicklung, AP2‑G, GDV1