Clear Sky Science · de
Multimodale KI für opportunistisches Screening, Stadieneinteilung und Risikostratifizierung des Fortschreitens der steatotischen Lebererkrankung
Warum Leberfett und Narbenbildung für alle wichtig sind
Fettlebererkrankung ist nicht mehr selten oder speziell: Etwa jeder dritte Erwachsene weltweit hat vermehrtes Fett in der Leber, und diese Zahl steigt. Bei vielen Menschen bleibt das unbemerkt, doch bei anderen führt es zu gefährlicher Narbenbildung (Fibrose), Leberzirrhose, Leberkrebs und Herzproblemen. Gleichzeitig erhalten Millionen von Menschen CT‑Scans aus anderen Gründen – Brustschmerzen, Krebsnachsorge oder Routineuntersuchungen – ohne dass ihre Leber dabei genau betrachtet wird. Diese Studie stellt eine einfache, aber wirkungsvolle Frage: Könnte künstliche Intelligenz (KI) diese vorhandenen Bilder unauffällig durchsuchen, versteckte Lebererkrankungen markieren und Ärzten helfen, bevor schwerer Schaden entsteht?
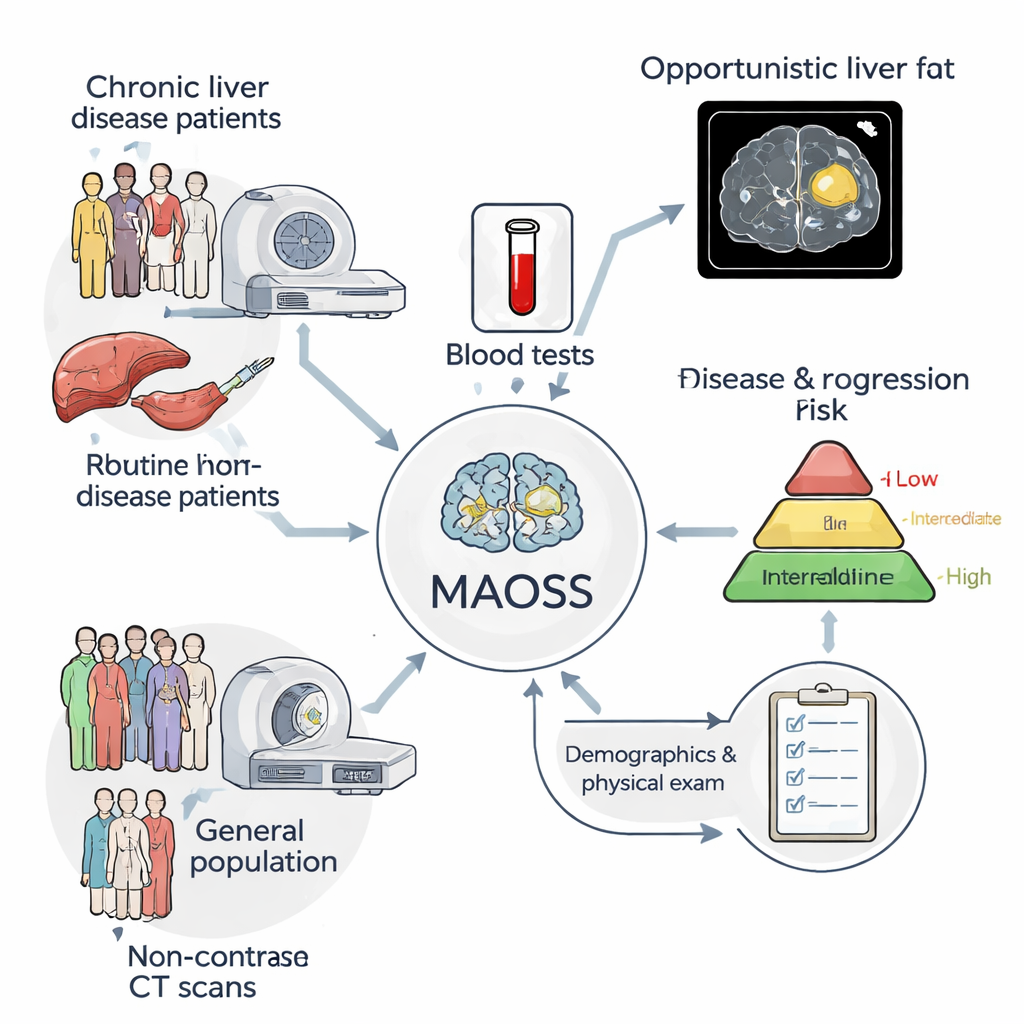
Ein neuer KI‑Assistent auf Basis realer Klinikdaten
Die Forschenden entwickelten ein multimodales KI‑System namens MAOSS (Multi‑modal AI for Opportunistic hepatic Steatosis Screening). Anstatt sich auf einen einzigen Informationstyp zu stützen, kombiniert MAOSS drei Quellen: 3D‑Nichtkontrast‑CT‑Bilder der Leber, standardmäßige Blutwerte und grundlegende klinische Angaben wie Alter und Körpergröße/-gewicht. Das Team trainierte das System an mehr als 2.000 Patientinnen und Patienten eines großen chinesischen Krankenhauses, darunter nahezu 1.000 mit unter dem Mikroskop untersuchtem Lebergewebe (die Goldstandard‑Biopsien) und über 1.100 mit detaillierten radiologischen Befunden. Diese Mischung erlaubte der KI, sowohl von den präzisesten Labels (Biopsien) als auch von den breiteren, leichter verfügbaren Berichten aus der täglichen Praxis zu lernen.
Der KI beibringen, Fett und Narben zu erkennen
MAOSS wurde so entworfen, dass es zwei zentrale Fragen für jeden CT‑Scan beantwortet: Wie viel Fett befindet sich in der Leber (Steatose) und wie weit fortgeschritten ist eventuell vorhandene Narbenbildung (Fibrose)? Dazu behandelt das Modell Krankheitsstadien als eine geordnete Leiter – von keinem über leicht und mäßig bis schwer – und lernt, jede Patientin bzw. jeden Patienten auf die passende Sprosse zu setzen. Ein spezielles „multimodales“ Design ermöglicht es dem System, flexibel mit fehlenden Informationen umzugehen; beispielsweise kann es auch dann arbeiten, wenn einige Blutwerte nicht vorliegen, und sich stärker auf die Bildgebung stützen. Die Forschenden ergänzten außerdem ein Erklärungswerkzeug auf Basis von „integrated gradients“, das die spezifischen Regionen und Dichten innerhalb des Leberbildes hervorhebt, die die Entscheidung der KI am stärksten beeinflussen, und so Klinikerinnen und Klinikern eine Heatmap verdächtiger Fettveränderungen liefert.
Wie gut MAOSS im Vergleich zu aktuellen Werkzeugen abschneidet
Bei Tests an getrennten Patientengruppen aus mehreren Krankenhäusern – darunter ein externer Kollektiv und eine Gruppe mit MRI‑basierten Leberfettmessungen – zeigte MAOSS eine hohe Genauigkeit bei der Erkennung bereits leichter Leberfettanteile, mit Flächen unter der ROC‑Kurve (AUCs) um etwa 0,90–0,93. Auch bei der Identifikation klinisch relevanter Fibrose erzielte es starke Werte, mit AUCs um 0,82–0,89. Diese Ergebnisse lagen durchgehend über denen von Modellen, die nur Bilder, nur klinische Daten oder standardmäßige ultraschallbasierte Messungen wie die transiente Elastographie nutzten. In einer Leserstudie mit 11 Radiologinnen und Radiologen fungierte MAOSS als Assistenz: Wenn die Ärztinnen und Ärzte den KI‑Score zusammen mit dem CT sahen, verbesserte sich ihre Fähigkeit, Frühstadien der Fettleber zu erkennen, deutlich – insbesondere beim Unterscheiden normaler Lebern von solchen mit subtilen Veränderungen.
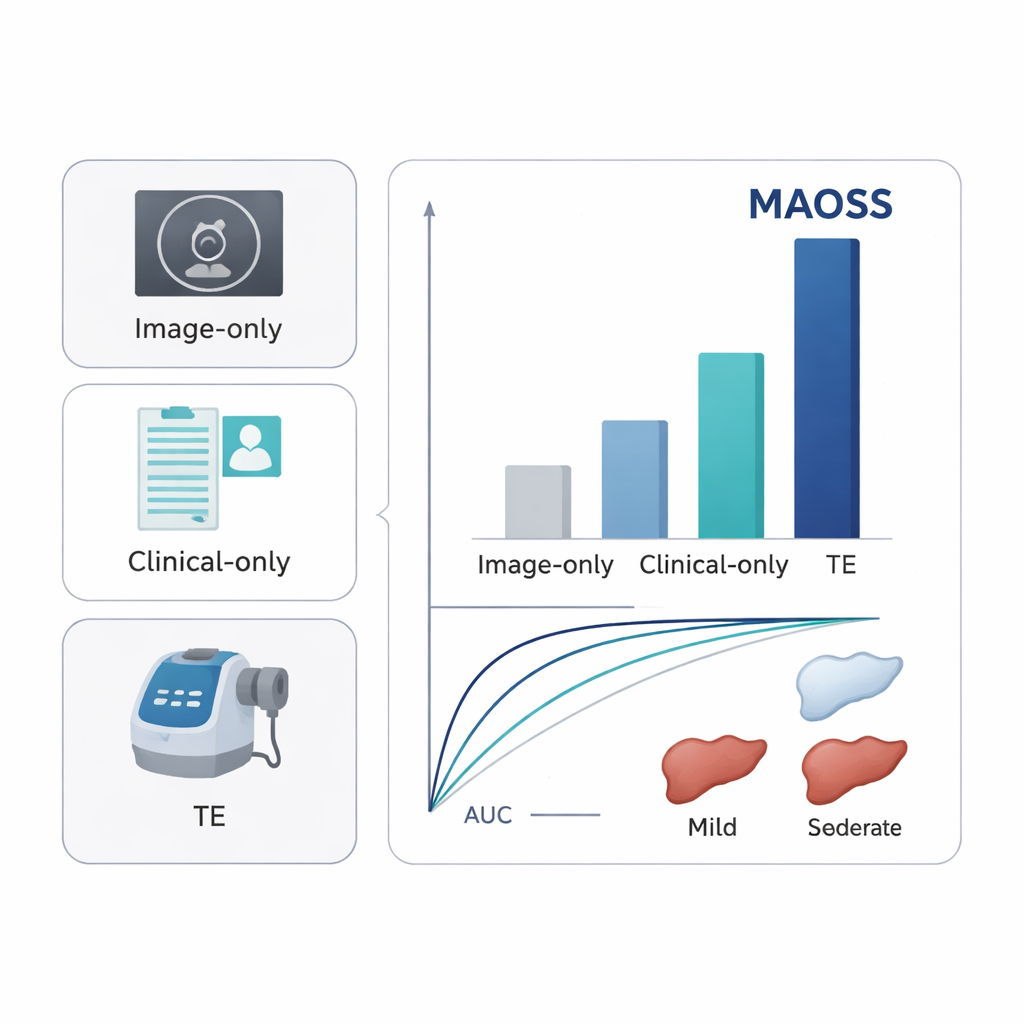
Routinescans in ein Frühwarnnetz verwandeln
Das Team fragte dann, wie MAOSS in der unordentlichen Realität der Alltagsmedizin funktionieren könnte. Sie wendeten das System auf mehr als 18.000 reale CT‑Scans aus Notaufnahmen, Stationen, Ambulanzen und Gesundheitscentern an, von denen die meisten ursprünglich aus nicht‑leberspezifischen Gründen angefordert wurden. MAOSS’ Einschätzungen von „Fettleber“ versus „keine Fettleber“ stimmten eng mit den radiologischen Berichten überein, besonders in großen Reihen von Vorsorgeuntersuchungen. Anschließend integrierten sie MAOSS in eine etablierte klinische Richtlinie, die entscheidet, welche Patientinnen und Patienten mit Fettleber an Spezialisten überwiesen werden sollten. In einer bioptisch bestätigten Kohorte von 1.192 Personen identifizierte der durch MAOSS ergänzte Weg etwa ein Drittel mehr Personen mit einem Risiko für das Fortschreiten zu Steatohepatitis oder fortgeschrittener Fibrose als der Standardansatz, der ausschließlich auf Ultraschallmessungen basiert, wobei gleichzeitig Niedrigrisiko‑Patienten sicher ausgeschlossen wurden.
Was das für Patientinnen, Patienten und die zukünftige Versorgung bedeutet
Für Laien lautet die Kernbotschaft: Dieselben CT‑Scans, die bereits aus anderen Gesundheitsgründen durchgeführt werden, könnten ohne zusätzliche Termine oder invasive Eingriffe als stilles Screening für Lebererkrankungen dienen. Indem CT‑Bilder automatisch zusammen mit routinemäßigen Blutwerten ausgewertet werden, kann MAOSS Fettleber und besorgniserregende Narbenbildung früher erfassen als traditionelle Methoden, Radiologinnen und Radiologen helfen, subtile Erkrankungen zu erkennen, die sie sonst übersehen könnten, und Patientengruppen genauer in niedriges, intermediäres und hohes Progressionsrisiko hin zu Zirrhose einteilen. Zwar weisen die Autorinnen und Autoren darauf hin, dass größere, längerfristige Studien nötig sind und die KI nicht perfekt ist, doch deuten ihre Ergebnisse darauf hin, dass multimodale KI ein wichtiges Instrument zur Verhinderung schwerer Lebererkrankungen werden könnte, bevor diese unbemerkt voranschreiten.
Zitation: Gao, Y., Li, C., Chang, W. et al. Multi-modal AI for opportunistic screening, staging and progression risk stratification of steatotic liver disease. Nat Commun 17, 1562 (2026). https://doi.org/10.1038/s41467-026-68414-3
Schlüsselwörter: Fettlebererkrankung, medizinische KI, CT‑Bildgebung, Leberfibrose, opportunistisches Screening