Clear Sky Science · de
Hierarchische Mechanismen steuern die Beseitigung von durch DNA-Schäden blockierter RNA-Polymerase II
Wenn die Gen-Kopiermaschinen auf eine Blockade stoßen
Jede Sekunde wandern Millionen winziger molekularer Maschinen, die RNA-Polymerase II genannt werden, entlang unserer DNA und kopieren Gene in RNA. Trifft die Polymerase auf beschädigte DNA – zum Beispiel durch ultraviolette (UV-)Strahlung der Sonne – kann sie ins Stocken geraten. Bleiben gestoppte Polymerasen liegen, können Zellen ihre Gene nicht mehr korrekt ablesen; das ist besonders gefährlich für Neuronen und kann zu seltenen Erkrankungen wie dem Cockayne-Syndrom führen. Diese Studie beschreibt detailliert, wie Zellen die blockierten Maschinen erkennen und entweder wieder in Gang setzen oder entfernen, bevor sie bleibenden Schaden anrichten.
Eine neue Methode, Zell-Verkehrsstaus zu beobachten
Um zu verstehen, wie Zellen blockierte Polymerasen räumen, bauten die Forschenden eine zeitaufgelöste „Verkehrskamera“ für die Transkription. Sie setzten ein Medikament ein, das bereits vorhandenen RNA-Polymerase-II-Molekülen erlaubt weiterzulaufen, aber die Initiation neuer Transkriptionsvorgänge verhindert, und erzeugten dann in jedem Zellkern einen kleinen UV-beschädigten Bereich. Indem sie einem chemischen Kennzeichen der aktiven Polymerase folgten, konnten sie beobachten, wie schnell diese aus der beschädigten Zone verschwand verglichen mit dem übrigen Genom. Parallel entwickelten sie einen Begleittest für die Gesamtmenge aktiver Polymerase in Zelllysaten, der nicht nur zeigte, wann Polymerasen die DNA verließen, sondern auch, wann sie vom zellulären Abbausystem zerstört wurden.
Die markierten, blockierten Maschinen zum Abtransport kennzeichnen
Die Gruppe konzentrierte sich auf die transkriptionsgekoppelte Reparatur, ein spezialisiertes System, das Schäden an aktiv abgelesenen Genen beseitigt. Sie nutzten ein kohärentes Set humaner Zelllinien, von denen jeweils ein anderer Reparaturfaktor fehlte. Zwei Proteine, CSB und CSA, traten als entscheidende Wächter hervor. Fehlt eines von beiden, häuft sich die Polymerase an und bleibt hartnäckig an den Schadstellen sitzen, und die Zelle versagt beim Abbau. Biochemisch konnten diese Zellen auch keine kleinen Ubiquitin-Anhängsel an einer Schlüssestelle der Polymerase anbringen. Im Gegensatz dazu räumten Zellen, denen spätere Reparaturproteine fehlten – also diejenigen, die die beschädigte DNA herausschneiden und ersetzen – die Polymerase weiterhin normal. Das zeigt, dass die initiale Ubiquitin-Markierung der blockierten Polymerase der kritische Auslöser für die Entscheidung über ihr Schicksal ist.
Zwei Aufräumteams: eines schnell, eines als Backup
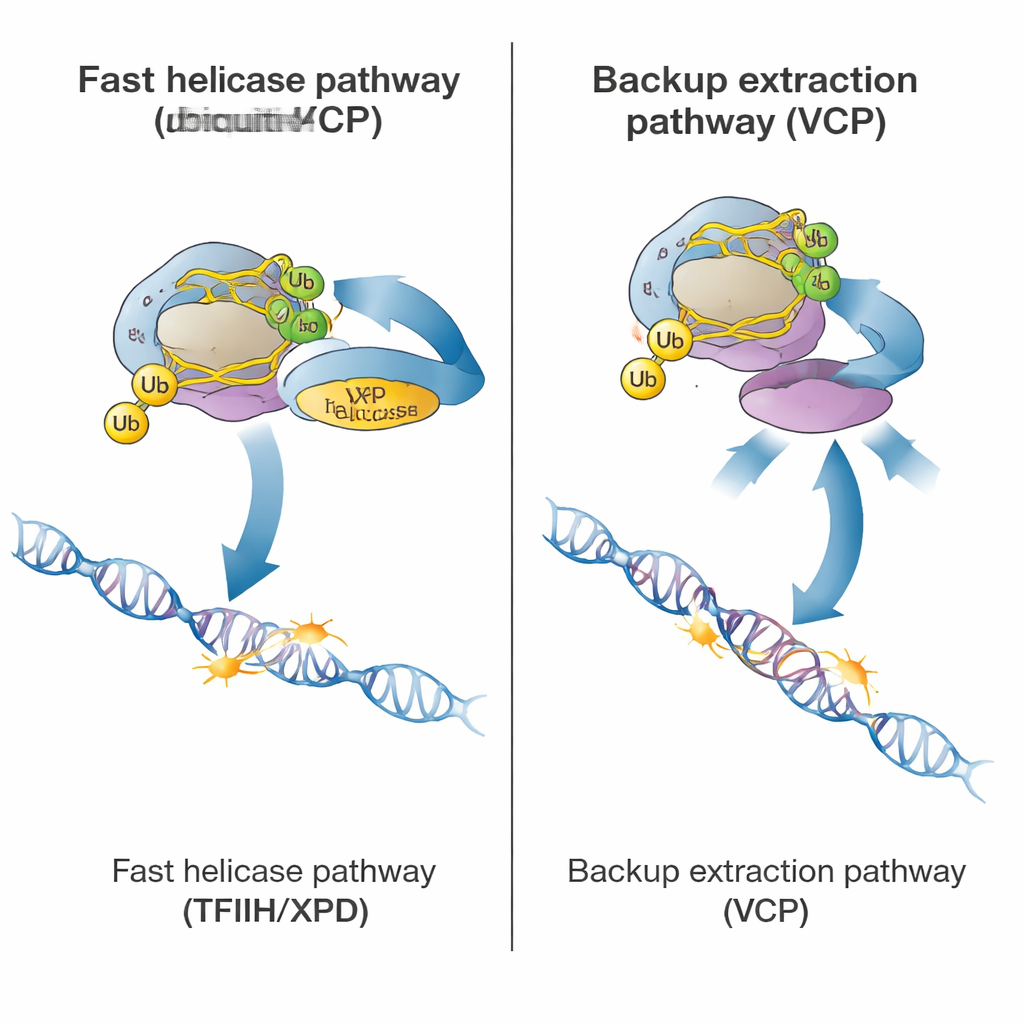
Ist die Polymerase markiert, kann die Zelle zwischen zwei Wegen zur Beseitigung wählen. Die primäre, schnelle Route beruht auf einem großen Reparaturkomplex namens TFIIH und insbesondere auf seiner XPD-Helikase-Untereinheit, die Energie nutzt, um DNA aufzuwinden. Helferproteine, darunter ELOF1, UVSSA und STK19, bringen TFIIH zur blockierten Polymerase und positionieren XPD auf der DNA direkt vor ihr. Mit neuen Tests in Patienten-Zellen, die eine helikase-inaktive XPD-Mutation tragen, zeigten die Autorinnen und Autoren, dass bei fehlender Entwindungsfähigkeit von XPD die Räumung der Polymerase drastisch verzögert ist, obwohl der Rest der Reparaturmaschinerie vorhanden ist. Das deutet darauf hin, dass die mechanische Zugwirkung von XPD normalerweise die Polymerase sozusagen „abrüttelt“, damit Reparaturenzyme die Schadstelle erreichen können.
Ein langsamer, aber essentieller Plan B
Die Studie zeigte außerdem einen langsameren Notfallweg zur Entfernung blockierter Polymerasen. Dieser Pfad ist abhängig von VCP (auch p97 genannt), einem Protein, das Ubiquitin-Marken erkennt und Proteine gewaltsam aus dem Chromatin herausziehen kann. In gesunden Zellen mit funktionsfähigem TFIIH hatte die Hemmung von VCP nur einen geringen Effekt. In Zellen, in denen TFIIH fehlte, falsch positioniert war oder helikase-inaktiv war, wurde die Räumung der Polymerase jedoch nahezu vollständig VCP-abhängig. Unter diesen Bedingungen konnte VCP die markierte Polymerase weiterhin von der DNA entfernen, selbst wenn die normale Reparatur nicht fortschreiten konnte. Entscheidend ist, dass dieser Backup-Weg dennoch einige Ubiquitin-Markierungen erforderte, was erklärt, warum Zellen ohne CSB oder CSA – und damit ohne Ubiquitin-Kennzeichen – sowohl den Haupt- als auch den Backup-Weg nicht nutzen können.
Warum das für Gesundheit und Krankheit wichtig ist
In der Gesamtschau skizziert die Arbeit ein hierarchisches Sicherheitsprogramm, das Zellen einsetzen, wenn RNA-Polymerase II auf DNA-Schäden trifft. Zuerst markieren CSB und CSA die blockierte Maschine mit Ubiquitin. Funktioniert alles richtig, lösen TFIIH und seine XPD-Helikase die Polymerase schnell, sodass die Schadstelle herausgeschnitten und repariert werden kann. Kann TFIIH nicht arbeiten, springt VCP ein, um die Polymerase zu extrahieren und zum Abbau zu schicken, sodass sie die Genexpression nicht verstopft, auch wenn die DNA-Schädigung bestehen bleibt. Dieses Modell erklärt, warum vererbte Defekte in CSB oder CSA besonders schwere neurologische Probleme verursachen: Ohne Ubiquitin-Markierung verlieren Zellen sowohl den primären reparaturgesteuerten Weg als auch den Backup-Extraktionsweg, sodass blockierte Polymerasen auf beschädigten Genen kleben bleiben und die Transkription chronisch blockiert ist.
Zitation: van der Meer, P.J., Yakoub, G., Tsukada, K. et al. Hierarchical mechanisms control the clearance of DNA lesion–stalled RNA polymerase II. Nat Commun 17, 1647 (2026). https://doi.org/10.1038/s41467-026-68413-4
Schlüsselwörter: transkriptionsgekoppelte DNA-Reparatur, RNA-Polymerase II, UV-induzierte DNA-Schäden, Proteinubiquitinierung, Cockayne-Syndrom