Clear Sky Science · de
In situ-Visualisierung der phänotypischen Heterogenität und Einzelzellmorphologie von Clostridioides difficile während einer Darminfektion
Warum Darmkeime nicht alle gleich reagieren
Clostridioides difficile, oft C. diff genannt, ist ein berüchtigter Krankenhauskeim, der nach einer durch Antibiotika gestörten Darmflora schwere, mitunter lebensbedrohliche Durchfälle auslösen kann. Doch selbst wenn diese Bakterien genetisch identisch sind und dieselbe Umgebung teilen, können einzelne Zellen sehr unterschiedlich agieren. Diese Studie zeigt in beispielloser Detailtiefe, wie einzelne C. diff-Zellen die Toxinproduktion an- oder ausschalten und sich während einer Infektion im Darminneren sogar in ihrer Form verändern — Hinweise darauf, warum die Erkrankung so hartnäckig ist und schwer zu behandeln sein kann.
Ein gefährlichen Darm‑Eindringling in Echtzeit verfolgen
Um zu verstehen, wie einzelne C. diff-Zellen im Körper handeln, brauchten die Forschenden eine Methode, sie innerhalb der dichten und vielfältigen Darmgemeinschaft sichtbar zu machen. Sie konstruierten C. diff-Stämme, die unter dem Mikroskop dauerhaft in kräftigen Farben leuchten, mithilfe spezieller fluoreszenter Proteine, die das Wachstum oder die Krankheitsfähigkeit der Bakterien nicht stören. Indem sie antibiotikabehandelte Mäuse mit diesen leuchtenden Stämmen infizierten und anschließend den Dickdarm schnitten und anfärbten, konnten sie die exakten Orte und das Verhalten von Tausenden einzelner Bakterienzellen im intakten Darmgewebe bestimmen. 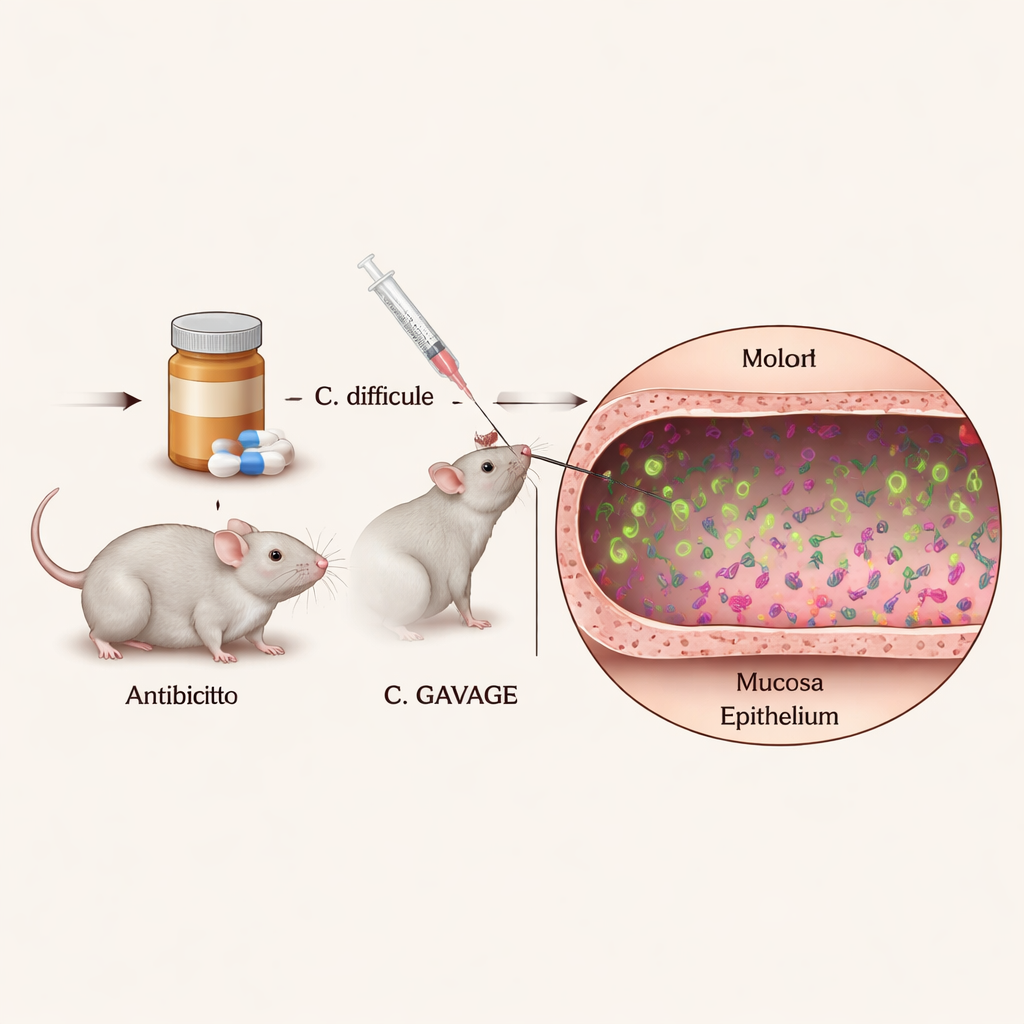
Wo die Bakterien im Dickdarm leben
Die Bilder zeigten, dass die meisten C. diff-Zellen im Zentrum des Darminhalts leben, dem Lumen, und bestätigten damit, dass der Erreger vorwiegend ein frei im Lumen schwebender („luminaler“) Krankheitserreger ist. Eine auffällige Minderheit der Zellen tauchte jedoch konsistent in der Nähe der Schleimschicht und direkt neben der Epitheloberfläche auf — der dünnen Zellschicht, die den Dickdarm auskleidet und als Barriere zur Außenwelt dient. Diese eng anliegenden Unterpopulation war in konventionellen Mäusen mit normalem Immunsystem zuvor nicht klar zu sehen. Wichtig ist, dass die eingebauten fluoreszenten Marker die Bakterien in den Tieren nicht merklich schwächten, sodass die Aufnahmen wahrscheinlich widerspiegeln, wie C. diff bei einer realistischen Infektion agiert.
Wer stellt Toxin her, und wo?
Die Gruppe ergänzte die Beobachtungen durch ein zweites fluoreszierendes Signal, das nur dann anschaltet, wenn C. diff seine Toxin-Gene aktiviert. Toxine sind die schädigenden Proteine, die die Darmschleimhaut verletzen und die Krankheitssymptome antreiben; sie werden auch in Stuhltests gemessen, um eine Infektion zu diagnostizieren. Überraschenderweise produzierten nicht alle Bakterien gleichzeitig Toxine. Stattdessen leuchtete zu jedem Zeitpunkt nur ein Bruchteil der Zellen als „Toxin‑ON“ auf, sowohl früh als auch spät in der Infektion. Dieser Anteil war bei einem Mutantenstamm höher, der genetisch auf Überproduktion von Toxin eingestellt ist, doch selbst dort beteiligte sich nicht jede Zelle. Ebenso bemerkenswert: Die Position einer Zelle — im Lumen schwimmend, im Schleim sitzend oder das Epithel berührend — veränderte nur wenig die Häufigkeit der Toxinproduktion oder die Stärke der Genaktivierung. 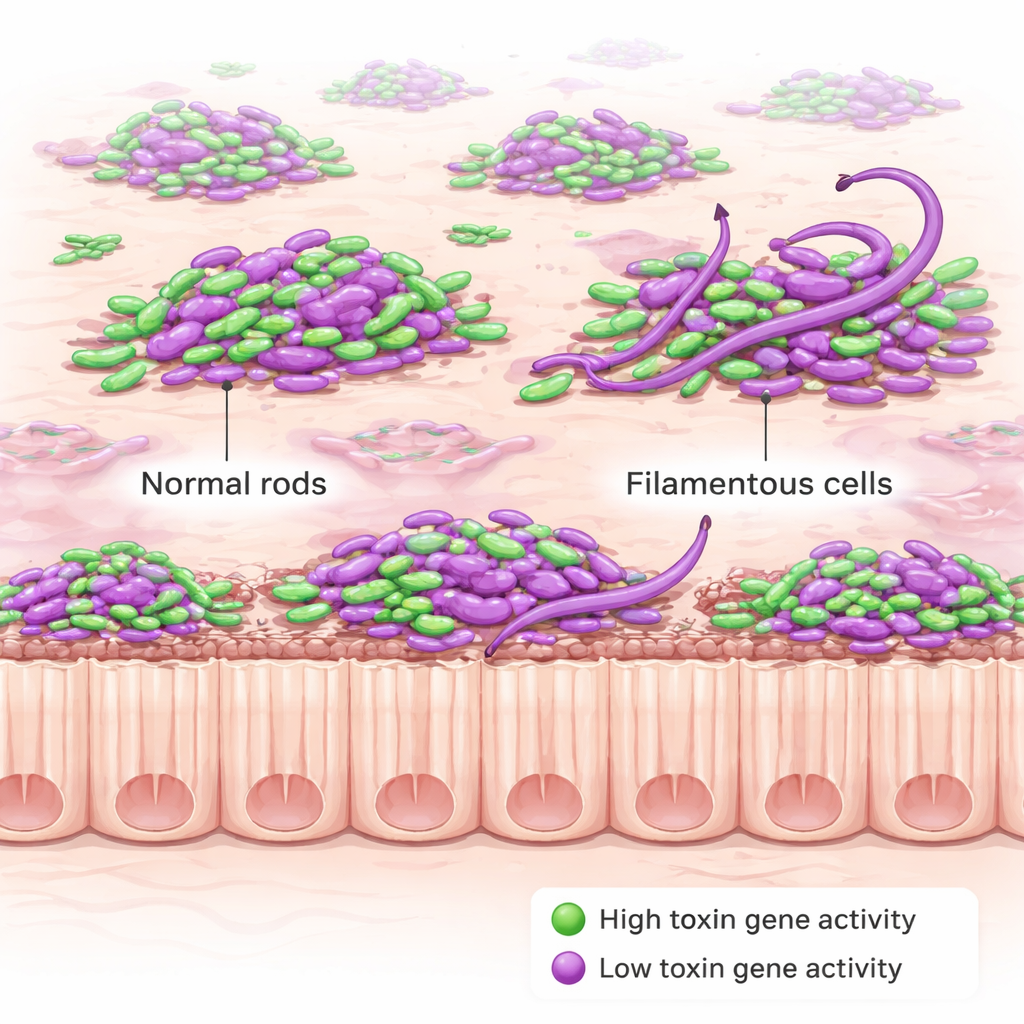
Formwandelnde Zellen unter Stress
Während sie die Toxinproduktion kartierten, stießen die Forschenden auf ein unerwartetes Verhalten. In Mäusen, die mit dem toxinüberproduzierenden Mutanten infiziert waren, wurden viele C. diff-Zellen in der akuten Krankheitsphase ungewöhnlich langgezogene, gebogene Filamente — teils mehr als zehnmal so lang wie normale kurze Stäbchen. Diese „schnurartige“ Morphologie trat vorwiegend während früher, schwerer Infektionen auf und ließ später nach; im Laborbrühe-Wachstum des Stamms zeigte sie sich nicht. Das deutet darauf hin, dass die stressigen Bedingungen im entzündeten Darm — und nicht allein die genetische Veränderung — diesen dramatischen Umbau auslösen. Folgeexperimente zeigten, dass der Verlust eines Regulationsproteins namens RstA, das sowohl Toxin-Gene als auch andere Stressantworten steuert, diese Filamentbildung begünstigt.
Was das für C. diff-Erkrankungen bedeutet
Für Nicht‑Fachleute ist die Kernbotschaft, dass sich selbst ein einzelner C. diff-Stamm wie eine geteilte Arbeitsgruppe verhält. Manche Zellen tragen die Energie- und Produktionskosten, um Toxin zu bilden und den Darm zu schädigen, wodurch Nährstoffe freigesetzt werden, die toxinfreiere Nachbarn nutzen können. Diese gemeinsame „Arbeitsteilung“ kann der Infektion helfen, anzudauern und wieder aufzublühen, weil nicht jede Zelle gleichermaßen anfällig für Behandlungen ist, die auf Toxin oder schnell wachsende Bakterien zielen. Das neu entwickelte leuchtende Reportersystem bietet Wissenschaftlern einen mächtigen Weg, Zelle für Zelle zu beobachten, wie C. diff und verwandte Darmmikroben sich räumlich und zeitlich im Körper anpassen. Diese Einblicke könnten schließlich Therapien anleiten, die nicht nur auf das Abtöten von Bakterien zielen, sondern darauf, die schädlichen Rollen bestimmter Unterpopulationen zu stören, die Krankheit und Rückfälle antreiben.
Zitation: DiBenedetto, N.V., Donnelly-Morell, M.L., Kumamoto, C.A. et al. In situ visualization of Clostridioides difficile phenotypic heterogeneity and single-cell morphology during gut infection. Nat Commun 17, 1716 (2026). https://doi.org/10.1038/s41467-026-68411-6
Schlüsselwörter: Clostridioides difficile, Darmmikrobiom, bakterielle Toxine, phänotypische Heterogenität, fluoreszenzbildgebung