Clear Sky Science · de
Ein Nanosystem, das den Tissue Inhibitor of Metalloproteinase‑1 für eine kontinuierliche spatiotemporale Therapie der idiopathischen Lungenfibrose anvisiert
Warum hartnäckige Lungenvernarbung wichtig ist
Idiopathische Lungenfibrose (IPF) ist eine unaufhaltsame Lungenerkrankung, bei der normales, schwammiges Lungengewebe allmählich durch steifes Narbengewebe ersetzt wird. Menschen mit IPF bekommen bei alltäglichen Aktivitäten Atemnot, und die meisten überleben nur wenige Jahre nach der Diagnose. Die heutigen Medikamente können die Krankheit bei einigen Patienten verlangsamen, heilen die vorhandenen Narben aber selten und verursachen oft Nebenwirkungen. Diese Studie untersucht eine intelligente, inhaliere „Nano‑Therapie“, die nicht nur das Fortschreiten der IPF verlangsamen soll, sondern aktiv Narbengewebe abbaut und die Selbstreparatur der Lunge fördert.
Das Problem: klebrige Narben und chemischer Stress
Bei IPF füllen sich die Räume, in denen Sauerstoff normalerweise ins Blut übergeht, mit überschüssigen Proteinen wie Kollagen, wodurch flexible Lungenbläschen zu starren Bereichen werden. Die Autoren konzentrierten sich auf ein Protein namens TIMP‑1, das wie eine Bremse auf natürliche Enzyme wirkt, die normalerweise überschüssiges Kollagen abbauen. Anhand von Lungenproben von Patienten und von Mäusen mit induzierter Lungenvernarbung stellten sie fest, dass die TIMP‑1‑Spiegel mehrere Male höher waren als in gesunden Lungen und mit der Kollagenansammlung anstiegen. Gleichzeitig zeigten beschädigte Lungen stark erhöhte Werte reaktiver Sauerstoffspezies (ROS) — chemische „Funken“, die Zellen schädigen — sowie einen Verlust wichtiger Marker gesunder Zellen der Lungenbläschen‑Auskleidung. Zusammen deuteten diese Befunde auf einen Teufelskreis hin: Zu viel TIMP‑1 verlangsamt den Narbenabbau, während oxidative Belastung die Lungenstruktur weiter schädigt.
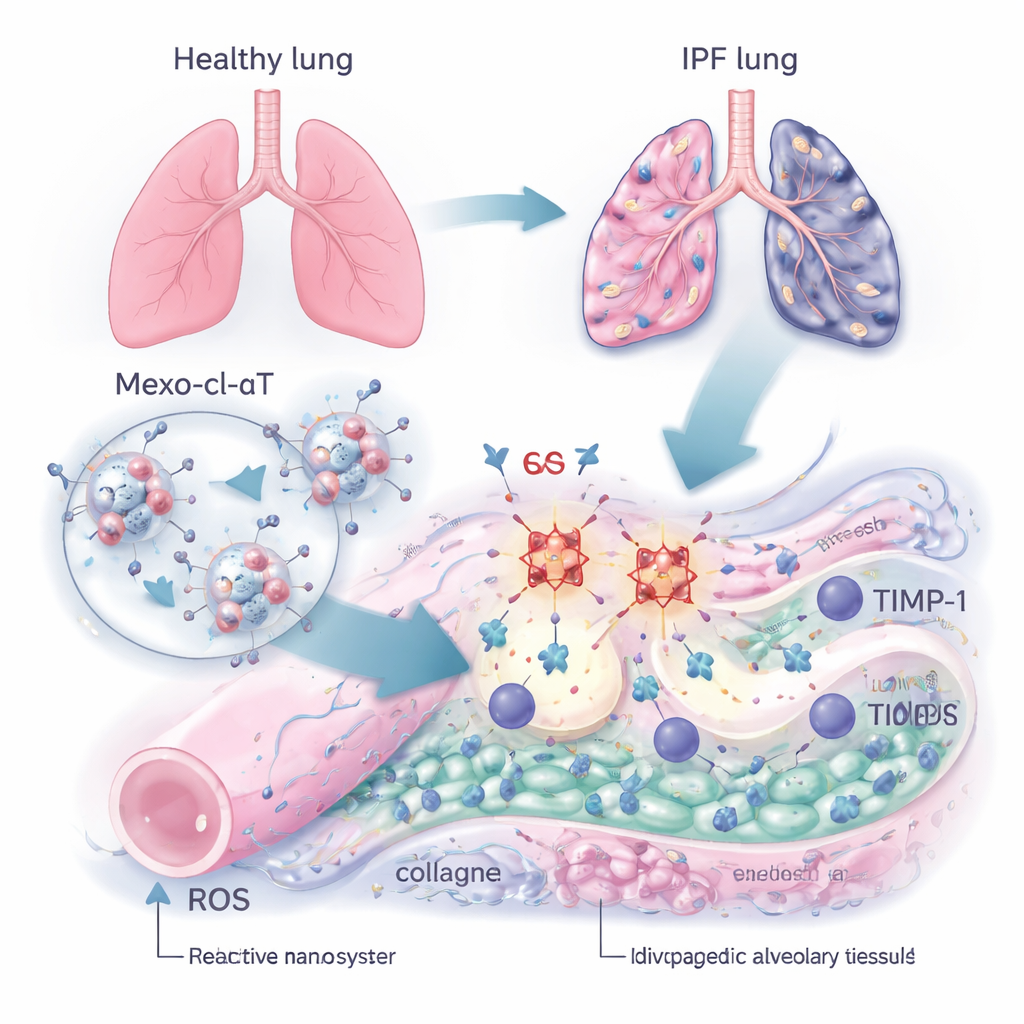
Ein intelligenter Transporter: winzige Reparaturpakete
Um diesen Kreislauf zu durchbrechen, entwickelten die Forscher eine nanoskalige Therapie namens Mexo‑cl‑aT. Sie begannen mit Exosomen — natürlichen, bläschenartigen Partikeln, die von Stammzellen freigesetzt werden und dafür bekannt sind, geschädigte Gewebe anzusteuern und die Heilung zu unterstützen. Auf der Oberfläche dieser Exosomen befestigten sie Antikörper, die spezifisch an TIMP‑1 binden. Die Verbindung zwischen Exosom und Antikörper wurde mithilfe eines speziellen chemischen Linkers hergestellt, der durch ROS gespalten werden kann. Mit anderen Worten: Die harsche chemische Umgebung einer vernarbten Lunge dient als Signal: Wenn das Exosom eine geschädigte Region mit hohen ROS‑Werten erreicht, bricht der Linker, nimmt einen Teil der ROS auf und setzt den Antikörper genau dort frei, wo TIMP‑1 konzentriert ist, während das Exosom selbst weiterhin die Gewebereparatur fördert.
Wie sich das Nanosystem verhält und wirkt
In Zellstudien zeigten die Forschenden, dass Mexo‑cl‑aT in Flüssigkeit stabil bleibt, die Antikörper aber schnell freisetzt, wenn es Mengen an Wasserstoffperoxid ausgesetzt wird, wie sie in erkrankten Lungen vorkommen. Gleichzeitig senkt es die vorhandene Peroxidmenge deutlich und bestätigt damit seine ROS‑fangende Funktion. In narbenähnlichen Zellmodellen verringerten die freigesetzten Antikörper die TIMP‑1‑Spiegel und aktivierten Enzyme, die Kollagen abbauen, während die Exosomkomponente den Zelltod verringerte, das Zellwachstum förderte und die Wundverschlussrate in sowohl Lungen‑ als auch Blutgefäßzellen beschleunigte. Im Vergleich zu Versionen mit nicht spaltbarem Linker entfernte das ROS‑reaktive Design mehr Kollagen und reduzierte die chemische Belastung effektiver, was die Bedeutung der kontrollierten Freisetzung unterstreicht.
Test in einem schweren Modell der Lungenvernarbung
Das Team testete die Therapie anschließend an Mäusen mit fortgeschrittener Lungenfibrose, ausgelöst durch das Medikament Bleomycin — ein Modell, das gewählt wurde, um die Spätphase der IPF nachzuahmen. Eine einzige inhaliere Dosis Mexo‑cl‑aT blieb mehrere Tage in der Lunge und hielt mehr Antikörper zurück als eine einfache Mischung ihrer Einzelbestandteile. Behandelte Lungen wirkten mit bloßem Auge und unter dem Mikroskop gesünder: Luftwege öffneten sich wieder, die Narbenschicht wurde dünner und der gesamte Kollagengehalt kehrte nahezu zum Normalwert zurück. Marker aktivierter narbenbildender Zellen sanken, während Proteine, die mit gesunden Lungenbläschen‑ und Blutgefäßauskleidungszellen assoziiert sind, zunahmen. Chemische Messungen zeigten, dass die Behandlung TIMP‑1‑Werte deutlich senkte, das Gleichgewicht kollagenabbauender Enzyme wiederherstellte und etwa drei Viertel des überschüssigen ROS entfernte. Wichtig: Entzündungswerte gingen zurück, und Bluttests sowie Organuntersuchungen zeigten keine offensichtliche Toxizität.
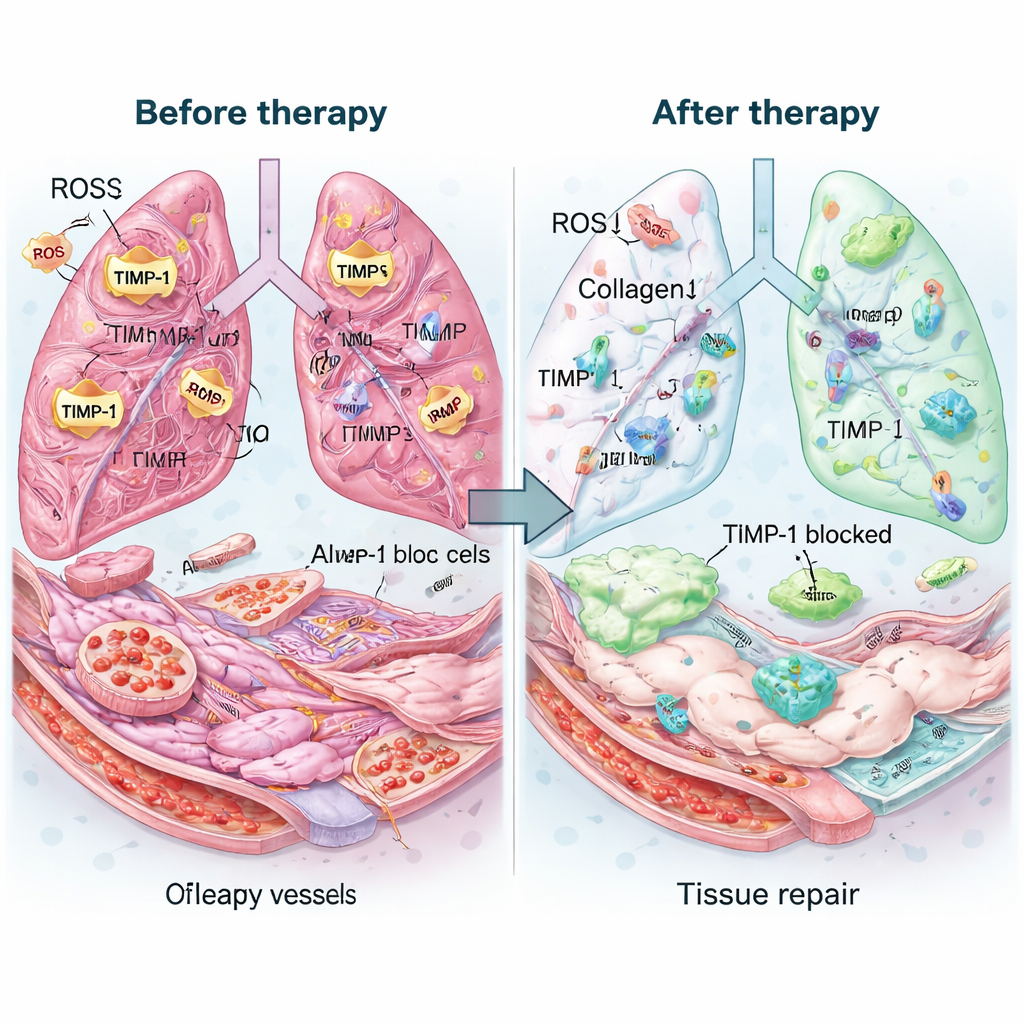
Was das für Patientinnen und Patienten bedeuten könnte
Für Menschen mit IPF bietet diese Arbeit noch keine sofortige Heilung, doch sie stellt eine vielversprechende Strategie vor. Anstatt nur neuen Schaden zu verlangsamen, zielt das Mexo‑cl‑aT‑Nanosystem darauf ab, vorhandene Narben aktiv abzubauen, schädlichen chemischen Stress zu dämpfen und den Wiederaufbau empfindlichen Lungengewebes zu unterstützen — alles in einer zielgerichteten, inhalierten Form, die die Behandlung dorthin konzentriert, wo sie am dringendsten gebraucht wird. Während Herausforderungen wie die großtechnische Exosomproduktion und klinische Prüfungen am Menschen noch zu lösen sind, legt die Studie nahe, dass präzise Nano‑Therapien, die an die kranke Umgebung angepasst sind, eines Tages die Behandlung hartnäckiger Lungenvernarbungen und möglicherweise anderer fibrotischer Erkrankungen verändern könnten.
Zitation: Li, C., Lu, G., Chen, H. et al. A nanosystem targeting tissue inhibitor of metalloproteinase-1 for continuous spatiotemporal idiopathic pulmonary fibrosis therapy. Nat Commun 17, 1694 (2026). https://doi.org/10.1038/s41467-026-68398-0
Schlüsselwörter: idiopathische Lungenfibrose, Lungenvernarbung, Nanomedizin, Exosomtherapie, TIMP‑1