Clear Sky Science · de
Geschädigte Epithelzell‑Zustände beeinflussen das Überleben von Nierentransplantaten nach T‑Zell‑vermittelter Abstoßung
Warum diese Nierenforschung für Patient:innen wichtig ist
Nierentransplantationen können lebensrettend sein, doch viele Transplantate versagen Jahre nach der Operation, selbst wenn Ärzt:innen die Immunreaktion, bekannt als T‑Zell‑vermittelte Abstoßung, scheinbar im Griff haben. Diese Studie stellt eine einfache, aber entscheidende Frage: Wenn die Immunreaktion unter dem Mikroskop „behandelt“ aussieht, warum verschleißen einige transplantierte Nieren trotzdem frühzeitig? Durch die Untersuchung einzelner Zellen in transplantierten Nieren von Mäusen und Menschen entdeckten die Forschenden eine versteckte Schicht von Schäden in den filtrierenden Tubuli der Niere, die erklärt, welche Transplantate überleben und welche nicht.
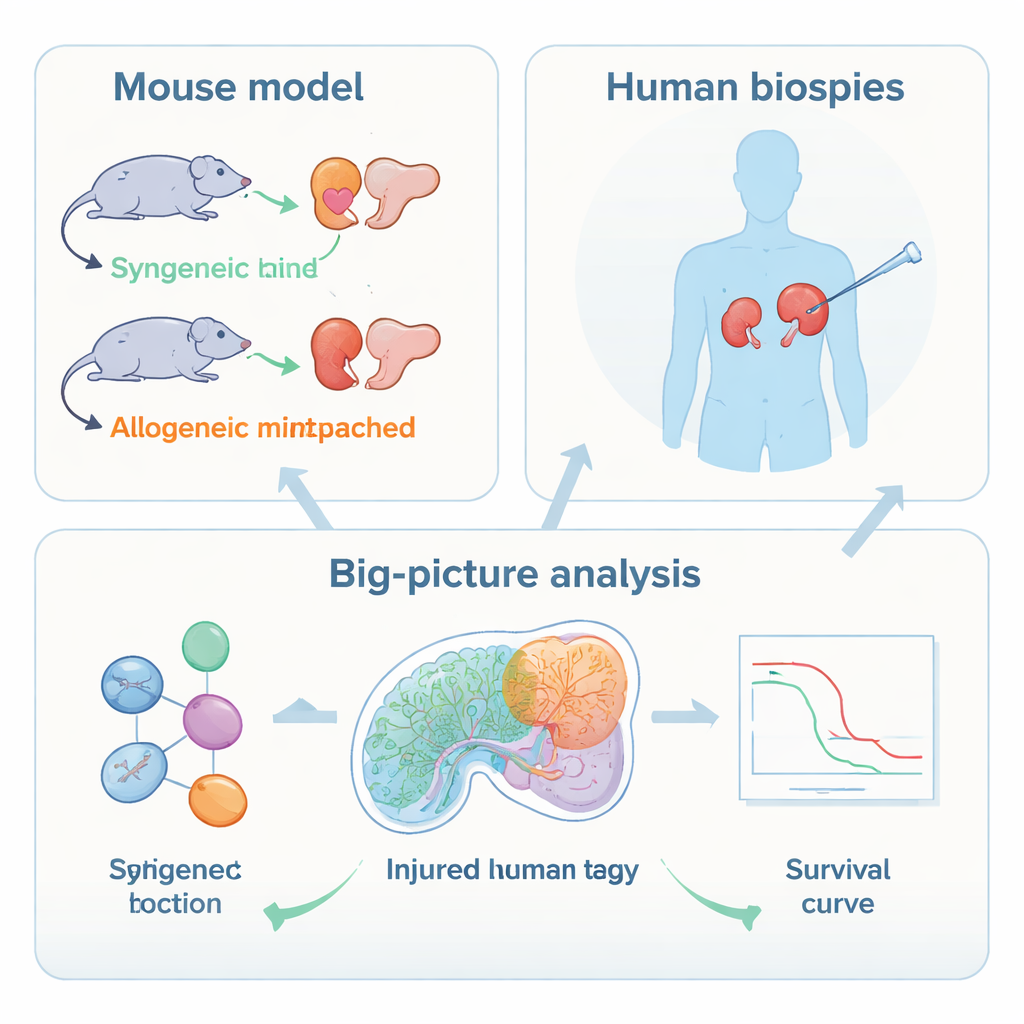
Blick über die klassischen Abstoßungszeichen hinaus
Ärzt:innen diagnostizieren die T‑Zell‑vermittelte Abstoßung meist, indem sie sehen, wie weiße Blutkörperchen in die Niere eindringen und die kleinen Tubuli angreifen, die den Urin verarbeiten. Starke Anti‑Abstoßungsmedikamente können diese Immunzellen oft verdrängen und die Biopsie besser erscheinen lassen. Dennoch haben Patient:innen mit dieser Form der Abstoßung weiterhin ein hohes Risiko für Transplantatverlust. Frühere groß angelegte Genstudien deuteten darauf hin, dass Signale von Gewebeschädigung innerhalb der Nierenzellen den Ausgang besser vorhersagen als die bloße Anzahl der Immunzellen. Die Autor:innen wollten diese Schädigungssignale auf Einzelzell‑Ebene definieren und prüfen, wie eng sie mit dem langfristigen Transplantatüberleben verbunden sind.
Abstoßung Zelle für Zelle auseinandernehmen
Das Team nutzte zunächst ein kontrolliertes Mausmodell, in dem Nieren entweder zwischen genetisch identischen Mäusen oder zwischen nicht übereinstimmenden Stämmen transplantiert wurden, um eine Abstoßung auszulösen. Anschließend setzten sie Single‑Nucleus‑RNA‑Sequencing ein, das die Aktivität tausender Gene in einzelnen Zellen erfasst, sowie räumliche Transkriptomik, die zeigt, wo diese Zellen in einer Gewebeschnittprobe liegen. Diese Werkzeuge zeigten, dass während der Abstoßung die stärksten molekularen Veränderungen nicht in den Immunzellen, sondern in den epithelialen Zellen der Niere auftreten, die die proximalen Tubuli und einen Abschnitt namens dicker aufsteigender Ast (thick ascending limb) auskleiden. In diesen Bereichen schalteten die Zellen Genprogramme für Schädigung und Stress, entzündliche Signale und Marker eines primitiveren, weniger spezialisierten Zustands an, während Transportfunktionen für eine gesunde Filtration heruntergefahren wurden.
Versteckte Nester stark geschädigter Tubuluszellen
Durch das Clustern von Zellen mit ähnlicher Genaktivität entdeckten die Forschenden mehrere unterschiedliche „Schädigungszustände“ unter Tubuluszellen in den Mäusenieren. Einige spiegelten frühe Stressantworten wider, andere stellten schwer geschädigte, stark veränderte Zellen dar, die ihre normale Identität verloren hatten und viele entzündliche und narbenbildende Moleküle produzierten. Die räumliche Kartierung zeigte, dass sich diese Zellzustände nicht gleichmäßig verteilten: Bestimmte schwere Schädigungszustände bildeten fleckenhafte Nester in der Nierenrinde und dem äußeren Mark und lagen in komplexen Nachbarschaften mit T‑Zellen, Makrophagen und Fibroblasten. Dagegen waren einige geschädigte Zellen in tieferen Regionen überraschend isoliert von Immunzellen, was auf unterschiedliche Entstehungs‑ und Persistenzweisen der Schäden hindeutet.
Abgleich der Maus‑Zustände mit menschlichen Transplantaten
Die Autor:innen prüften anschließend, ob ähnliche Zellzustände auch beim Menschen vorkommen. Sie analysierten Biopsien von menschlichen Nierentransplantaten mit aktiver T‑Zell‑vermittelter Abstoßung und von stabilen Transplantaten. Die Einzelzell‑Daten zeigten erneut geschädigte proximalen Tubuluszellen und Zellen des dicken aufsteigenden Astes, deren Genmuster den schwersten verletzten Maus‑Zuständen sehr ähnlich waren. Mit diesen humanen Signaturen „dekodierte“ das Team tausende ältere Bulk‑Biopsie‑Expressionsprofile und fand, dass schwere Tubulus‑Schädigungszustände bei T‑Zell‑vermittelter Abstoßung und gemischter Abstoßung häufiger waren als bei reiner Antikörper‑vermittelter Abstoßung oder keiner Abstoßung. Wichtig war auch, dass sie kompakte Gen‑Sätze für jeden Schädigungszustand entwickelten und diese in einer großen Kohorte mit detaillierter Nachverfolgung bewerteten.
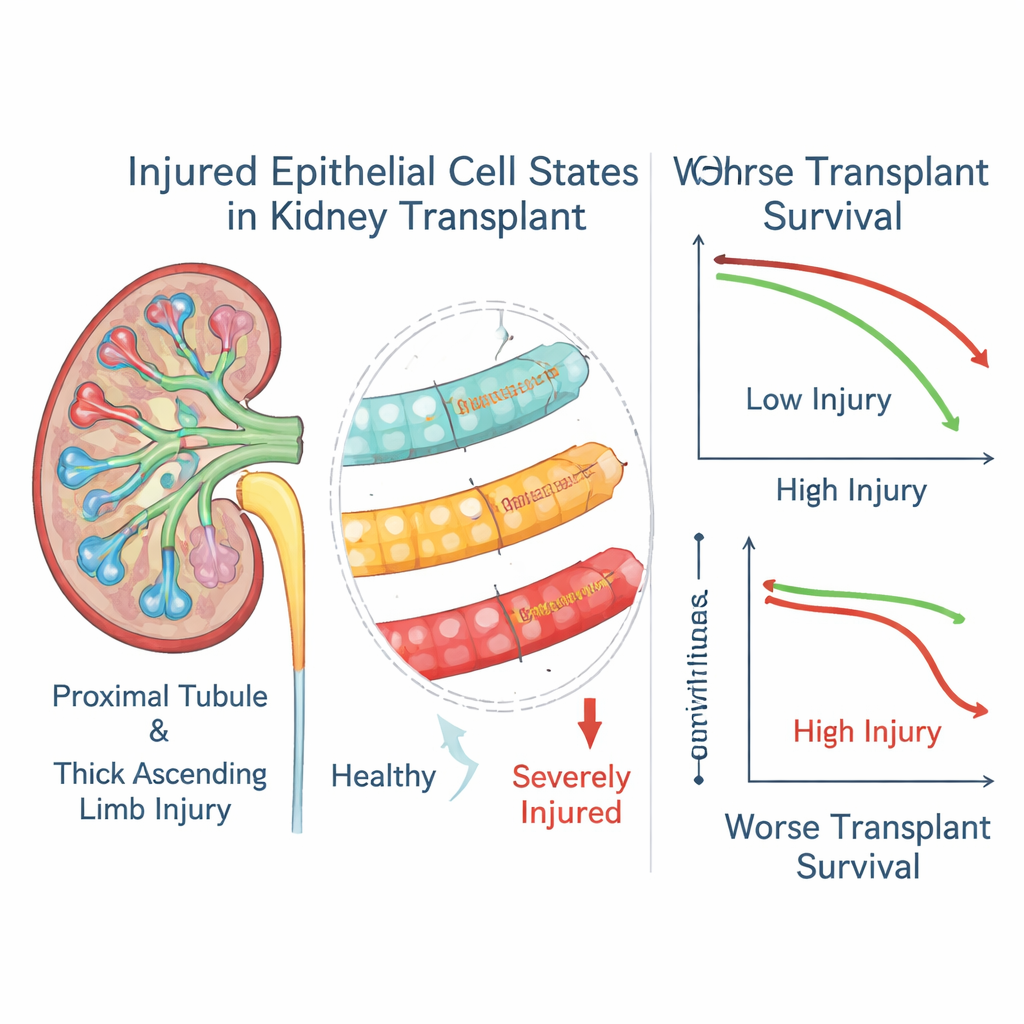
Geschädigte Tubuluszellen als Prädiktoren für das Transplantatschicksal
Als die Autor:innen diese Genscores mit Dreijahres‑Ergebnissen von über tausend Transplantatempfänger:innen verknüpften, zeigte sich ein klares Muster. Hohe Werte von Markern für die schwersten geschädigten epithelialen Zustände sowohl in den proximalen Tubuli als auch im dicken aufsteigenden Ast standen in starkem Zusammenhang mit einem höheren Risiko für Transplantatverlust, selbst bei Patient:innen, deren Biopsien ansonsten als behandelte Abstoßung klassifiziert waren. Ein milderer Tubulus‑Schädigungszustand zeigte den umgekehrten Trend und war mit besserem Überleben verbunden, was darauf hindeutet, dass er ein erfolgreicheres Reparaturprogramm repräsentieren könnte. In einer Untergruppe von Patient:innen mit wiederholten Biopsien blieben die „schweren Schädigungs“‑Scores oft lange Zeit erhöht, nachdem die Abstoßungsphase scheinbar abgeklungen war, was darauf hindeutet, dass diese veränderten Zellen anhaltend vorhanden bleiben und den Krankheitsverlauf weiter prägen können.
Was das für die Transplantationsversorgung bedeutet
Für nicht‑Fachleute lautet die zentrale Botschaft: Nicht jeder Schaden in einer abgestoßenen Niere stammt direkt von Immunzellen, und nicht jede Verletzung verschwindet, wenn der Immunangriff sich beruhigt. Die Studie zeigt, dass hartnäckige Nester schwer geschädigter Tubuluszellen als Frühwarnsystem für zukünftigen Transplantatverlust dienen. Langfristig könnten einfache Tests auf Basis dieser Schädigungs‑Gen‑Signaturen — möglicherweise sogar mit Zellen, die im Urin ausgeschieden werden — Ärzt:innen helfen, Hochrisiko‑Patient:innen zu identifizieren, Therapien anzupassen und zu überwachen, ob die Nieren tatsächlich genesen. Die Arbeit weist außerdem auf diese geschädigten epithelialen Zellen selbst als potenzielle Ziele für neue Therapien hin, die transplantierte Nieren über die übliche Immunsuppression hinaus schützen könnten.
Zitation: Pfefferkorn, A.M., Jahn, L., Gauthier, P.T. et al. Injured epithelial cell states impact kidney allograft survival after T-cell-mediated rejection. Nat Commun 17, 1060 (2026). https://doi.org/10.1038/s41467-026-68397-1
Schlüsselwörter: Nierentransplantations‑Abstoßung, Schädigung von Tubuluszellen, Einzelzellsequenzierung, Transplantat‑Überleben, Epithelzell‑Zustände