Clear Sky Science · de
Gewebespezifische Modellierung des Drosophila‑Stoffwechsels identifiziert durch hochzuckerhaltige Ernährung verursachte metabolische Dysregulation in Muskel auf Reaktions‑ und Pfadebene
Warum diese Fliegenstudie für die menschliche Gesundheit wichtig ist
Zuviel Zucker in unserer Ernährung kann die Fähigkeit des Körpers, Treibstoff zu verwalten, überlasten und langfristig zur Entstehung von Typ‑2‑Diabetes beitragen. Diese Studie nutzt Fruchtfliegen, um mit bemerkenswerter Detailtiefe zu zeigen, wie verschiedene Gewebe den Stoffwechsel handhaben und wie eine hochzuckerhaltige Ernährung die Muskel‑Funktion stört. Da Fliegen viele Stoffwechselgene und Organsysteme mit Menschen teilen, tragen diese Erkenntnisse dazu bei zu erklären, was in unseren eigenen Muskeln bei langfristiger Zuckerüberladung schiefgehen kann.
Stoffwechsel Gewebe für Gewebe kartieren
Unser Körper, wie auch der der Fruchtfliege, besteht aus Geweben mit sehr unterschiedlichen metabolischen Aufgaben: Muskel verbrennt Treibstoff, Fett speichert ihn, der Darm verarbeitet Nahrung und so weiter. Anstatt jedes Enzym direkt zu messen, bauten die Forschenden groß angelegte „Landkarten“ des Stoffwechsels – sogenannte genomweite Stoffwechselmodelle – für 32 unterschiedliche Fliegengewebe. Sie kombinierten ein vorhandenes, kuratiertes Netzwerk chemischer Reaktionen mit Einzelzell‑Genexpressionsdaten, die anzeigen, welche Stoffwechselgene in jedem Gewebe aktiviert sind. So konnten sie vergleichen, wie viele Reaktionen, Metabolite und Gene in jedem gewebespezifischen Netzwerk aktiv sind und welche Pfade in Muskel, Fettkörper, Darm und verschiedenen Nervenzelltypen betont werden.
Unterschiedliche Treibstoffaufgaben für verschiedene Organe
Der Vergleich zeigte klare metabolische „Persönlichkeiten“ der Gewebe. Fettkörper und Oenocyten – die Fliegenentsprechungen von menschlichem Fett und Leber – enthielten die vielfältigsten Reaktionssets, insbesondere solche, die Fette über Beta‑Oxidation verbrennen. Der Muskel hingegen hatte zwar nicht das größte Netzwerk, zeigte aber den höchsten Anteil an Reaktionen, die Substanzen in und aus Zellen transportieren, was darauf hindeutet, dass Muskel ein wichtiges Zentrum für den Austausch von Treibstoffen und Bausteinen mit dem restlichen Körper ist. Die Forschenden prüften außerdem, ob die vorhergesagten Pfade mit echten Metabolitmustern aus verschiedenen Körperregionen übereinstimmen. Mit zielgerichtetem Metabolomik‑Profiling analysierten sie Hunderte kleiner Moleküle aus Fliegenköpfen, Thorax, Darm und Abdomen und fragten dann, ob in den Daten angereicherte Pfade mit den Modellen übereinstimmen. In Muskel und Fettkörper war die Übereinstimmung stark, was Vertrauen gibt, dass die gewebespezifischen Modelle die reale Biologie besser erfassen als allein die Genexpression.
Was eine hochzuckerhaltige Ernährung mit dem Treibstofffluss im Muskel macht
Mit einem validierten Muskelmodell simulierte das Team, was passiert, wenn Fliegen langfristig mit einer hochzuckerhaltigen Diät gefüttert werden – einem etablierten Modell für Typ‑2‑Diabetes. Sie schränkten das Modell mit bekannten Merkmalen diabetischer Muskulatur ein, etwa vermindertem Glukose‑Aufnahmevermögen und verlangsamtem Ablauf des zentralen Energiestrahls in den Mitochondrien. Computergestützte „Fluss“‑Analysen – Berechnungen, wie schnell Reaktionen ablaufen können – zeigten breite Reduktionen bei Reaktionen, die vom Redoxpaar NAD/NADH abhängen, Moleküle, die Elektronen transportieren und für die Energieproduktion essenziell sind. Insbesondere verlangsamten sich Reaktionen in dem zentralen zuckerabbauenden Pfad, der Glykolyse, einschließlich solcher, die durch das Enzym GAPDH katalysiert werden. Das Modell sagte außerdem einen etwa ein Vierteligen Rückgang der Fähigkeit des Muskels voraus, insgesamt NADH zu produzieren, was auf eine gestresste Redox‑Bilanz hindeutet. Direkte Messungen im thorakalen Muskel der Fliege bestätigten, dass das Verhältnis von NAD zu NADH unter einer hochzuckerhaltigen Ernährung tatsächlich sank.
Markierten Zucker und oxidierte Proteine verfolgen
Um zu prüfen, ob diese vorhergesagten Engpässe tatsächlich in lebenden Tieren auftreten, fütterten die Forschenden Fliegen mit einer hochzuckerhaltigen Diät, die vollständig mit Kohlenstoff‑13 markierte Glukose enthielt, und verfolgten dann, wohin der markierte Kohlenstoff gelangte. Sie fanden, dass frühe glykolytische Zwischenprodukte stromaufwärts von GAPDH akkumulierten, während nachgelagerte Produkte und deren markierte Anteile sanken, was auf eine echte Verlangsamung an und unterhalb dieses Schritts hinweist. Ebenso waren Beiträge von Glukosekohlenstoff zum zentralen Energiestoffwechsel reduziert. Gleichzeitig zeigte Redox‑Proteomik – eine Methode zur Erkennung oxidativer Veränderungen an spezifischen Aminosäuren in Proteinen – eine verstärkte Oxidation vieler glykolytischer Enzyme, einschließlich mehrerer Stellen an GAPDH. Entlang der Glykolyse neigten Enzyme, die mehr oxidative Modifikationen trugen, dazu, größere Vorhersagerückgänge im Fluss zu zeigen, obwohl ihre Gesamtproteinmengen meist unverändert blieben. Das legt nahe, dass chemische Schäden durch oxidativen Stress, nicht der Verlust der Enzymmenge, ein treibender Faktor für die beeinträchtigte Zuckerverarbeitung im Muskel sind.
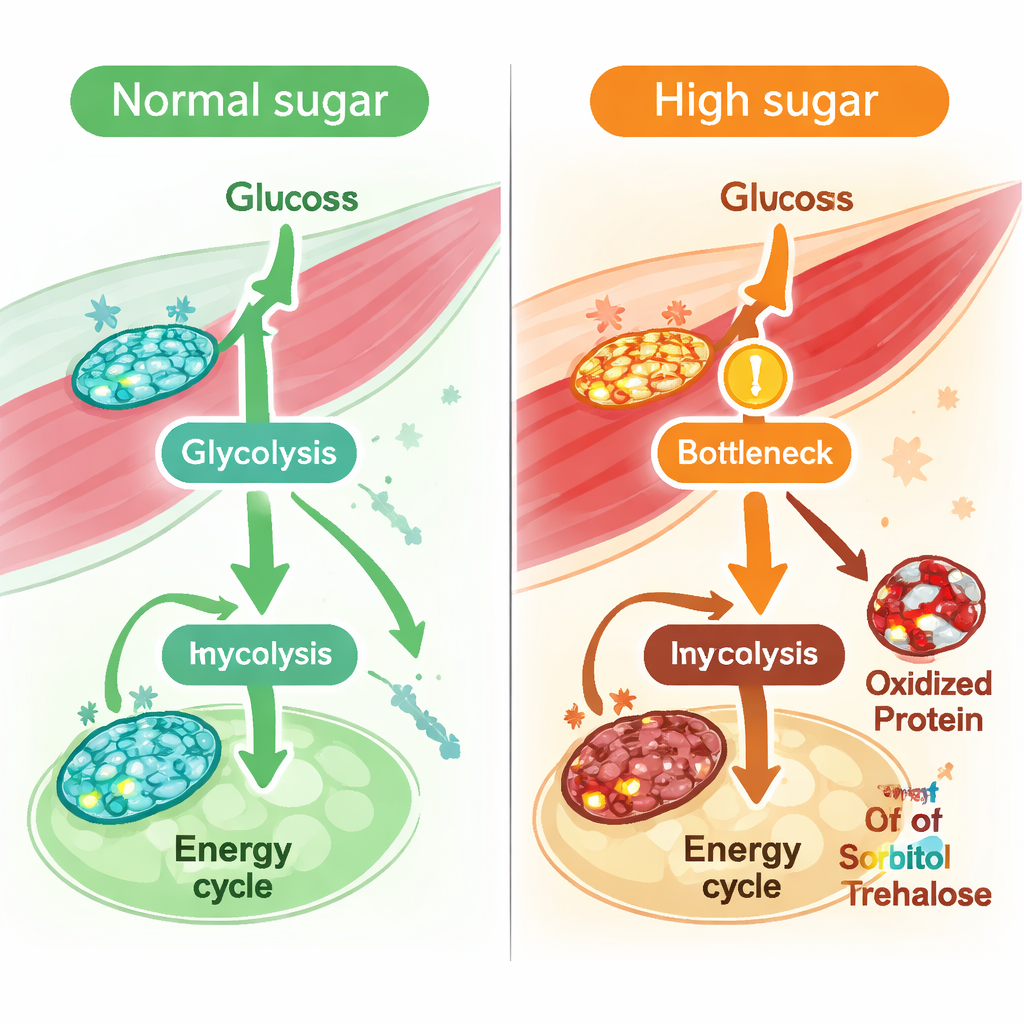
Verborgene Probleme bei Fructose‑ und Saccharose‑Verarbeitung
Über einzelne Reaktionen hinaus mittelte das Team Flüsse über ganze Pfade, um zu sehen, welche am stärksten durch hohen Zucker gestört wurden. Glykolyse, Zitratzyklus und oxidative Phosphorylierung zeigten alle Rückgänge, doch einer der stärksten vorhergesagten Abnahmen betraf den Fructose‑Stoffwechsel. Die Metabolitprofilierung des Muskels unterstützte diese Beobachtung: Sorbitol und Trehalose/Saccharose stiegen an, und ein Schlüsselenzym, das Trehalose in Glukose umwandelt – Trehalase – zeigte sowohl reduzierte vorhergesagte Aktivität als auch vermehrte Oxidation an einer empfindlichen Methionin‑Reststelle. Zusammengenommen deuten diese Befunde auf eine breitere Störung in der Art und Weise hin, wie Muskel mit diätetischen Zuckern umgeht – insbesondere mit fructoseähnlichen und saccharoseabgeleiteten Treibstoffen – bei chronischer Zuckerüberladung.
Was das für das Verständnis von Diabetes bedeutet
Kurz gesagt zeigt diese Arbeit, dass zu viel Zucker nicht nur die Blutbahn überlädt; er formt auch unauffällig um, wie Muskelzellen Treibstoff leiten und verbrennen. Durch den Aufbau detaillierter, gewebespezifischer Stoffwechselkarten für die Fruchtfliege und deren Abgleich mit Metabolomik, Isotopenverfolgung und Redox‑Proteomik zeigen die Forschenden, dass hoher Zuckerkonsum Redox‑Stress treibt, Schlüssel‑Glykolyse‑Enzyme wie GAPDH oxidiert, den Zuckerabbau verlangsamt und Fructose‑bezogene Pfade stört. Diese in einem gut handhabbaren Modellorganismus gewonnenen Einsichten bieten einen starken Rahmen, um zu identifizieren, welche Reaktionen und Pfade in menschlichem Muskel am wichtigsten sind, um sie zu schützen oder wiederherzustellen, um Typ‑2‑Diabetes vorzubeugen oder zu behandeln.
Zitation: Moon, S.J., Hu, Y., Dzieciatkowska, M. et al. Modeling tissue-specific Drosophila metabolism identifies high sugar diet-induced metabolic dysregulation in muscle at reaction and pathway levels. Nat Commun 17, 1692 (2026). https://doi.org/10.1038/s41467-026-68395-3
Schlüsselwörter: Drosophila‑Stoffwechsel, gewebespezifische Stoffwechselmodelle, hochzuckerhaltige Ernährung, Muskuläre Glykolyse, Redox‑Regulation