Clear Sky Science · de
OCT4 erhöht die Start-Effizienz spät replizierender DNA-Ursprünge in Maus-embryonalen Stammzellen
Warum das für unsere Zellen wichtig ist
Jedes Mal, wenn sich eine Zelle teilt, muss sie ihre gesamte DNA genau und nach Plan kopieren. Schlägt dieser Kopiervorgang fehl, kann das zu Entwicklungsstörungen oder Erkrankungen bis hin zu Krebs führen. Diese Studie untersucht, wie ein zentrales Stammzellprotein, OCT4, die Organisation des Zeitpunkts und der Orte steuert, an denen die DNA in Maus-embryonalen Stammzellen begonnen wird zu kopieren — und liefert damit Einblicke, wie frühe Embryonen ihr Genom stabil halten, obwohl sie äußerst schnell teilen.
Kartierung, wann DNA kopiert wird
Die Autorinnen und Autoren konzentrieren sich auf die „Replikationszeit“ — die Reihenfolge, in der verschiedene Genomabschnitte während der DNA-Kopierphase des Zellzyklus, der S-Phase, dupliziert werden. Das Genom ist in große Nachbarschaften oder Timing-Domänen unterteilt, die früh, in der Mitte oder spät in der S-Phase kopiert werden. Mithilfe hochdurchsatzfähiger Sequenziermethoden, die neu synthetisierte DNA markieren, kartierte das Team die Landschaft der Replikationszeitpunkte in Maus-embryonalen Stammzellen und verglich sie mit reiferen Zelltypen wie Fibroblasten und mesenchymalen Stammzellen. Sie identifizierten Tausende von „Initiationszonen“, DNA-Abschnitte, an denen die Replikation tatsächlich beginnt, und klassifizierten sie als früh, mittel oder spät, je nachdem, in welche Timing-Domäne sie fallen.
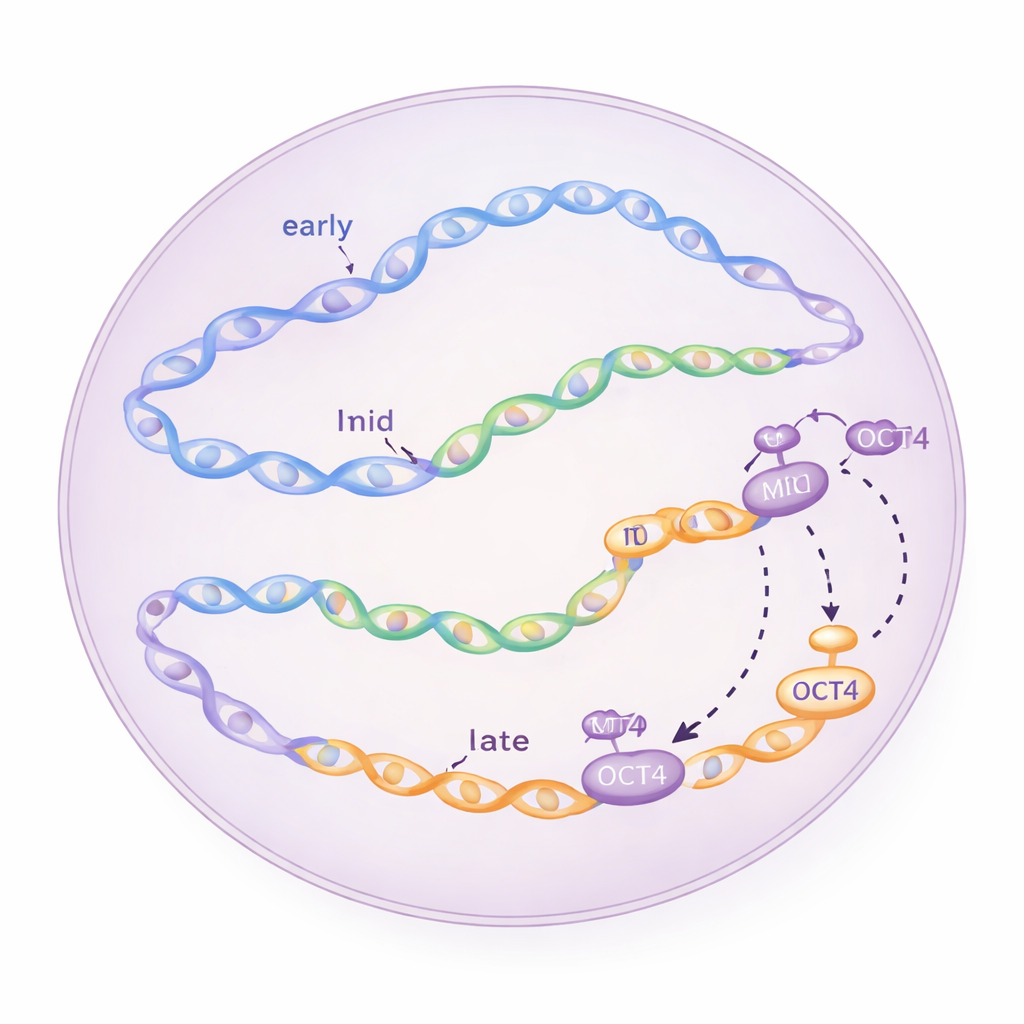
Späte Starter, die vorrücken
Konventionelle Annahme ist, dass Regionen, die für eine späte Replikation vorgesehen sind, größtenteils bis zum Ende der S-Phase warten, um mit der Kopie zu beginnen. Überraschenderweise beobachteten die Forschenden in embryonalen Stammzellen, dass einige Initiationszonen in späten Domänen bereits sehr kurz nach Beginn der S-Phase aktiv wurden — innerhalb nur einer bis zwei Stunden. Durch Synchronisieren der Zellen in verschiedenen Zellzyklusphasen und wiederholte Aufnahmen neu synthetisierter DNA bestätigten sie, dass diese „späten“ Zonen tatsächlich früh aufleuchten und dass ihre Aktivität von üblichen Zellzyklus-Regulatoren wie den Kinasen CDC7 und CDK1 sowie vom ATR-Checkpointweg abhängt, der normalerweise Überlastung der Replikationsmaschinerie verhindert.
Offene DNA-Nachbarschaften und die Rolle von OCT4
Um zu verstehen, was diese ungewöhnlich früh aktivierten späten Regionen besonders macht, untersuchte das Team ihre lokale Umgebung. Sie überlagerten Replikationskarten mit Daten zur RNA-Produktion und zu Chromatinmarken — chemischen Markierungen und Strukturmerkmalen, die anzeigen, ob DNA offen und zugänglich ist oder dicht verpackt vorliegt. Frühe Initiationszonen lagen tendenziell in der Nähe aktiver Gene und offenem Chromatin, während späte Zonen häufiger in reprimierten, eng gepackten Bereichen vorkamen. Dennoch zeigten gerade jene späten Zonen, die in embryonalen Stammzellen früh aktiv wurden, Merkmale von Offenheit: Sie fielen mit zugänglichem Chromatin, enhancerähnlichen Elementen und Bindungsstellen für Pluripotenzfaktoren wie OCT4, SOX2, NANOG und KLF4 zusammen. Das legt nahe, dass dieselben Proteine, die die Entwicklungsflexibilität von Stammzellen erhalten, auch bestimmte späte Regionen des Genoms für eine frühere Replikation vorbereiten könnten.
OCT4 ausschalten verschiebt den Zeitplan
Die Autorinnen und Autoren prüften diese Idee mit einer speziellen Stammzelllinie, in der sich OCT4-Spiegel durch Zugabe des Medikaments Doxycyclin schnell reduzieren lassen. Wurde OCT4 nur für einen Teil eines einzigen Zellzyklus vermindert, blieb der allgemeine Übergang in die S-Phase weitgehend unverändert, doch das Starten vieler mittel- und spätliegender Initiationszonen wurde abgeschwächt oder verzögert. Genomweite Analysen zeigten, dass in Regionen, in denen OCT4 normalerweise bindet, sowohl die Chromatinzugänglichkeit als auch Signale für Replikationsinitiation parallel sanken, wenn OCT4 ausgeschaltet wurde. Statistische Modellierungen bestätigten, dass dieser Effekt in spät replizierenden Zonen am stärksten war: Je stärker eine Initiationszone für offenes Chromatin auf OCT4 angewiesen war, desto stärker litt ihre Replikationseffizienz bei dessen Fehlen.
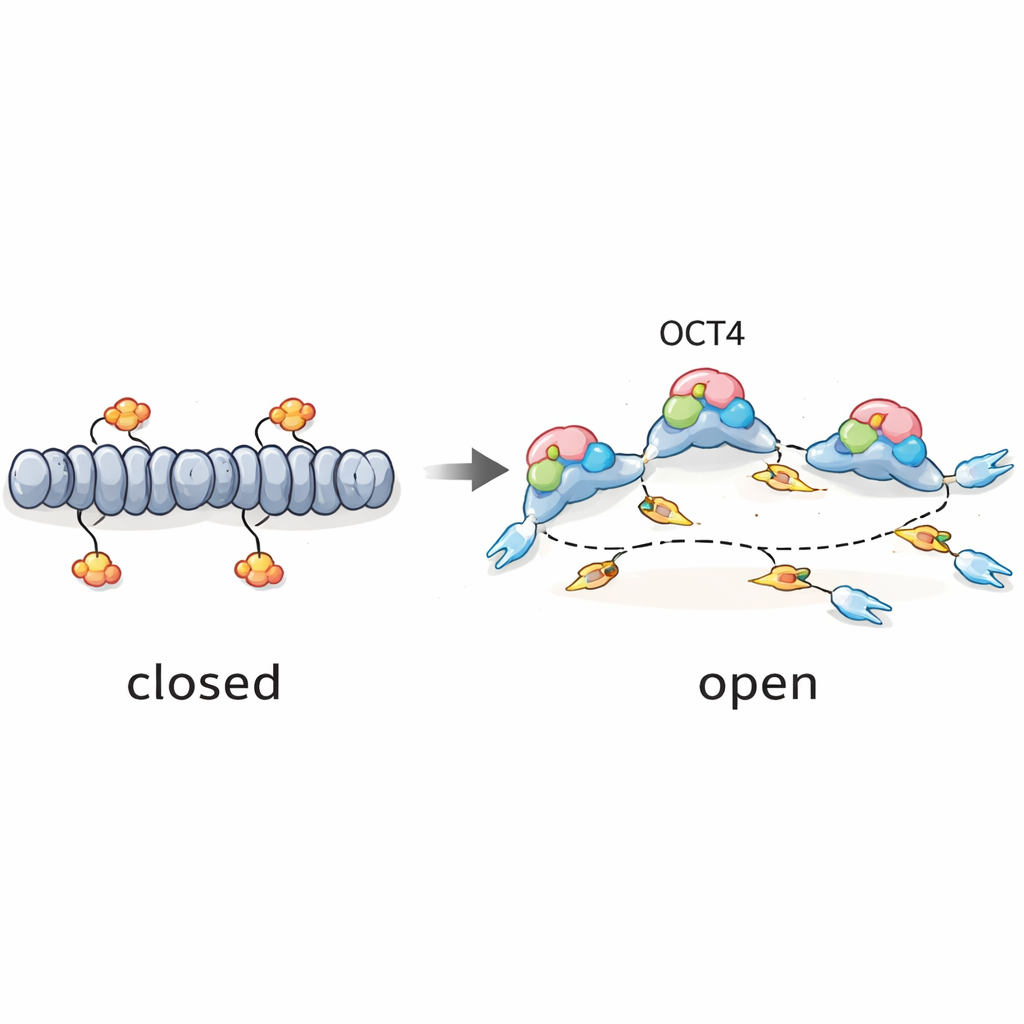
Ein Pionierfaktor, der auch das DNA-Kopieren timt
Insgesamt stützen die Ergebnisse eine einfache Idee: OCT4 wirkt nicht nur als „Pionier“-Faktor für Genaktivität, sondern auch für die DNA-Replikation. Indem OCT4 bestimmte späte Regionen des Genoms in embryonalen Stammzellen aufschließt, schafft es effiziente Startpunkte für die DNA-Replikation, die früher und zuverlässiger aktiv werden können als in differenzierten Zellen. Gleichzeitig justieren globale Regulatoren wie ATR, CDC7 und CDK1, wie viele dieser Stellen aktiviert werden dürfen, um eine Überlastung des Replikationssystems zu verhindern. Für eine allgemeine Leserschaft lautet die Kernbotschaft: Dieselben Proteine, die Stammzellen vielseitig halten, helfen auch dabei zu steuern, wann verschiedene Teile ihrer DNA kopiert werden — und fügen damit eine weitere Ebene zum Verständnis hinzu, wie sich schnell teilende embryonale Zellen Ordnung in ihrem Genom bewahren.
Zitation: Rodriguez-Carballo, E., Dionellis, V.S., Ntallis, S.G. et al. OCT4 enhances the firing efficiency of late DNA replication origins in mouse embryonic stem cells. Nat Commun 17, 1686 (2026). https://doi.org/10.1038/s41467-026-68389-1
Schlüsselwörter: DNA-Replikationszeitpunkt, embryonale Stammzellen, OCT4, Chromatinzugänglichkeit, Origin-Firing