Clear Sky Science · de
Mechanische Verjüngung seneszenter Stammzellen und gealterter Knochen durch Chromatin-Umlagerung
Warum es wichtig ist, Knochen jung zu halten
Mit dem Alter verlieren unsere Knochen allmählich an Festigkeit: sie werden dünner und brüchiger. Das erhöht das Risiko für Frakturen, den Verlust von Selbstständigkeit und chronische Schmerzen. Die meisten aktuellen Behandlungen zielen darauf ab, den Knochenabbau zu verlangsamen oder Mineralien zuzuführen, reparieren aber nicht direkt die Alterung der Stammzellen, die Knochen aufbauen. Diese Studie verfolgt einen anderen Ansatz: gezielt eingesetzte physikalische Kräfte – statt Medikamente – zu nutzen, um alternde knochenbildende Stammzellen „zu verjüngen“ und so die Knochengesundheit und die allgemeine Fitness älterer Mäuse zu verbessern.
Wenn die Knochenbauer altern
Tief im Inneren unserer Knochen liegen Knochenmark-Mesenchymstammzellen, die Baumeister, die sich in knochenbildende Zellen verwandeln können. Mit dem Alter teilen sich diese Stammzellen weniger, bauen weniger Knochen und zeigen typische Merkmale zellulären Alterns wie DNA-Schäden und entzündliche Signale. Die Forschenden verglichen Zellen von jüngeren und älteren menschlichen Spendern und stellten fest, dass gealterte Stammzellen nicht nur biochemisch anders waren – sie waren mechanisch schwächer. Sie erzeugten geringere innere Zugkräfte, hatten ein schlafferes inneres Gerüst und zeigten eine schlechtere Übertragung mechanischer Signale in den Zellkern. In Knochengewebe alter Mäuse zeigte sich ein ähnlicher Rückgang: das schwammige Knochengeflecht war ausgedünnt, wichtige mechanische Signalproteine waren reduziert und Altersmarker erhöht.
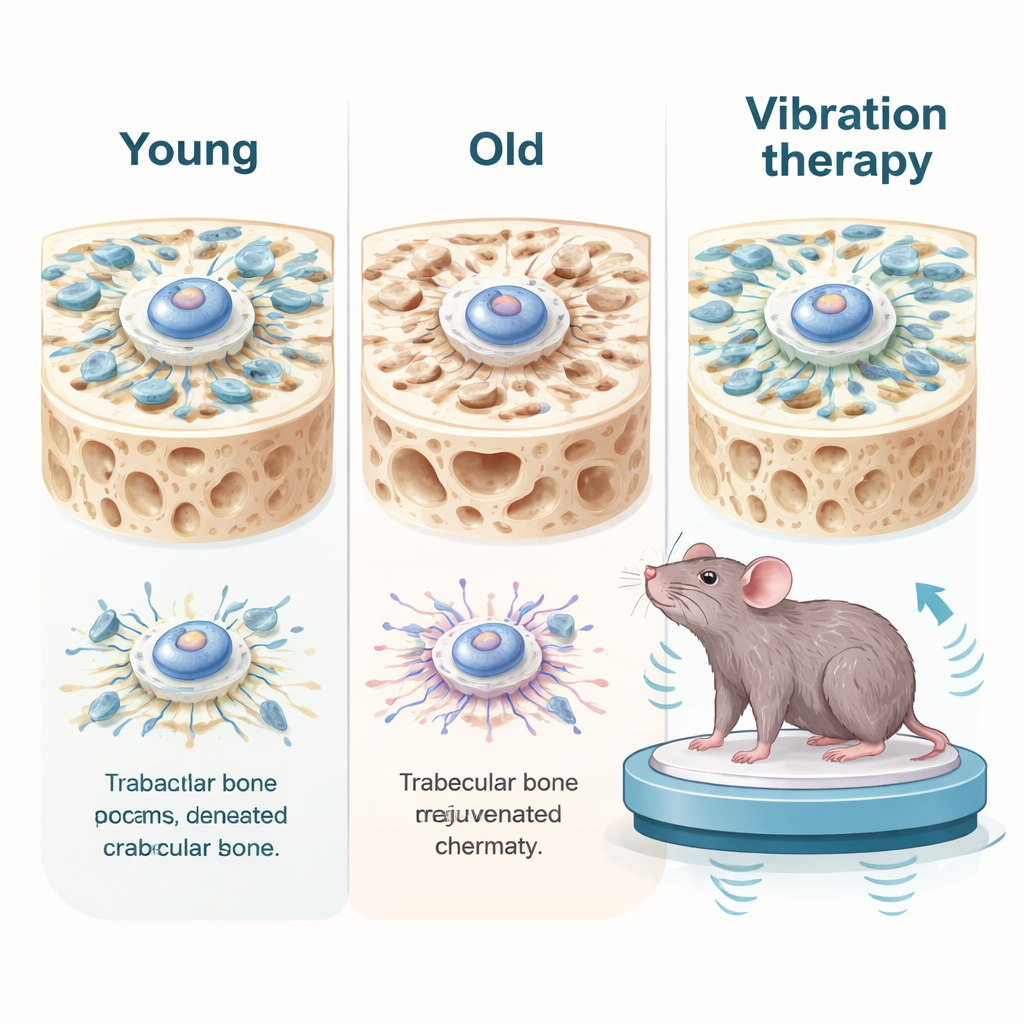
Zellen durch sanftes Ziehen zurück zur Jugend
Das Team fragte dann, ob sich diese Alterungsmerkmale durch Wiederherstellung mechanischer Kräfte umkehren lassen. In Zellkulturen übten sie sanftes Dehnen auf seneszente Stammzellen aus oder setzten ein Medikament ein, das die Aktivität molekularer Motoren steigert. Diese Behandlungen stärkten die zellulären Zugkräfte und verbesserten die Organisation des inneren Gerüsts. Bemerkenswerterweise begannen gealterte Zellen jünger zu wirken: Seneszenzmarker fielen, DNA-Schäden nahmen ab und die Zellen teilten sich wieder leichter. Das Gegenteil war ebenfalls der Fall – wenn sie die Umgebung junger Zellen abmilderten oder ihre kontraktile Maschinerie chemisch schwächten, glitten die Zellen in einen altersähnlichen Zustand, verlangsamten sich und zeigten Altersmarker, sogar in einem knochenähnlichen 3D-Gel.
Wie Kraft mit Genen kommuniziert
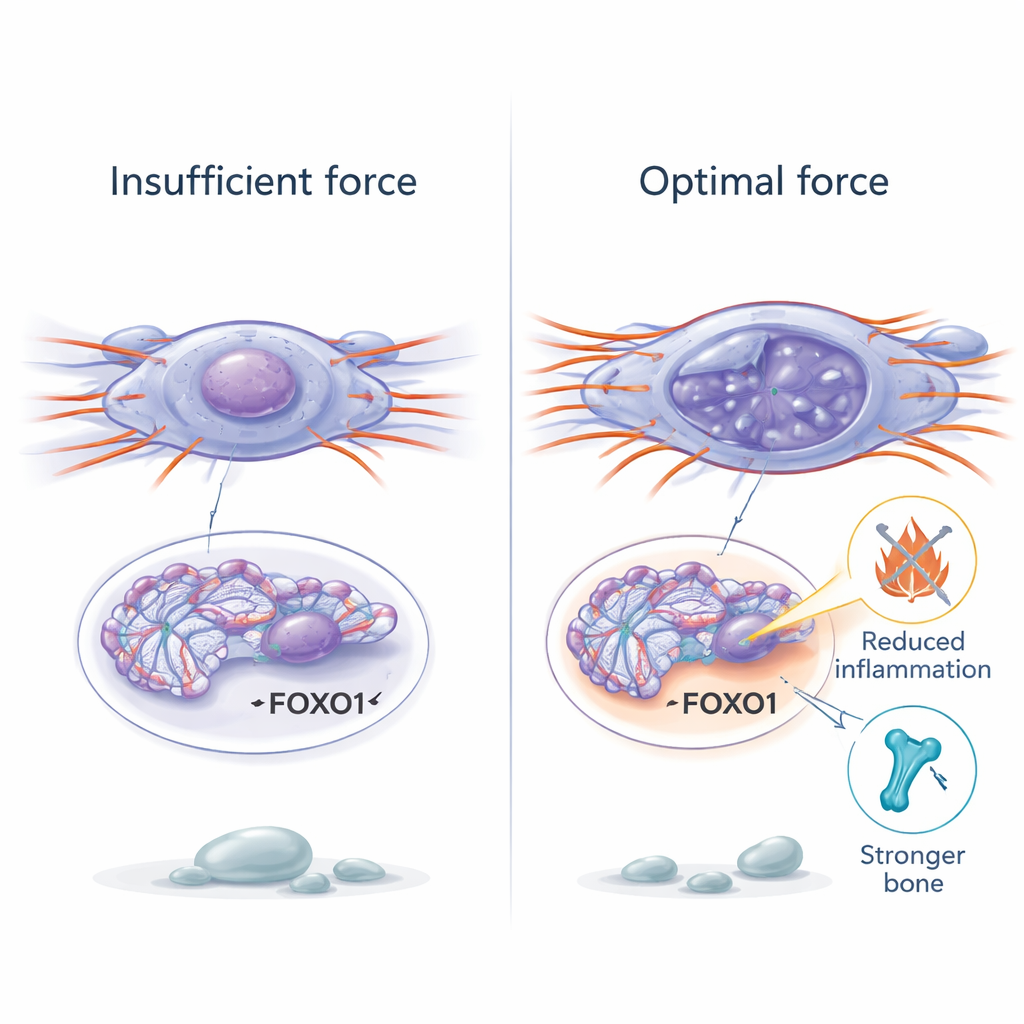
Um zu verstehen, wie physische Kräfte das Zellverhalten so tiefgreifend ändern können, betrachteten die Forschenden das Chromatin – die verpackte Form der DNA im Zellkern. In alten Stammzellen war das Chromatin dichter kondensiert und weniger zugänglich, sodass hilfreiche Gene schwerer aktiviert werden konnten. Die Wiederherstellung mechanischer Kräfte ließ das Chromatin lokal entspannen und erhöhte chemische Markierungen, die mit offenem, aktivem Erbgut assoziiert sind. Mit einem genomweiten Test der Chromatinzugänglichkeit fanden sie, dass sanfte mechanische Stimulation Regionen in der Nähe von Genen öffnete, die an der Steuerung des Alterns beteiligt sind. Ein Gen, FOXO1, fiel als besonders kraftempfindlich auf. Bei erhöhter mechanischer Belastung wurde die DNA-Region von FOXO1 zugänglicher, seine Aktivität stieg und die Zellen wurden weniger seneszent. Die Blockade von FOXO1 beseitigte die Vorteile der mechanischen Stimulation und zeigte es als wichtigen Schalter, der physische Belastung mit genetischen Programmen für Widerstandsfähigkeit und Reparatur verbindet.
Die richtige Balance mechanischer Therapie finden
Die Forschenden testeten mechanische Stimulation dann an lebenden Mäusen. Ältere Tiere wurden einen Monat lang täglich für kurze Sitzungen einer niederintensiven Vibrationsplattform ausgesetzt, während andere Tiere durch Aufhängung am Schwanz eine Entlastung der Hinterbeine erhielten, was extreme Inaktivität nachahmt. Bei gealterten Mäusen steigerte sanfte Vibration die mechanischen Signale im Knochen, reduzierte Alters- und Entzündungsmarker und baute das schwammige Knochengeflecht teilweise wieder auf. Sie verbesserte zudem die Griffkraft, die Ausdauer bei Bewegung, leistungsbezogene Gedächtnisaufgaben und senkte Entzündungswerte im Blut, in Leber und Nieren. Wurde die Vibration jedoch ohne Erholungstage kontinuierlich angewandt, verschwanden die Vorteile und kehrten sich sogar um: die Knochenstruktur verschlechterte sich, DNA-Schäden nahmen zu und die Entzündung stieg. In Zellstudien führten zu starke oder zu häufige Dehnungen zu DNA-Brüchen und trieben die Zellen zurück in die Seneszenz, was zeigt, dass mechanische Kraft je nach Dosis heilen oder schaden kann.
Von Bewegungssimulatoren zu künftigen Therapien
Für Laien lautet die zentrale Botschaft: Unsere Zellen reagieren nicht nur auf Hormone und Chemikalien – sie „hören“ auch genau auf physische Kräfte. In dieser Arbeit zeigen die Autorinnen und Autoren, dass moderate, gut abgestimmte mechanische Stimulation alternde Knochenstammzellen wieder wecken kann, schützende Genprogramme wie FOXO1 öffnet, geschwächte Knochen wiederaufbaut und chronische Entzündung bei älteren Mäusen dämpft. Zugleich beschleunigen zu wenig oder zu viel Kraft den zellulären Verschleiß. Diese Ergebnisse deuten darauf hin, dass sorgfältig konzipierte mechanische Therapien – etwa spezifische Bewegungsprogramme oder sichere, vibrationsbasierte Geräte – eines Tages Medikamente ergänzen könnten, um Knochen und möglicherweise andere Gewebe länger gesund zu erhalten.
Zitation: Liu, X., Ye, Y., Li, Z. et al. Mechanical rejuvenation of senescent stem cells and aged bone via chromatin remodeling. Nat Commun 17, 1684 (2026). https://doi.org/10.1038/s41467-026-68387-3
Schlüsselwörter: Knochenalterung, mechanische Stimulation, Stammzellverjüngung, Chromatin-Umlagerung, FOXO1