Clear Sky Science · de
Effiziente und stabile katalytische Hydrolyse von Perfluorkohlenstoff durch SO2-vermittelte Protonenzufuhr
Warum dieses hartnäckige Treibhausgas wichtig ist
Einige industrielle Gase sind so beständig, dass sie nach ihrer Freisetzung Zehntausende von Jahren in der Atmosphäre verbleiben. Tetrafluormethan (CF4), ein Perfluorkohlenstoff, der bei der Aluminiumgewinnung und in der Halbleiterfertigung verwendet und freigesetzt wird, gehört zu den schlimmsten Verursachern: Es speichert Wärme etwa 7.400-mal wirksamer als Kohlendioxid. Diese Studie untersucht einen neuen Weg, CF4 effizient und zuverlässig abzubauen und dieses nahezu unzerstörbare Schadstoffmolekül unter praxisnahen Bedingungen in sicherere Produkte umzuwandeln.
Ein hartes Molekül, das sich weigert zu zerbrechen
CF4 gehört zur größeren Familie der PFAS, Chemikalien, die für ihre Umweltpersistenz bekannt sind. Was CF4 besonders herausfordernd macht, sind seine extrem starken Kohlenstoff–Fluor-Bindungen und seine sehr lange atmosphärische Lebensdauer, die auf mehr als 50.000 Jahre geschätzt wird. Traditionelle Verfahren zum Abbau von CF4 erfordern sehr hohe Temperaturen und führen oft zu schneller Abnutzung und Aktivitätsverlust der dafür eingesetzten Katalysatoren. Neue Klimapolitiken, wie der CO2-Grenzausgleich der Europäischen Union, üben jedoch zunehmend Druck auf energieintensive Branchen aus, diese Emissionen zu reduzieren, ohne den Energieverbrauch stark zu erhöhen.
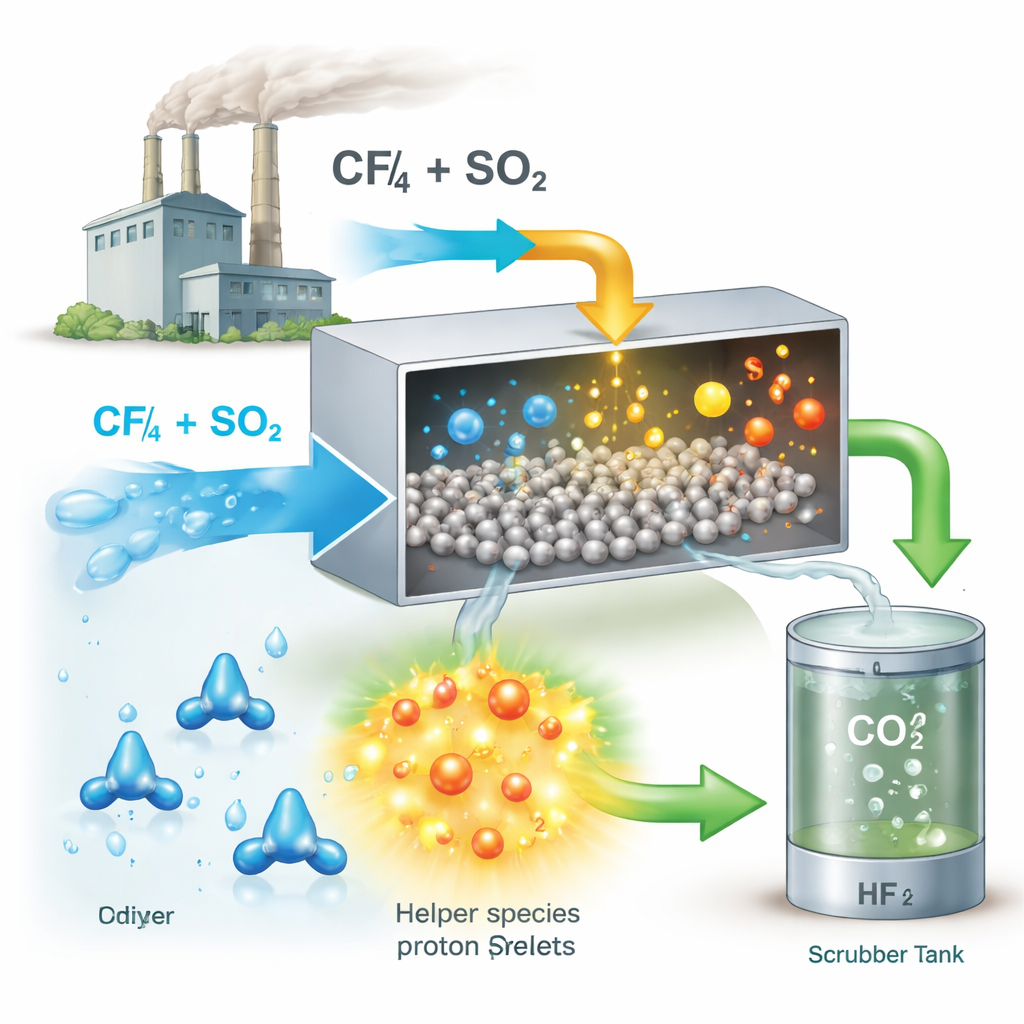
Aus einem häufigen Schadstoff einen Helfer machen
Überraschenderweise fanden die Forschenden heraus, dass ein anderer bekanntes Schadgas, Schwefeldioxid (SO2), zur Lösung des CF4-Problems eingesetzt werden kann. SO2 wird bei der Aluminiumproduktion häufig zusammen mit CF4 freigesetzt. Während SO2 normalerweise Katalysatoren schadet, indem es an deren Oberflächen haftet, zeigte das Team, dass es unter den richtigen Bedingungen das Gegenteil bewirken kann: Es verändert die Katalysatoroberfläche so, dass Wasser leichter zerfällt und mehr reaktive Wasserstoffionen (Protonen) bereitstellt. Diese Protonen sind entscheidend, um die hartnäckigen Bindungen in CF4 zu schwächen und Fluor vom Katalysator zu entfernen, damit dieser weiterarbeitet.
Aufbau von Protonen-»Tankstellen« auf der Oberfläche
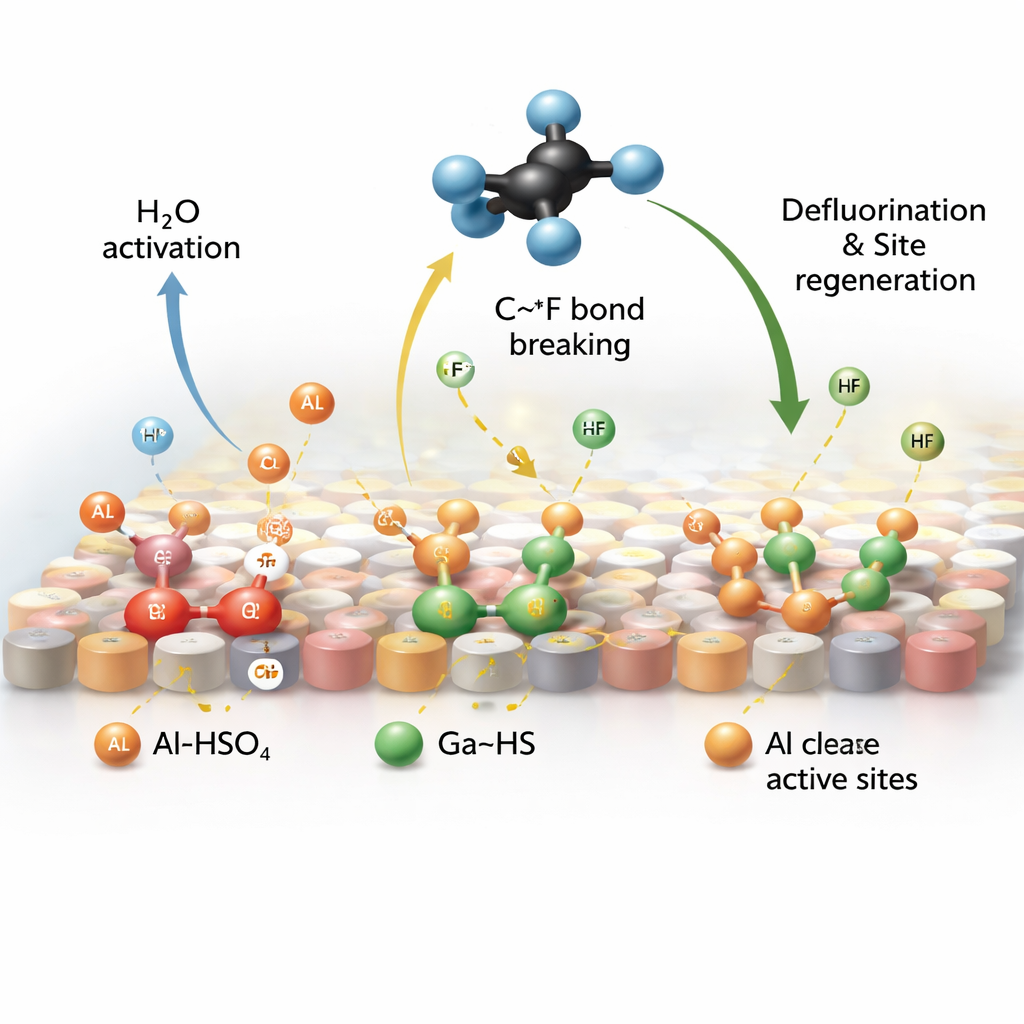
Der entscheidende Fortschritt ist die Schaffung spezieller protonenreicher Stellen direkt auf dem Katalysator, der auf Aluminiumoxid basiert und mit Gallium dotiert ist. Wenn SO2, Wasserdampf und CF4 bei hohen Temperaturen über dieses Material strömen, wandelt sich SO2 in fest gebundene saure Gruppen auf der Oberfläche um. Es entstehen zwei Typen solcher Gruppen: eine hauptsächlich an Aluminium gebundene (Al–HSO4) und eine an Gallium gebundene (Ga–HS). Mithilfe empfindlicher spektroskopischer Methoden und Computersimulationen zeigen die Autorinnen und Autoren, dass die aluminiumbasierten Gruppen CF4 anziehen und die Wasserspaltung fördern, sodass Protonen freigesetzt werden, während die galliumbasierten Gruppen diese Protonen nutzen, um Fluor von vergifteten Stellen abzuziehen und als Fluorwasserstoff freizusetzen, wodurch die Aktivität des Katalysators wiederhergestellt wird.
Rekordleistung unter realen Bedingungen
Da diese Protonen-»Tankstellen« stark verankert sind und bei hohen Temperaturen stabil bleiben, liefern sie reaktive Wasserstoffionen deutlich effektiver als herkömmliche Zusätze. Die Studie zeigt, dass die Aktivierung von Wasser im Vergleich zum Betrieb ohne SO2 etwa sechsmal höher ist und die Protonenverfügbarkeit ungefähr um das Zehnfache zunimmt. Dadurch gelingt der vollständige Abbau von CF4 bei 550 °C statt der üblichen 700 °C, wodurch der Energiebedarf des Prozesses gesenkt wird. Ebenso wichtig ist, dass der Katalysator über mehr als 2.500 Stunden—also über drei Monate Dauerbetrieb—ohne spürbaren Leistungsverlust läuft und über einen weiten Bereich von SO2-Konzentrationen funktioniert, wie sie in Industrieabgasen vorkommen.
Ein neuer Weg zur Reinigung persistenter Luftschadstoffe
Für Nichtfachleute lässt sich das Ergebnis so beschreiben: Dem Katalysator wird eine neue Fähigkeit beigebracht—ein unerwünschtes Gas (SO2) zu nutzen, um winzige, robuste Säurestellen zu erzeugen, die ihm die Protonen liefern, die nötig sind, um eines der stärksten bekannten Treibhausgase aufzubrechen. Indem sowohl die Zerstörung von CF4 erleichtert als auch die Lebensdauer des Katalysators verlängert wird, weist diese Strategie auf praktikable Gaswäscher hin, die an den Schornsteinen von Aluminium- und Halbleiterwerken angebracht werden könnten. Allgemeiner könnte dasselbe Prinzip der lokalen Protonenregulierung angepasst werden, um andere gasförmige PFAS zu zersetzen und so ein vielversprechendes Instrument zur Verringerung der langfristigen Klima- und Umweltbelastung moderner Fertigungsprozesse bereitzustellen.
Zitation: Zhang, H., Luo, T., Chen, Y. et al. Efficient and stable catalytic hydrolysis of perfluorocarbon enabled by SO2-mediated proton supply. Nat Commun 17, 597 (2026). https://doi.org/10.1038/s41467-026-68386-4
Schlüsselwörter: Tetrafluormethan, PFAS-vernichtung, katalytische Hydrolyse, Schwefeldioxid-Förderung, industrielle Emissionskontrolle