Clear Sky Science · de
Präzise Entfernung expandierter GGC-Repeat in NOTCH2NLC mittels CRISPR/Cas9 zur Behandlung der neuronal-intranukleären Inklusionskrankheit
DNA bearbeiten, um eine rätselhafte Gehirnkrankheit anzugehen
Die neuronal-intranukleäre Inklusionskrankheit (NIID) ist eine seltene, aber verheerende Erkrankung des Gehirns, die Demenz, Bewegungsstörungen und in schweren Fällen einen vorzeitigen Tod verursachen kann. Eine Heilung gibt es derzeit nicht. Diese Studie untersucht, ob ein mächtiges Geneditierungswerkzeug, CRISPR, benutzt werden kann, um einen kleinen, aber toxischen DNA-Abschnitt auszuschneiden, der NIID antreibt, und damit einen Ausblick darauf zu geben, wie künftige Therapien unsere Gene umschreiben könnten, um Hirnerkrankungen zu bekämpfen. 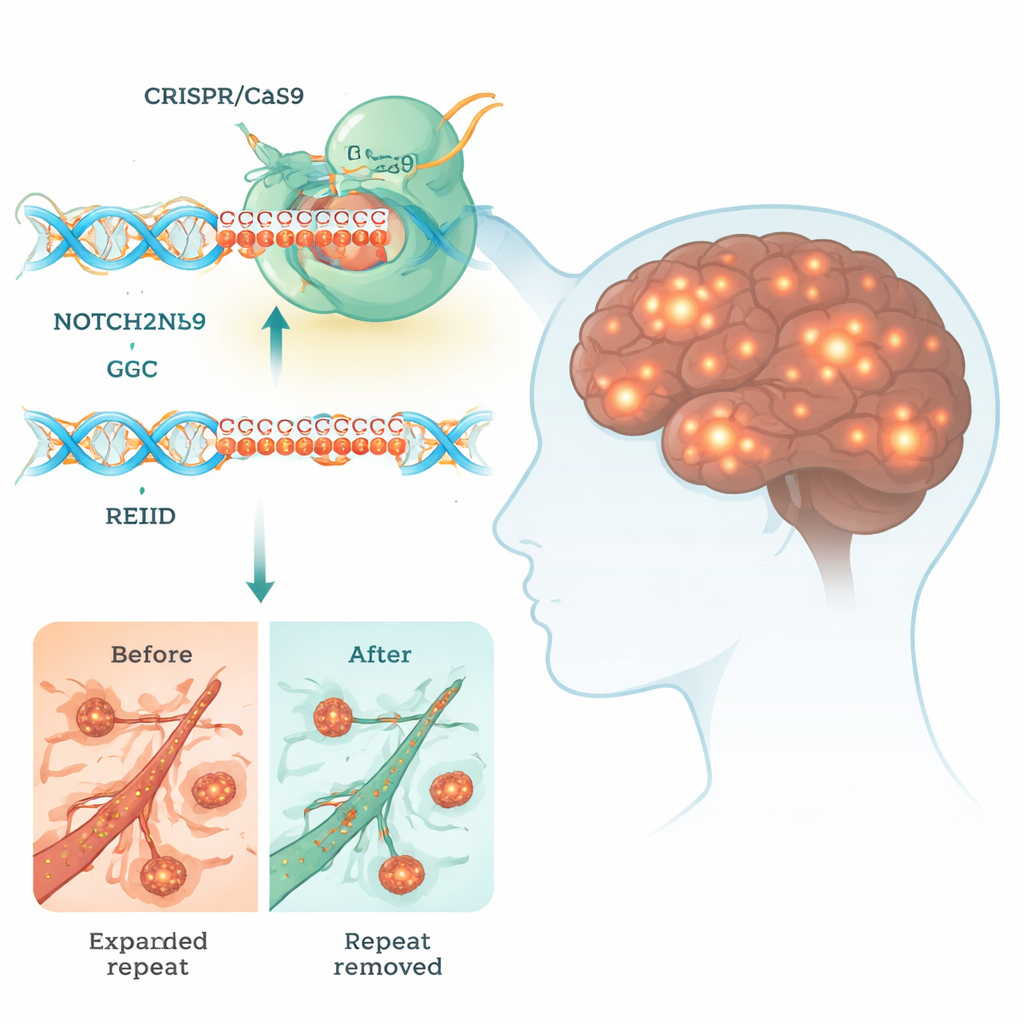
Ein verborgener genetischer Täter
Viele vererbte Gehirnerkrankungen werden durch kurze DNA-Sequenzen verursacht, die weit über ihre normale Länge hinaus expandiert sind. Bei NIID liegt das Problem in einer überlangen Folge der dreibuchstabigen DNA-Einheit „GGC“ im Gen NOTCH2NLC. Obwohl diese Sequenz in einer Region sitzt, die nicht klassisch für ein Protein kodiert, kann sie dennoch von der zellulären Maschinerie abgelesen werden und abnorme Polyglycin-(polyG)-Ketten produzieren. Diese klebrigen Ketten verklumpen zu Einschlusstkörperchen im Zellkern von Nervenzellen und anderen Geweben und stören lebenswichtige Prozesse wie Energieproduktion, RNA-Verarbeitung und den Verkehr von Molekülen zwischen Kern und Zytoplasma.
Die Herausforderung präziser Genchirurgie
Die Entwicklung einer Geneditierungsbehandlung für NIID ist ungewöhnlich schwierig, weil NOTCH2NLC mehrere nahezu identische Schwester-Gene hat, die für die menschliche Gehirnentwicklung wichtig sind. Schneidet CRISPR das falsche Gen, könnte das mehr schaden als nützen. Die Forscher durchsuchten deshalb sorgfältig die DNA-Region um den GGC-Repeat und identifizierten kleine Sequenzunterschiede, die NOTCH2NLC von seinen Verwandten unterscheiden. Anschließend entwarfen sie Paare von CRISPR-Leit-RNAs, die das Cas9-„molekulare Scheren“-Enzym genau vor und nach dem expandierten Repeat positionieren. Diese Doppel-Schnitt-Strategie ermöglicht es dem zellulären Reparatursystem, das toxische Segment zu entfernen, während der Rest der Genfamilie unberührt bleibt.
Von Zellen in der Schale zu patientenabgeleiteten Neuronen
Das Team testete das CRISPR-Design zunächst in Standard-Humanzelllinien und in Zellen, die so konstruiert waren, dass sie einen großen NOTCH2NLC-Repeat tragen. In diesen Modellen schnitt der Editierer effizient den Repeat heraus, und die Menge an polyG-Einschlüssen sank um etwa die Hälfte oder mehr. Danach gingen die Forscher zu induzierten pluripotenten Stammzellen (iPSCs) über, die aus einem NIID-Patienten gewonnen und in neuronale Vorläuferzellen, einen frühen Entwicklungsstand von Gehirnzellen, differenziert wurden. Mithilfe von CRISPR löschten sie entweder den expandierten Repeat oder ersetzten ihn durch eine normallange Version. Detaillierte DNA- und Ganzgenomsequenzierungen zeigten, dass das Editing sehr präzise war, mit geringen Hinweisen auf unerwünschte Schnitte, und die bearbeiteten Zellen teilten und reiften weiterhin normal. 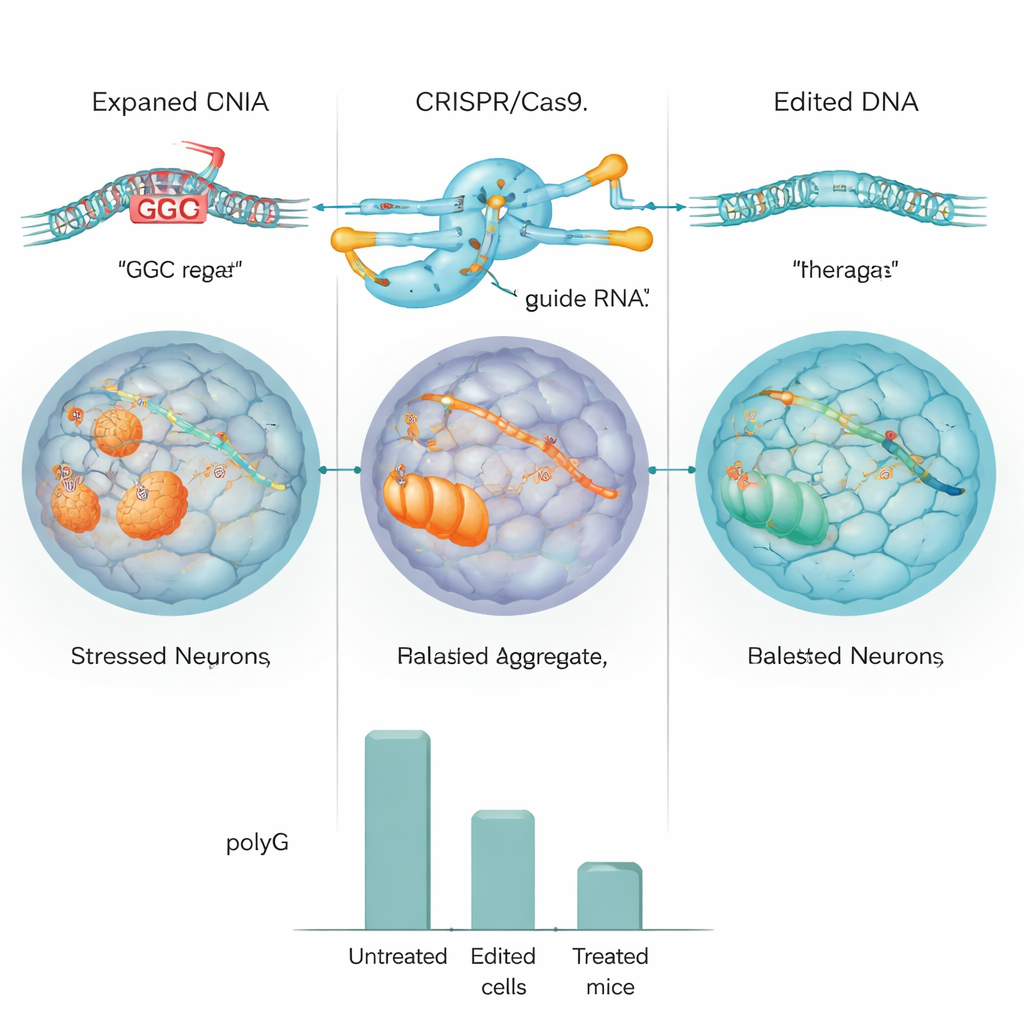
Rettung von Gehirn und Körper in einem Mausmodell
Um zu prüfen, ob dieser Ansatz die Erkrankung tatsächlich verbessern kann, verwendeten die Forscher Mäuse, die so genetisch verändert wurden, dass sie den humanen NOTCH2NLC-Repeat tragen und NIID-ähnliche Merkmale entwickeln, einschließlich nukleärer Einschlüsse, Bewegungsstörungen und verkürzter Lebensdauer. Sie verpackten das CRISPR-System in ein modifiziertes Virus, das sich nach einer einfachen Injektion in den Blutkreislauf neugeborener Mäuse im Gehirn verbreiten kann. Bei behandelten Tieren wurde der expandierte Repeat im Gehirngewebe erfolgreich entfernt. In der Folge fielen die toxischen polyG-Spiegel deutlich, Marker für die Gesundheit der Nervenzellen verbesserten sich, und die fehlregulierte Aktivierung unterstützender Gehirnzellen ging zurück. Verhaltensuntersuchungen zeigten, dass behandelte Mäuse aktiver waren, besser das Gleichgewicht hielten und länger überlebten als ihre unbehandelten Wurfgeschwister. Ähnliche Verbesserungen wurden im Herzen beobachtet, das in diesem Modell ebenfalls polyG akkumuliert.
Was das für künftige Therapien bedeuten könnte
Für Laien lautet die Kernbotschaft, dass NIID überwiegend von einem spezifischen, überlangen DNA-Repeat angetrieben zu sein scheint und dass das präzise Entfernen dieses Repeats viele Krankheitszeichen in Zellen und Mäusen rückgängig machen kann. Diese Arbeit ist noch keine unmittelbar einsatzbereite Therapie für Menschen: Forscher müssen weiterhin die Langzeitsicherheit verfeinern, die Liefermethoden verbessern und in größeren, menschlicheren Tiermodellen testen. Dennoch liefert die Studie einen starken Proof-of-Concept dafür, dass sorgfältig zielgerichtetes Genediting einen toxischen Repeat sicher stummschalten kann, während nahe verwandte Gene verschont bleiben. Diese Strategie könnte eines Tages nicht nur für NIID, sondern auch für andere Gehirn- und Muskelkrankheiten mit ähnlichen Repeat-Expansionen angepasst werden.
Zitation: Xie, N., Pan, Y., Tong, H. et al. Precise excision of expanded GGC repeats in NOTCH2NLC via CRISPR/Cas9 for treating neuronal intranuclear inclusion disease. Nat Commun 17, 1683 (2026). https://doi.org/10.1038/s41467-026-68385-5
Schlüsselwörter: CRISPR-Geneditierung, neuronal-intranukleäre Inklusionskrankheit, Repeat-Expansions-Erkrankungen, NOTCH2NLC, Neurodegeneration