Clear Sky Science · de
Sequenzbasierte generative KI‑Gestaltung vielseitiger Tryptophan‑Synthasen
Enzymen mit KI neue Fähigkeiten beibringen
Die moderne Gesellschaft beruht auf Molekülen – Arzneimitteln, Materialien und Spezialchemikalien –, die oft mit energieintensiven und verschmutzenden Verfahren hergestellt werden. Natürliche Katalysatoren, Enzyme, können ähnliche Aufgaben sauberer und effizienter erledigen, doch das Finden oder Konstruieren des passenden Enzyms für eine neue industrielle Anwendung ist langsam und unsicher. Diese Studie zeigt, dass generative künstliche Intelligenz, dieselbe Technologieklasse, die hinter textschreibenden Chatbots steht, dazu genutzt werden kann, völlig neue Enzyme zu entwerfen, die nicht nur im Labor gut funktionieren, sondern mitunter die besten durch Evolution und jahrelange Ingenieursarbeit hervorgebrachten Varianten übertreffen.
Warum Enzyme im Alltag wichtig sind
Enzyme sind winzige Proteinfabriken, die chemische Reaktionen in lebenden Zellen beschleunigen. Chemiker haben gelernt, sie umzunutzen, um mit weniger Energie und weniger giftigen Reagenzien Arzneimittel, Lebensmittelzutaten und andere wertvolle Produkte herzustellen. Der Haken ist, dass jede neue Anwendung meist ein Enzym mit genau passenden Eigenschaften erfordert – in der Lage, bestimmte Ausgangsstoffe zu akzeptieren, Verarbeitungsbedingungen zu überstehen und hohe Ausbeuten zu liefern. Konventionelle »gerichtete Evolution« verbessert Enzyme, indem viele mutierte Varianten hergestellt und getestet werden, Generation für Generation. Das funktioniert gut, setzt aber auf ein brauchbares Ausgangsenzym und kann Monate bis Jahre Versuch und Irrtum bedeuten, sodass viele nützliche Reaktionen ungeprüft bleiben.
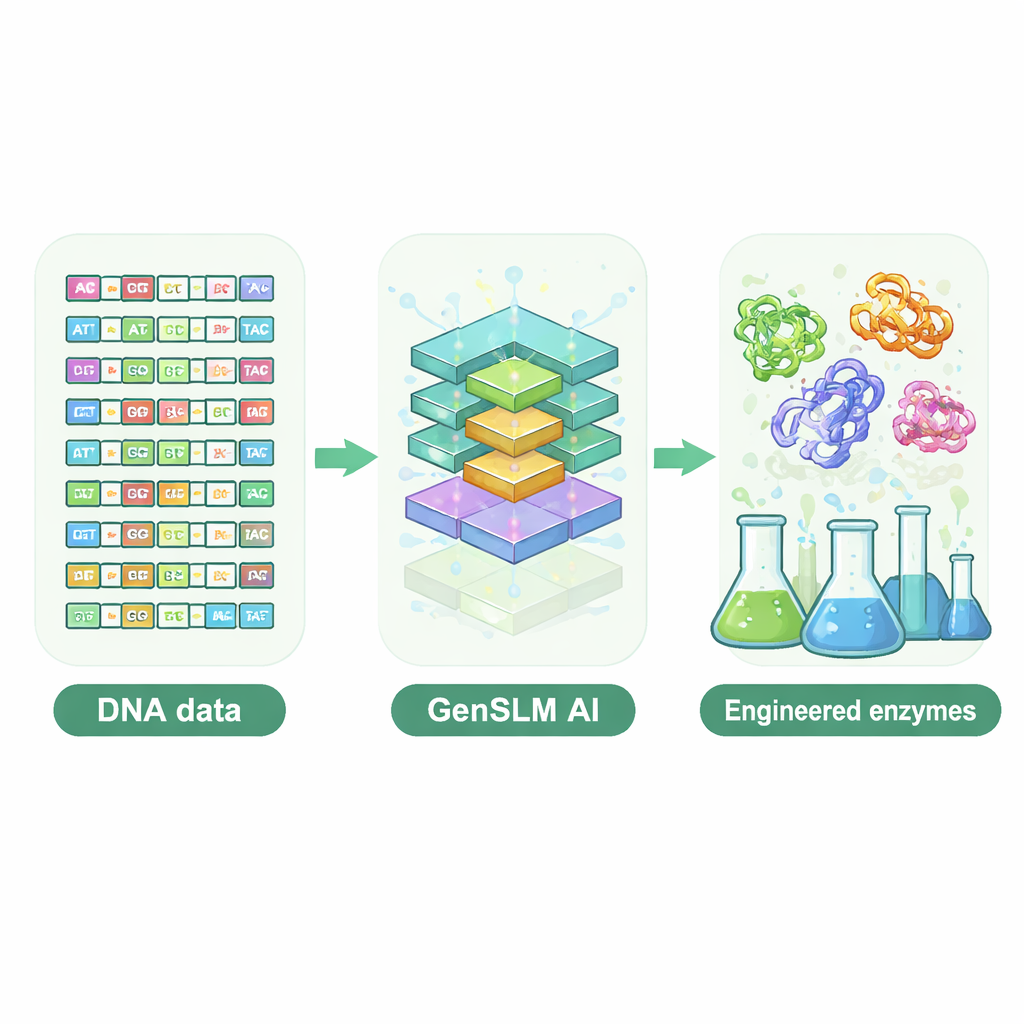
Ein Sprachmodell, das DNA schreibt
Die Forschenden wandten sich einem genomweiten Sprachmodell namens GenSLM zu, das Muster in DNA auf ähnliche Weise lernt, wie ein Sprachmodell Grammatik und Stil in Text erfasst. Anstatt mit fertigen Proteinsequenzen zu arbeiten, liest und schreibt GenSLM DNA in Dreier‑Codons und spiegelt damit wider, wie Zellen Gene in Proteine übersetzen. Das Team feinabgestimmte das Modell zunächst auf Zehntausenden natürlicher Gene für eine besonders komplexe Enzymuntereinheit namens TrpB, die beim Aufbau der Aminosäure Tryptophan hilft. Danach bat man das Modell, Tausende völlig neuer trpB‑Gene zu generieren. Einfache rechnerische Filter sortierten Sequenzen aus, die zu kurz oder zu lang waren, wahrscheinlich nicht richtig falteten oder nahezu identisch mit bekannten natürlichen Enzymen waren, sodass 105 verschiedene Kandidaten für experimentelle Tests in Bakterien übrigblieben.
Von Computerdesigns zu funktionierenden Katalysatoren
Als diese 105 KI‑entworfenen TrpB‑Enzyme in E. coli hergestellt wurden, falteten sich viele gut und lagen in hoher Menge vor. Dutzende konnten ihre Hauptaufgabe erfüllen: Indol und die natürliche Partneraminosäure Serin zu Tryptophan umzusetzen. Einige arbeiteten robust sogar bei erhöhten Temperaturen, obwohl keine explizite Wärme‑Resistenz entworfen worden war. In Gegenüberstellungen erreichte ein Teil der GenSLM‑TrpBs die Leistung oder übertraf ein Referenzenzym, das über Jahre mühseliger Evolution im Labor so optimiert worden war, dass es eigenständig bei 75 °C funktioniert. Ein besonders herausragendes Design mit der Bezeichnung 230 produzierte mehr Tryptophan als diese industriell eingesetzte Referenz sowohl bei Raumtemperatur als auch bei hoher Temperatur und zeigte damit, dass ein nur auf Sequenzdaten trainiertes Modell direkt Spitzenleistungen erreichen kann.
Neue Flexibilität jenseits dessen, was die Natur baute
Das Team forderte die Enzyme anschließend mit einem Panel nicht‑natürlicher Substrate heraus – Indolderivate, ein anderes alkoholähnliches Partnermolekül und eine fluorierte Verbindung, die in der Arzneimittelherstellung verwendet wird. Natürliche TrpB‑Versionen sind in der Regel wählerisch: Sie bevorzugen stark ihre nativen Substrate und zeigen kaum Aktivität gegenüber Alternativen. Bemerkenswerterweise waren die KI‑generierten Enzyme oft experimentierfreudiger. Für jedes getestete nicht‑natürliche Substrat zeigte mindestens ein GenSLM‑Design messbare Aktivität, und viele schnitten besser ab als natürliche Enzyme. Wieder hob sich Variante 230 hervor, die alle sieben alternativen Substrate mit Ausbeuten von mäßig bis nahezu vollständig umsetzte – eine Breite an »Promiskuität«, wie man sie in dieser Enzymfamilie zuvor nicht gesehen hatte. Verglichen mit ihrem nächsten natürlichen Verwandten – die sich nur an 78 von 400 Aminosäurepositionen unterschieden – fehlte diesem natürlichen Enzym diese Vielseitigkeit, obwohl Struktur und wichtige Reste des aktiven Zentrums nahezu identisch waren.
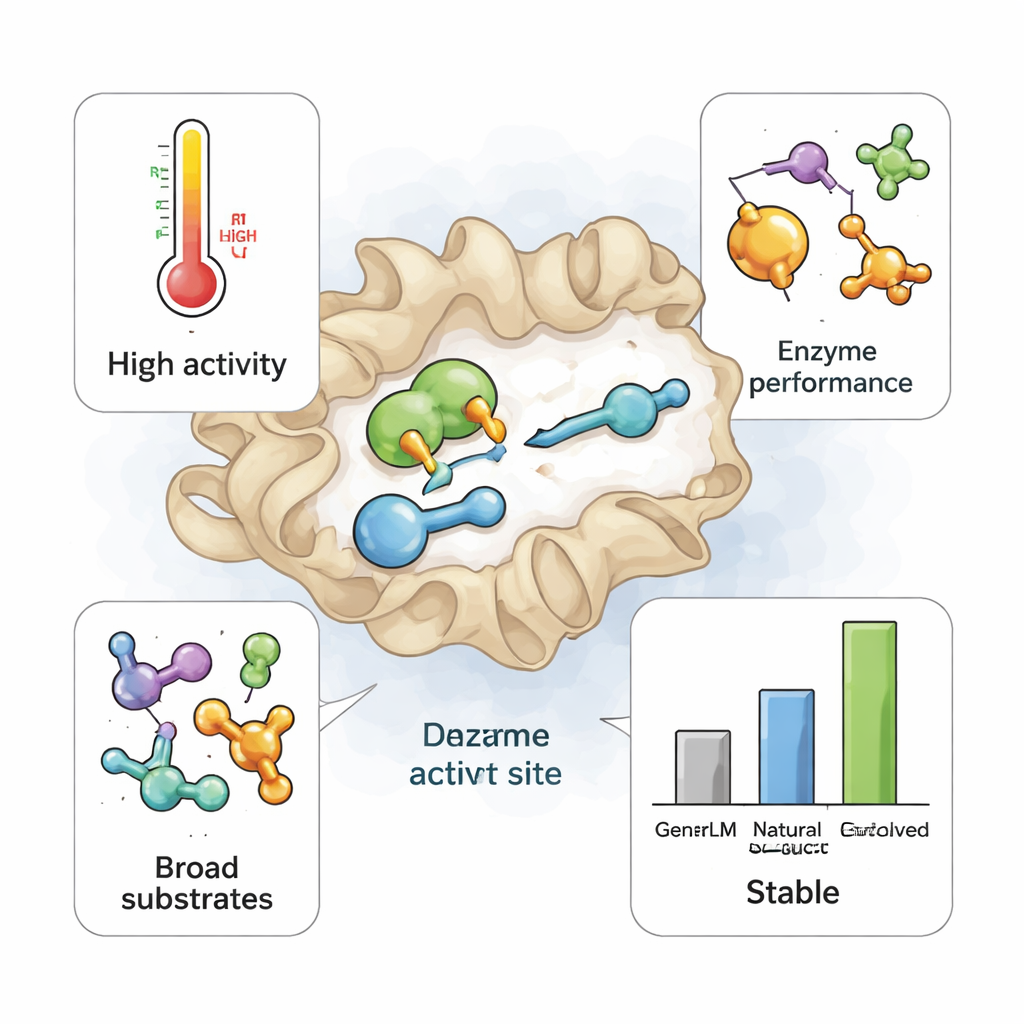
Was das für die grüne Chemie der Zukunft bedeutet
Für nicht‑Fachleute ist die Kernbotschaft: Ein KI‑Modell, das nur auf bestehenden DNA‑Sequenzen trainiert wurde, kann realistische neue Enzyme erfinden, die die Natur nie ausprobiert hat, von denen einige bessere Werkzeuge für die Chemie sind als die derzeit verwendeten. Diese KI‑entworfenen TrpB‑Varianten behalten die wesentliche Form und Funktion ihrer natürlichen Verwandten bei, gewinnen aber eine ungewöhnliche Fähigkeit, viele verschiedene Ausgangsstoffe zu verarbeiten. Diese Flexibilität könnte den Laboraufwand zur Entdeckung enzymatischer Wege zu neuen Arzneimitteln und anderen Produkten drastisch reduzieren. Wenn Design, DNA‑Synthese und Tests schneller und billiger werden, könnten ähnliche generative Modelle die Enzymentdeckung von einer langsamen Schatzsuche in eine schnelle, routinemäßige Designaufgabe verwandeln und dazu beitragen, mehr industrielle Chemie auf sauberere, enzymgetriebene Prozesse umzustellen.
Zitation: Lambert, T., Tavakoli, A., Dharuman, G. et al. Sequence-based generative AI design of versatile tryptophan synthases. Nat Commun 17, 1680 (2026). https://doi.org/10.1038/s41467-026-68384-6
Schlüsselwörter: Enzym‑Engineering, generative KI, Protein‑Design, Tryptophan‑Synthase, Biokatalyse