Clear Sky Science · de
Tmem110 reguliert die Konformation von TRPML1, um endolysosomale Homöostase aufrechtzuerhalten und die Freisetzung mitochondrialer DNA sowie pathologische Selbst‑DNA‑Verarbeitung zu verhindern
Warum ausgelaufene DNA nach Verletzung wichtig ist
Wenn wir schwere Traumata erleiden, etwa einen heftigen Schlag auf den Kopf, beschränkt sich der Schaden nicht auf die Verletzungsstelle. Viele Patienten entwickeln eine gefährliche Allgemeinreaktion, bei der Lunge, Leber, Nieren und andere Organe zu versagen beginnen. Diese Studie zeigt, wie winzige Strukturen innerhalb von Zellen—Lysosomen, Mitochondrien und Immunsensoren—miteinander kommunizieren, um zu entscheiden, ob der Körper die Trümmer leise beseitigt oder in eine selbstgerichtete Immunantwort abrutscht. Das Verständnis dieses verborgenen Aufräumsystems könnte neue Wege eröffnen, Organversagen nach Trauma zu verhindern und Autoimmun‑ sowie Entzündungskrankheiten zu behandeln.
Von der Kopfverletzung zur Krisenlage im ganzen Körper
Eine traumatische Hirnverletzung (TBI) kann einen heftigen Entzündungssturm auslösen, das sogenannte multiple Organfunktionsversagen (MODS), doch es war unklar, wie sich der Schaden vom Gehirn auf entfernte Organe ausbreitet. Die Autorinnen und Autoren konzentrieren sich auf Monozyten und Makrophagen, Immunzellen, die Blut und Gewebe durchstreifen und als professionelle Müllabfuhr fungieren. Nach einer TBI sterben Zellen unkontrolliert ab und setzen ganze Mitochondrien—kleine Energiefabriken mit eigener DNA—ins Blut frei. Diese mitochondriale DNA (mtDNA) ähnelt bakterieller DNA und kann starke antivirale Abwehrreaktionen auslösen, wenn sie nicht schnell entfernt wird. Normalerweise nehmen Zellen diese fremden Mitochondrien in saure Kompartimente auf, die Lysosomen genannt werden, wo Enzyme die DNA abbauen, bevor sie ins Zellplasma entweichen kann. 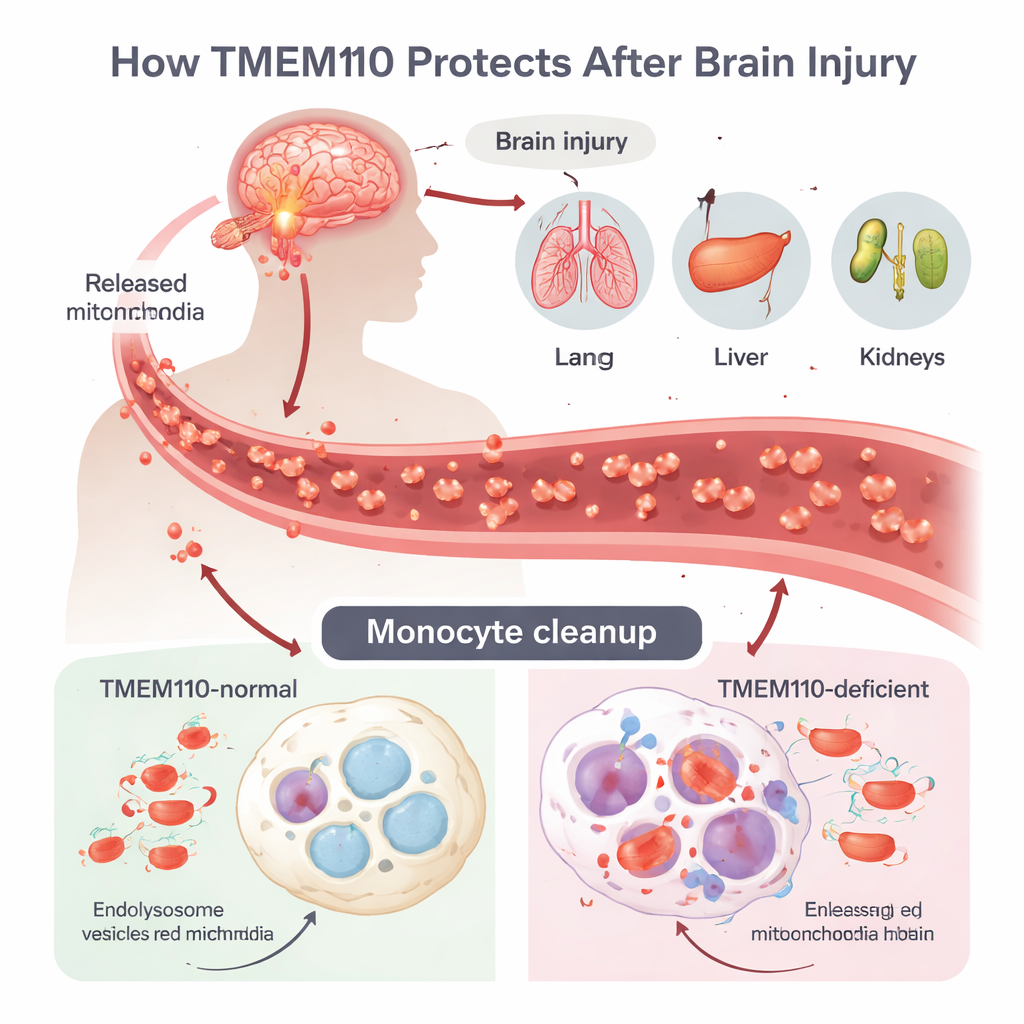
Ein Wächterprotein, das Lysosomen stabil hält
Das Team identifizierte TMEM110, ein Protein, das die Membran des endoplasmatischen Retikulums (ein wichtiges intrazelluläres Membrannetzwerk) durchspannt, als entscheidenden Wächter in diesem Prozess. Mithilfe genetisch veränderter Mäuse, die TMEM110 nur in Monozyten und Makrophagen nicht exprimierten, entwickelten die Forschenden ein kontrolliertes Hirnverletzungsmodell. Im Vergleich zu normalen Mäusen entwickelten TMEM110‑defiziente Tiere deutlich höhere Spiegel von Typ‑I‑Interferonen—starke antivirale Botenstoffe—in Blut und Hirnwasser. Lunge, Leber, Nieren und Lymphknoten zeigten schwerere Schäden und das Langzeitüberleben nach TBI war deutlich eingeschränkt. Als die Forschenden den Rezeptor für Typ‑I‑Interferone blockierten oder das mutierte Knochenmark durch normales ersetzten, gingen Organverletzungen und Sterblichkeit deutlich zurück, was zeigt, dass übermäßige Interferon‑Signale aus peripheren Monozyten ein wesentlicher Treiber von MODS in diesem Modell sind.
Wie fehlerhafte Ionensteuerung DNA entweichen lässt
Im Inneren dieser Immunzellen fanden die Autorinnen und Autoren heraus, dass TMEM110‑defiziente Lysosomen chemisch aus dem Gleichgewicht geraten waren: Sie waren weniger sauer und mit Kalzium überladen. Unter diesen Bedingungen verlor die Enzymaktivität von DNase II—die normalerweise DNA in Lysosomen zerschneidet—an Wirksamkeit, Lysosomenmembranen wurden fragil und mtDNA entwich ins umgebende Zytosol. Laborexperimente mit humanen Monozyten, die markierte Fremdmitochondrien aufnahmen, bestätigten, dass ohne TMEM110 mehr mtDNA in das Zellplasma gelangte und eine Welle interferon‑stimulierter Gene auslöste. Die Studie zeigt, dass TMEM110 wirkt, indem es ein anderes Protein kontrolliert: den lysosomalen Ionenkanal TRPML1. Wenn TMEM110 vorhanden ist, steht es in physischem Kontakt mit TRPML1 und verschiebt diesen in eine „offene“ Konformation, die winzige Kalzium‑Freisetzungshotspots an der Lysosomenoberfläche erzeugt. Diese kontrollierten Kalziumabflüsse tragen dazu bei, den richtigen Säuregrad zu erhalten, Membranreparatur zu unterstützen und mtDNA im Inneren gefangen zu halten und zu degradieren. 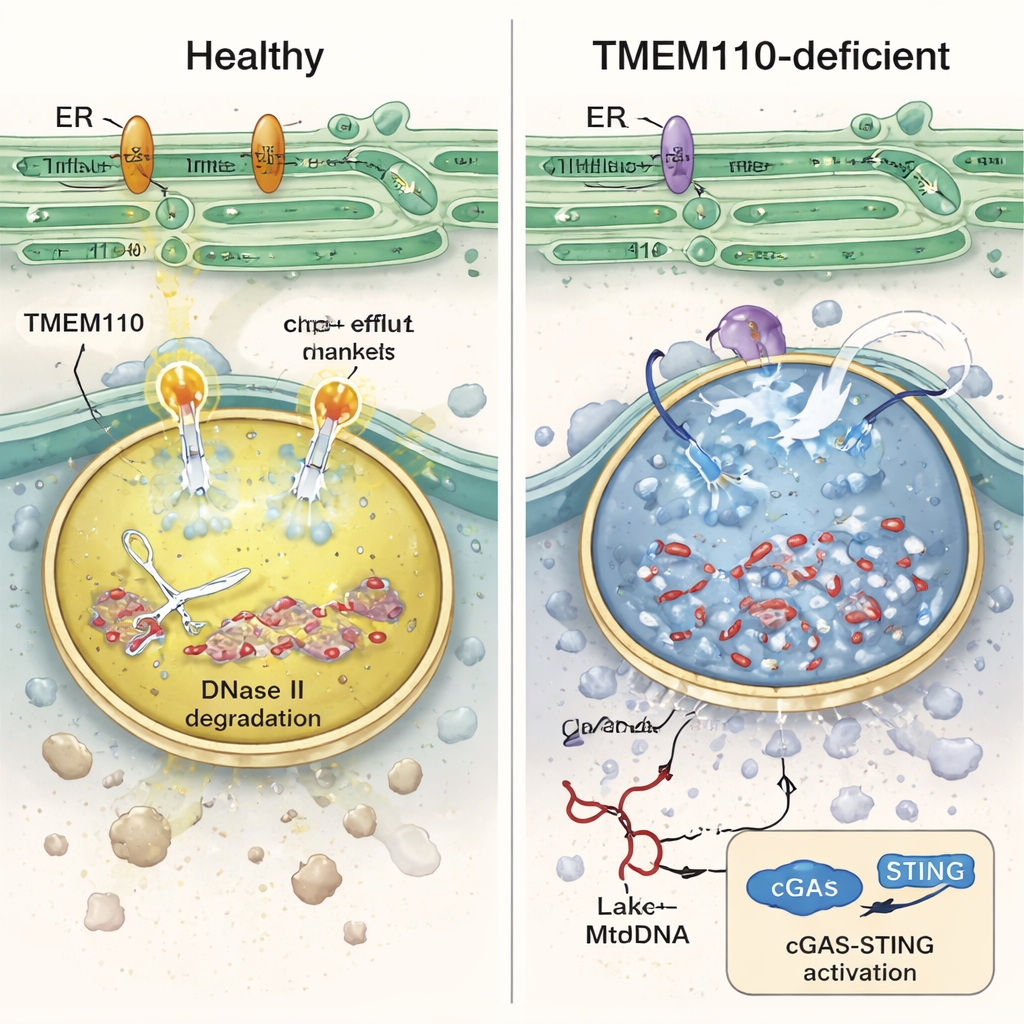
Eine Rückkopplungsschleife mit dem DNA‑Alarmsystem der Zelle
Sobald mtDNA ins Zytosol gelangt, wird sie vom cGAS–STING‑Signalweg erkannt, dem wichtigsten Alarmmechanismus der Zelle für fremde DNA. Interessanterweise bindet TMEM110 auch im Ruhezustand an STING und hält es im endoplasmatischen Retikulum zurück, um unnötige Alarme zu verhindern. Wenn sich zytosolische DNA ansammelt, wird STING aktiviert und lockert seine Bindung an TMEM110. Das wiederum legt eine andere Region von TMEM110 frei, die TRPML1 anbindet und den lysosomalen Kalziumefflux verstärkt, wodurch eine Rückkopplung entsteht: Das Erkennen von Selbst‑DNA aktiviert einen Mechanismus, der die DNA‑Beseitigung fördert. Krankheitsassoziierte STING‑Mutationen, die bei menschlichen autoinflammatorischen Syndrome gefunden wurden, stören diesen Übergang, halten TMEM110 in einem inhibierten Zustand gefangen und tragen so zu chronischer Interferonaktivierung bei. In Mäusen mit einer solchen STING‑Mutation führte TBI zu stärkeren Organschäden und höherer Sterblichkeit, aber die Verabreichung eines kleinen TMEM110‑Fragments in Lysosomen mittels einer mRNA–Lipid‑Nanopartikeltherapie stellte die Kontrolle über mtDNA teilweise wieder her und verbesserte das Überleben.
Hinweise aus Patienten und Wege zu neuen Therapien
Die Autorinnen und Autoren untersuchten anschließend eine klinische Kohorte von 143 Personen mit trauma‑bedingter Hirnverletzung und MODS. Patienten, deren Monozyten früh nach der Verletzung höhere TMEM110‑Spiegel aufwiesen, hatten eine größere Wahrscheinlichkeit, die Organfunktion wiederzuerlangen und zu überleben. Bei Patienten mit niedrigerem TMEM110 fanden sich mehr zirkulierende mtDNA und dezellulierte Mitochondrien, stärkere Interferonantworten, höhere Scores für Organversagen und breitere Autoantikörperprofile, einschließlich Antikörper gegen DNA und nukleäre Proteine. Diese Muster spiegelten die Befunde bei Mäusen eng wider und stützen die Idee, dass die TMEM110‑gesteuerte Kontrolle der lysosomalen Stabilität und der mtDNA‑Entsorgung ein gemeinsamer Mechanismus bei menschlichen Erkrankungen ist.
Was das für Patienten mit schweren Traumata bedeutet
Vereinfacht gesagt legt diese Arbeit nahe, dass unser Immunsystem nach einer schweren Verletzung vor einer heiklen Wahl steht: die Flut selbstfreigesetzter DNA aus sterbenden Zellen geräuschlos verdauen oder sie als viralen Angriff deuten und eine umfassende Abwehr auslösen, die die eigenen Organe schädigen kann. TMEM110 hilft, indem es einen lysosomalen Ionenkanal abstimmt und mit dem DNA‑Sensor STING koordiniert, sodass die Zellen den sicheren Weg wählen. Versagt dieses System—weil TMEM110 fehlt, STING mutiert ist oder Lysosomen überlastet sind—entweicht mtDNA, der Alarm bleibt aktiviert und es folgt Multiorganschaden. Die gezielte Beeinflussung dieser TMEM110–TRPML1–STING‑Achse, etwa durch lysosomengerichtete mRNA‑Therapien, könnte einen neuen Ansatz bieten, Organversagen und autoimmunartige Komplikationen nach schweren Traumata zu verhindern oder zu behandeln.
Zitation: Feng, Z., Pan, Y., Zhou, J. et al. Tmem110 regulates the conformation of TRPML1 to maintain endolysosomal homeostasis and prevent mitochondrial DNA leakage and pathological self-DNA processing. Nat Commun 17, 1678 (2026). https://doi.org/10.1038/s41467-026-68382-8
Schlüsselwörter: traumatische Hirnverletzung, mitochondriale DNA, Lysosomen, Typ‑I‑Interferon, cGAS‑STING‑Signalweg