Clear Sky Science · de
Versican-Expression von Lungenfibroblasten unterdrückt Lungenfibrose
Warum Lungenvernarbung eine stärkere Bremse braucht
Die idiopathische Lungenfibrose ist eine unerbittliche Lungenerkrankung, bei der normale Heilung in ungehemmte Vernarbung umschlägt und den Betroffenen nach und nach die Atemkraft raubt. Diese Studie enthüllt ein überraschendes natürliches „Bremssystem“ in der Lunge: ein großes zuckerbeschichtetes Molekül namens Versican, das von Bindegewebszellen, den Fibroblasten, produziert wird. Statt Schaden anzutreiben, hilft Fibroblasten-abhängiges Versican, die Narbenbildung in Schach zu halten, verändert damit unser Verständnis von Vernarbung und deutet auf neue Behandlungsansätze für diese ansonsten schwer therapierbare Erkrankung hin.
Eine tödliche Reparatur, die schiefgeht
In gesunden Lungen stützt ein feines Geflecht aus Proteinen und Zuckern – die extrazelluläre Matrix – die winzigen Lungenbläschen, in denen der Gasaustausch stattfindet. Nach einer Verletzung eilen Fibroblasten herbei, bauen neue Matrix auf und schalten dann wieder herunter. Bei der idiopathischen Lungenfibrose schaltet dieses Reparaturprogramm nie richtig ab. Fibroblasten häufen sich, weben dichte Kollagenskelette und verhärten das Lungengewebe, sodass das Atmen sich anfühlt, als würde man einen mit Zement gefüllten Gummiball aufblasen. Die Autorinnen und Autoren wollten verstehen, wie eine bestimmte Matrixkomponente, Versican, in diese Geschichte passt, denn sie ist in erkrankten Lungen reichlich vorhanden, ihre Rolle aber rätselhaft.
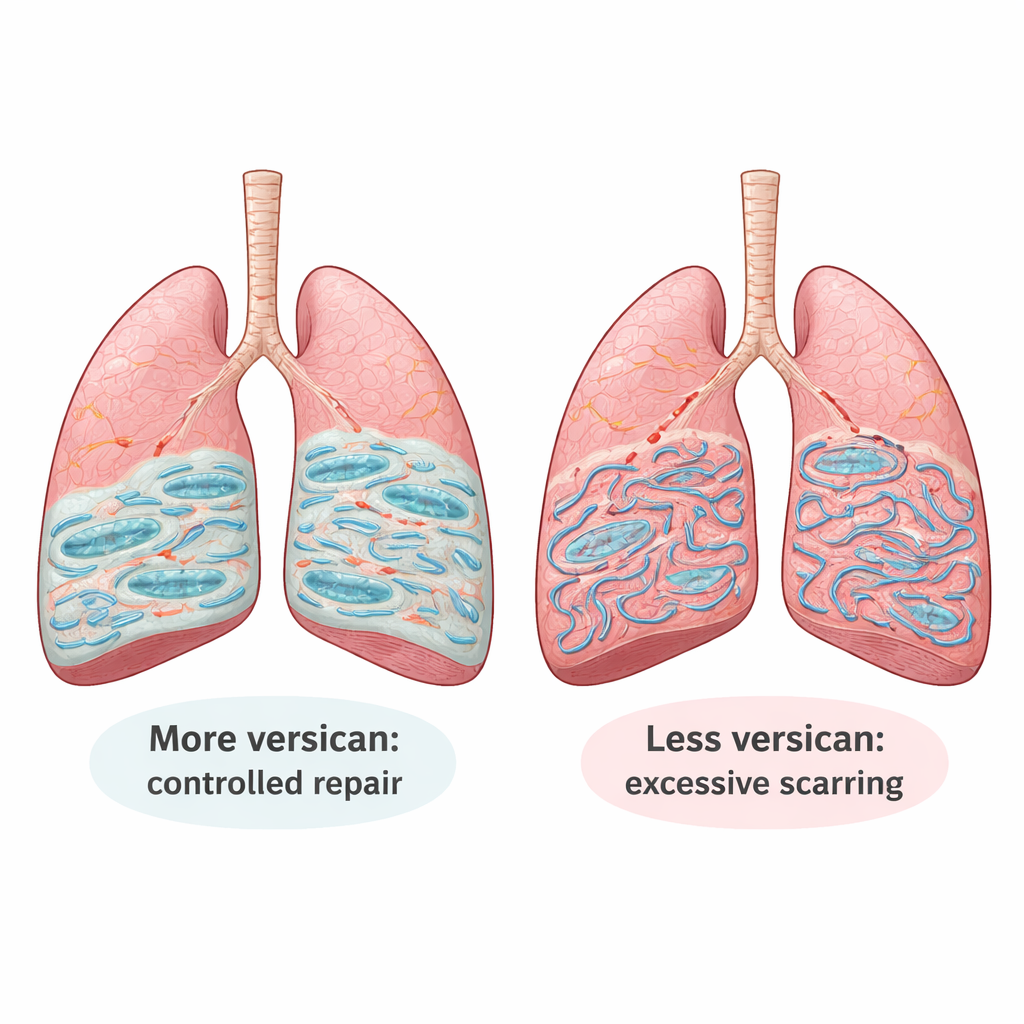
Ein schützender Mantel um Lungenzellen
Durch die Auswertung großer Gen-Datenbanken von Patientinnen und Patienten und die Untersuchung von Lungenbiopsien fanden die Forschenden heraus, dass die Versican-Spiegel in fibrotischen Lungen konstant erhöht sind und besonders in Fibroblasten sowie in bestimmten Immunzellen zunehmen. In einem weit verbreiteten Mausmodell der Lungenfibrose zeigte sich dasselbe Muster: Nach einer Verletzung stieg die Versican-Produktion an, wenn die Vernarbung ihren Höhepunkt erreichte, und fiel dann wieder, als sich die Lunge zu erholen begann. In Zellkulturen reagierten normale Lungenfibroblasten auf ein starkes Vernarbungssignal (den Wachstumsfaktor TGF-β) oder auf eine bereits vernarbte Matrix, indem sie mehr Versican produzierten – was nahelegt, dass Versican Teil der eingebauten Reaktion der Lunge auf eine starre, kollagenreiche Umgebung ist.
Wenn die Bremse nachlässt, wird die Vernarbung schlimmer
Um zu prüfen, ob Versican Freund oder Feind ist, nutzte das Team Mäuse, die nur etwa die Hälfte der normalen Versican-Menge produzieren. Im Gegensatz zu dem, was die hohen Werte bei Erkrankung vermuten lassen, schnitten diese „Versican-armen“ Mäuse nach Lungenverletzung schlechter ab. Sie verloren mehr Gewicht, sammelten mehr Flüssigkeit und lösliches Kollagen in den Lufträumen an und entwickelten dickere, steifere Lungen, die länger zur Erholung brauchten. Detaillierte Bildgebung zeigte stärkere Kollagenablagerungen und eine verzerrtere Gewebestruktur. Messungen an Lungenschnitten mit der Rasterkraftmikroskopie bestätigten, dass das vernarbte Gewebe dieser Mäuse mechanisch steifer war – ein zentraler Treiber anhaltender Fibroblastenaktivierung.
Wie eine gelockerte Matrix zur Schnellstraße für Invasion wird
Tiefergehend untersuchten die Wissenschaftlerinnen und Wissenschaftler, wie Versican das physische Gerüst der Lunge formt. In zellfreien Tests verlangsamte Zugabe von Versican das enge Zusammenpacken von Kollagenfasern, während eine Verringerung von Versican es Kollagen erlaubte, sich zu dickeren, stärker verflochtenen Bündeln zusammenzusetzen. In lebendem Gewebe und in von Fibroblasten im Labor gebildeter Matrix bedeutete weniger Versican nicht nur mehr und dickeres Kollagen, sondern auch vermehrte andere Matrixkomponenten wie Tenascin-C und Hyaluronan sowie mehr Quervernetzungen, die Fasern in starre Netzwerke einklinken. Fibroblasten, die auf dieser veränderten Matrix saßen, schalteten in einen hochinvasiven Modus um und bildeten viele kleine, enzymreiche „Podosome“, die das umliegende Material abtragen und den Zellen ein tieferes Eindringen ermöglichen. Die Blockade wichtiger Rezeptoren für Kollagen und Tenascin-C verringerte dieses invasive Verhalten und verband die strukturellen Änderungen direkt mit zellulären Aktionen.
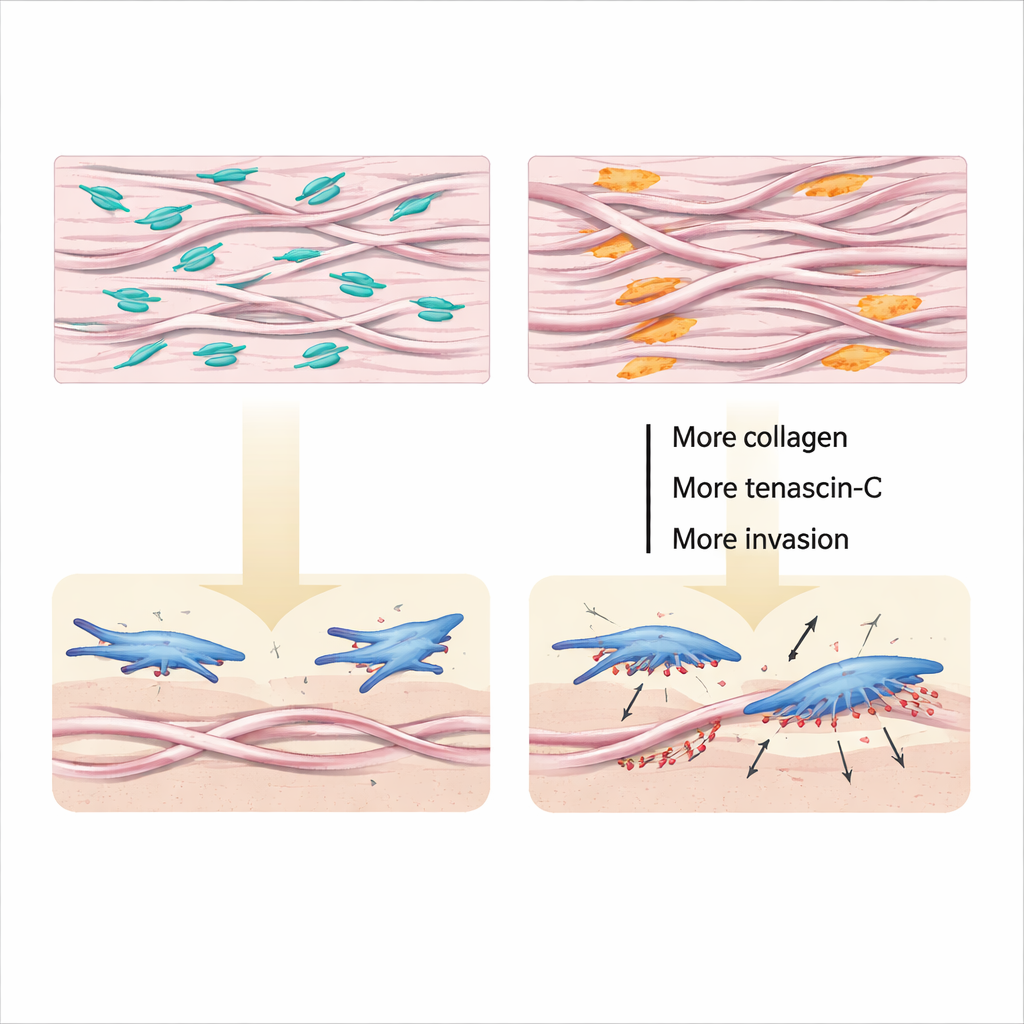
Ein zweischneidiges Molekül mit Potenzial
Aus diesen Experimenten entsteht ein klares Bild: Von Lungenfibroblasten gebildetes Versican wirkt als innerer Bremsmechanismus gegen Vernarbung. Wenn Verletzung und Wachstumsfaktoren die Kollagenproduktion antreiben, reagieren Fibroblasten, indem sie Versican erhöhen, das verhindert, dass Kollagenfasern zu dick und verfilzt werden, dämpft übermäßige Versteifung und hemmt die Bildung invasiver Podosome. Fallen die Versican-Spiegel, schießen Kollagen und Tenascin-C in die Höhe, die Matrix verhärtet und verknäult, Fibroblasten werden invasiver, und die Fibrose verschlimmert sich und bleibt bestehen. Da andere Zelltypen, etwa Immunzellen, Versican möglicherweise anders nutzen, bleibt es ein „zweischneidiges Schwert“, doch zeigt diese Arbeit, dass ein gezieltes Verstärken oder Nachahmen der fibroblastenspezifischen Versican-Wirkung ein vielversprechender neuer Weg sein könnte, Lungenvernarbung zu verlangsamen oder sogar umzukehren.
Zitation: Kanellopoulou, P., Barbayianni, I., Fanidis, D. et al. Versican expression from lung fibroblasts suppresses pulmonary fibrosis. Nat Commun 17, 1676 (2026). https://doi.org/10.1038/s41467-026-68377-5
Schlüsselwörter: idiopathische Lungenfibrose, extrazelluläre Matrix, Versican, Lungenfibroblasten, Gewebenarben