Clear Sky Science · de
Cryo‑EM‑Struktur des menschlichen COP1‑DET1‑Ubiquitin‑Ligase‑Komplexes
Wie Zellen entscheiden, welche Proteine abgebaut werden
In jeder Zelle müssen Tausende von Proteinen ständig neu gebaut, umgebaut oder zum richtigen Zeitpunkt entfernt werden. Diese Studie untersucht eine der wichtigsten Qualitätskontroll‑Maschinen der Zelle, einen molekularen Schredder, der darüber entscheidet, wann potente Genregulatoren, die mit Krebs und Entwicklung verknüpft sind, entfernt werden. Indem die Autoren seine dreidimensionale Struktur bis auf nahezu atomare Details auflösen, zeigen sie, wie diese Maschine zwischen einem inaktiven, geschichteten Zustand und einer aktiven, Substrat‑verarbeitenden Form umschalten kann — ein Einblick, der langfristig helfen könnte, Wirkstoffe zu entwickeln, die sie an- oder abschalten.
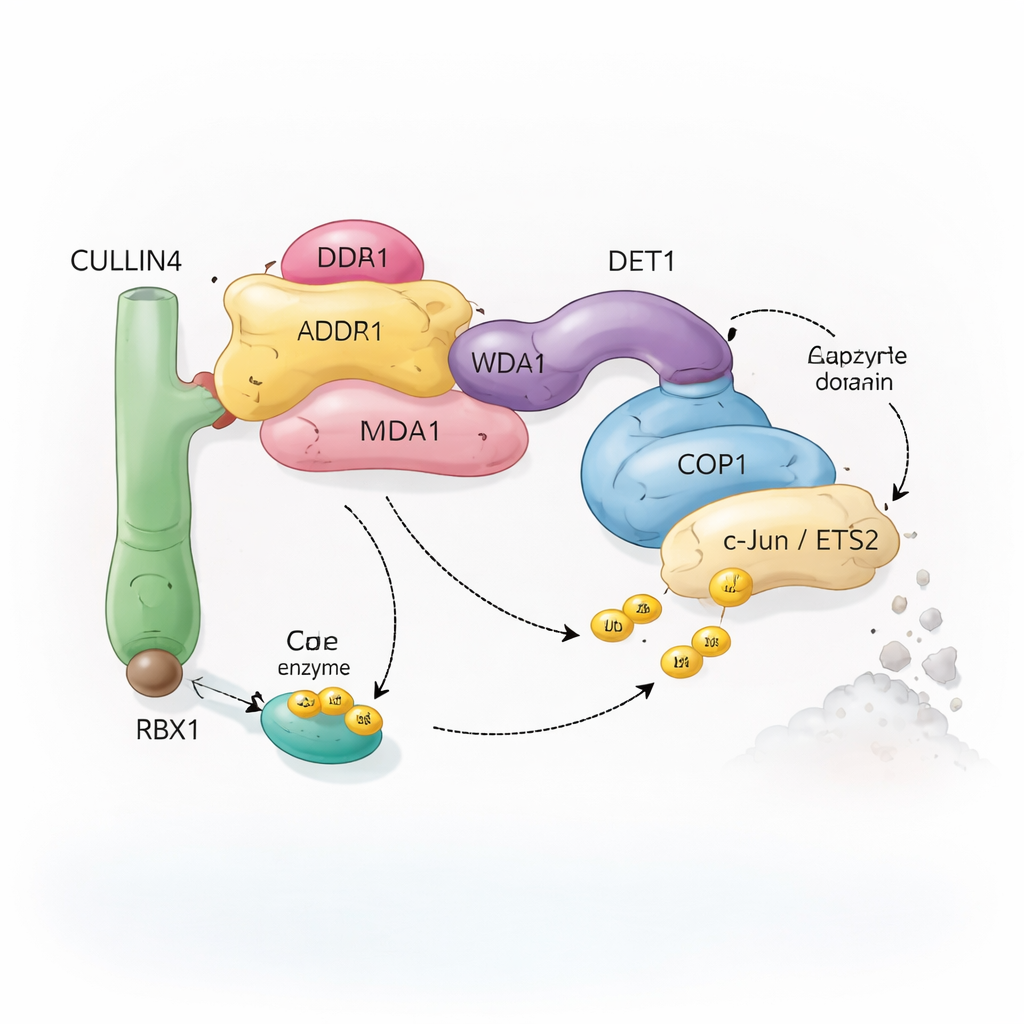
Eine molekulare Recycling‑Crew mit vielen Teilen
Zellen verlassen sich auf ein System namens Ubiquitinierung, um Proteine zur Wiederverwertung zu markieren. Kleine Ubiquitin‑Moleküle wirken wie abnehmbare Fähnchen, die der Zelle signalisieren, ob ein Protein verändert, umgelagert oder zerstört werden soll. Spezielle Enzymkomplexe, sogenannte Ubiquitin‑Ligasen, befestigen diese Markierungen an ausgewählten Zielen. Der hier untersuchte Komplex zentriert sich auf COP1, ein Protein, das von Pflanzen bis zum Menschen vorkommt und wichtige Transkriptionsfaktoren markiert — Proteine, die steuern, welche Gene an- oder abgeschaltet werden. COP1 arbeitet nicht allein: Es kann sich in eine größere Anordnung einfügen, die um das Gerüstprotein CULLIN4 aufgebaut ist und mehrere Adapter wie DDB1, DDA1 und DET1 umfasst. Zusammen bilden diese Komponenten eine flexible „Recycling‑Crew“, die spezifische Transkriptionsfaktoren wie c‑Jun und ETS2 erkennt, von denen viele an Zellwachstum und Krebs beteiligt sind.
Den Komplex in 3D erfassen
Um zu verstehen, wie diese Crew arbeitet, nutzten die Forscher Einzelpartikel‑Cryo‑Elektronenmikroskopie, eine Technik, die blitzgefrorene Proteine abbildet und ihre Formen in hoher Auflösung rekonstruiert. Sie rekonstruierten das menschliche COP1–DET1‑System in kultivierten Zellen, reinigten die Komplexe und visualisierten mehrere unterschiedliche Strukturzustände. Zunächst lösten sie die Struktur des DDB1–DDA1–DET1‑Modules, das als zentrales Hub fungiert. DET1 nimmt eine ungewöhnliche, teilweise flexible Form an statt einer starren Scheibe, mit einer herausragenden „Klaue“, die Partnerenzyme greifen kann. Durch Zugabe von COP1 und einer Klasse von Helferenzymen, den sogenannten E2s, erfassten sie anschließend größere Assemblies, die zeigen, wie alle Teile zusammenpassen und sowohl kompakte Stapel als auch offenere dimerische (zwei‑COP1) Anordnungen offenbaren.
Ein inaktiver Stapel und ein aktives Dimer
Einer der auffälligsten Befunde ist eine geschichtete, filamentartige Struktur aus wiederholten Lagen des Komplexes. In jeder Lage verweben sich acht COP1‑Moleküle über ihre Coiled‑Coil‑Segmente und bilden einen diamantförmigen Ring. Ihre Substraterkennungsregionen, die WD40‑Domänen, zeigen alle in die gleiche Richtung und sind teilweise durch benachbarte Lagen abgeschirmt. Diese enge Packung repräsentiert wahrscheinlich einen „ausgeschalteten“ Zustand, in dem der Zugang für Zielproteine begrenzt ist. Im Gegensatz dazu sah das Team bei Komplexen, die zusammen mit COP1‑Substraten wie c‑Jun oder ETS2 exprimiert wurden, eine andere, dimerische Form: zwei COP1‑Moleküle nebeneinander, mit ihren WD40‑Domänen nach außen gerichtet und verfügbar, um an kurze „VP“‑Motife in vielen Transkriptionsfaktoren zu binden. Biochemische Tests bestätigten, dass nur dieser dimerische Zustand effizient den Aufbau langer Ubiquitin‑Ketten auf c‑Jun unterstützt.
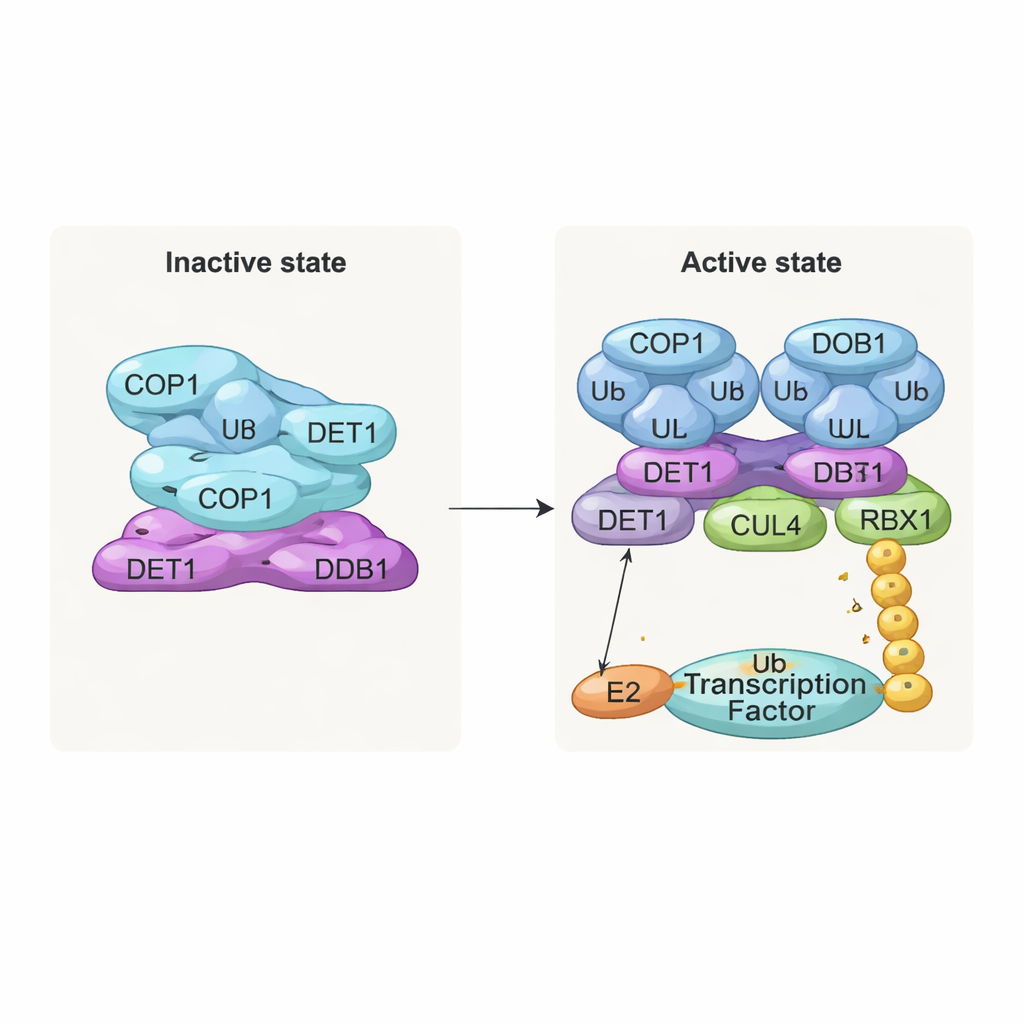
DET1 als flexibler Brückenbauer und Verkehrsdirigent
DET1 tritt als Schlüsselorchestrator hervor, der alle Teile der Maschine verbindet. Sein N‑terminaler Bereich schmiegt sich in DDB1 ein und verankert den Komplex am CULLIN4‑Gerüst, während seine Klauenregion eine Familie von E2‑Enzymen namens Ube2e umschließt. Detaillierte Mutationsversuche zeigen, dass DET1 — und nicht COP1 — diese E2s direkt greift und sie nahe an die katalytische RING‑Region von COP1 positioniert. In dieser Anordnung scheint Ube2e zu helfen, die allerersten Ubiquitin‑Marken auf das Substrat zu setzen. Ein zweites E2‑Enzym, Ube2d3, wird dann über den CULLIN4–RBX1‑Arm rekrutiert, um diese Markierungen zu längeren Ketten zu verlängern, die den vollständigen Abbau signalisieren. Anders gesagt, wirkt DET1 als flexible Brücke, die ein E2 an COP1 präsentiert, während das größere Gerüst ein zweites E2 zur Fertigstellung der Aufgabe heranführt.
Warum das für Gesundheit und Krankheit wichtig ist
Indem die Studie diese Strukturzustände und ihre Aktivitäten kartiert, erklärt sie, wie derselbe Proteinsatz zwischen einer ruhenden, geschichteten Form und einem aktiven Dimer wechseln kann, das Transkriptionsfaktoren zur Zerstörung bestimmt. Dieser Schalter ist besonders wichtig für Faktoren wie c‑Jun, die die Zellteilung antreiben und bei Fehlregulation eng mit Krebs verbunden sind. Zu verstehen, wie COP1 und DET1 zusammenarbeiten — wie DET1s Klaue spezifische E2‑Enzyme auswählt, wie COP1s WD40‑Oberfläche VP‑haltige Substrate erkennt und wie sich das aktive Dimer bildet — liefert einen Bauplan für künftige Arbeiten. Langfristig könnten Wirkstoffe, die den inaktiven Stapel stabilisieren oder das aktive Dimer begünstigen, Forschern neue Wege eröffnen, Gensteuerungs‑Wege bei Krebs und anderen Erkrankungen, bei denen der Proteinabbau aus dem Gleichgewicht geraten ist, gezielt zu modulieren.
Zitation: Wang, S., Teng, F., Stjepanovic, G. et al. Cryo-EM structure of the human COP1-DET1 ubiquitin ligase complex. Nat Commun 17, 543 (2026). https://doi.org/10.1038/s41467-026-68375-7
Schlüsselwörter: Ubiquitin‑Ligase, COP1, Proteinabbau, Cryo‑EM‑Struktur, c‑Jun