Clear Sky Science · de
INCENP und CDCA8 sagen das Ansprechen auf neoadjuvante Chemotherapie und die Ergebnisse beim Plattenepithelkarzinom der Speiseröhre vorher
Warum diese Forschung für Krebspatienten wichtig ist
Viele Menschen mit Tumoren der Speiseröhre, der Brust oder der Lunge erhalten vor einer Operation intensive Chemotherapie, um die Tumoren zu verkleinern. Nur etwa die Hälfte dieser Patienten profitiert jedoch wirklich; für die übrigen verursachen die Medikamente Nebenwirkungen, ohne das Tumorwachstum aufzuhalten. Diese Studie stellt eine einfache, aber entscheidende Frage: Kann man im Voraus vorhersagen, wer auf die Chemotherapie anspricht, und lässt sich die Behandlung für diejenigen verbessern, die derzeit nicht ansprechen?
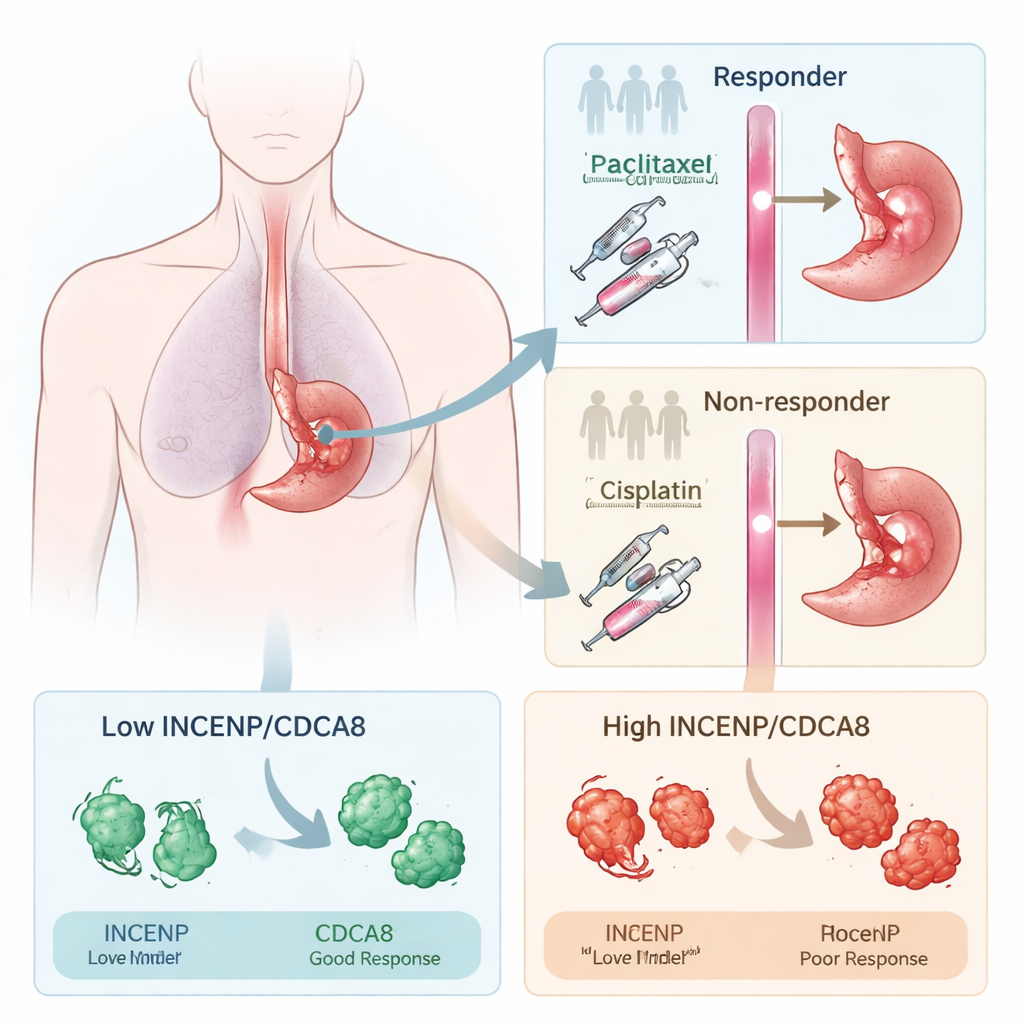
Erkennen, wer auf die Behandlung anspricht
Die Forschenden konzentrierten sich auf ein standardmäßiges präoperatives Regime aus Paclitaxel und Cisplatin, das in mehreren Krebsarten weit verbreitet ist. Zunächst verglichen sie bei Patientinnen und Patienten mit Plattenepithelkarzinom der Speiseröhre Tumorproben von Personen, deren Tumoren nach dieser Therapie stark zurückgingen (Responder), mit Proben von solchen, deren Tumoren kaum reagierten (Non-Responder). Durch die Analyse hoch- und herunterregulierter Gene zeigte sich, dass viele Unterschiede mit der Zellteilung zusammenhängen — ein Prozess, auf den Chemotherapie abzielt. Zwei Proteine, die die Chromosomentrennung während der Zellteilung steuern, INCENP und CDCA8, fielen wiederholt dadurch auf, dass sie in therapieresistenten Tumoren deutlich stärker exprimiert waren.
Zwei Proteine, die wahrscheinliche Resistenz signalisieren
Um zu prüfen, ob INCENP und CDCA8 bloße Begleiterscheinungen oder aktive Treiber der Resistenz sind, veränderte das Team deren Konzentration in im Labor gezüchteten Speiseröhrenkrebszellen. Wenn sie eines der beiden Proteine reduzierten, wurden die Krebszellen deutlich empfindlicher gegenüber Paclitaxel und Cisplatin: Sie bildeten weniger Kolonien und es waren viel geringere Wirkstoffdosen nötig, um sie zu töten. Wurden INCENP oder CDCA8 dagegen überexprimiert, zeigte sich das Gegenteil: Die Medikamente wirkten weniger effektiv. In Mäusen mit implantierten humanen Speiseröhrentumoren führte die Herunterregulierung dieser Proteine dazu, dass die Chemotherapie die Tumoren stärker schrumpfen ließ. Patientinnen und Patienten, deren Tumoren vor der Behandlung hohe INCENP‑ und CDCA8‑Spiegel aufwiesen, hatten zudem häufiger Krankheitsprogression und eine kürzere Überlebenszeit, was ihren Wert als Warnsignale unterstreicht.
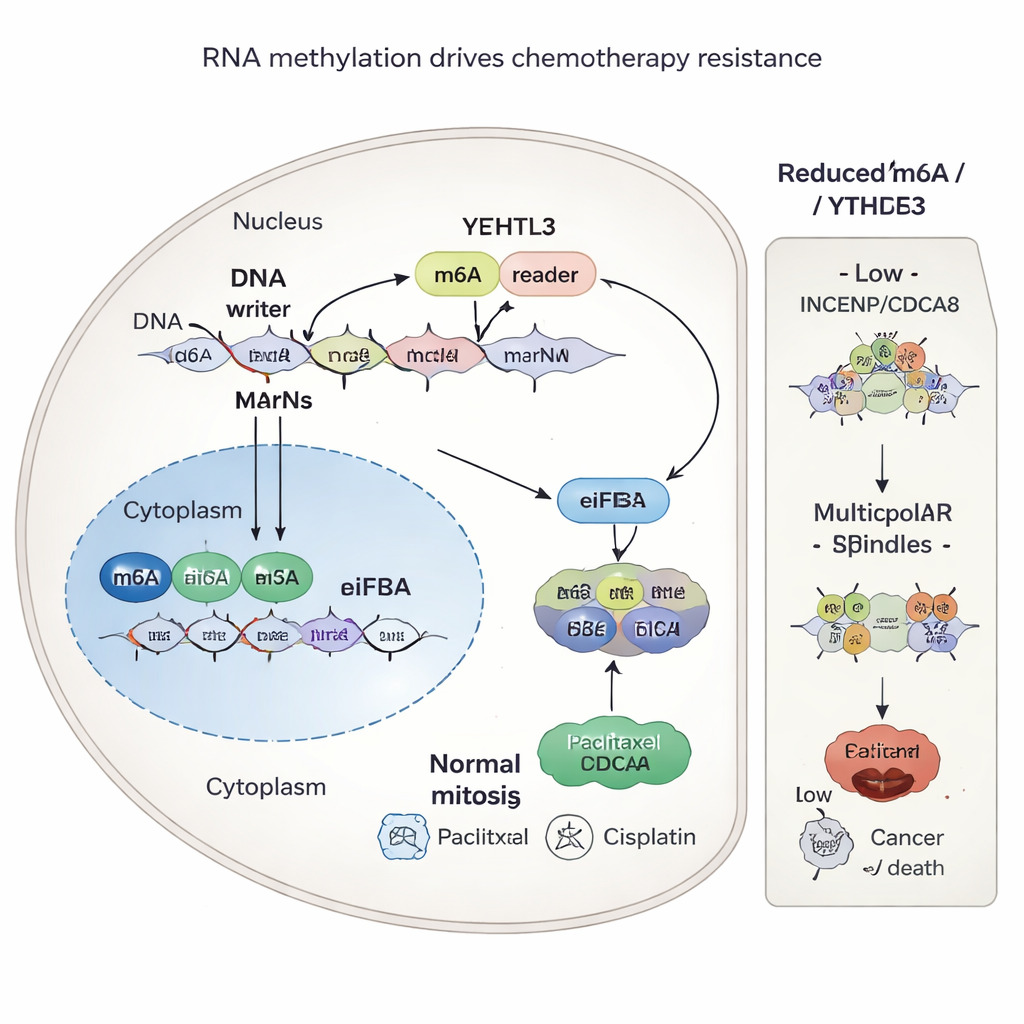
Ein chemischer Marker auf RNA, der die Resistenz antreibt
Die Studie fragte weiter, warum INCENP und CDCA8 in resistenten Tumoren so reichlich vorhanden sind. Die Antwort führte zu einer feinen chemischen Markierung auf RNA namens m6A, die wie ein Stellrad dafür wirkt, wie effizient genetische Botschaften in Protein übersetzt werden. Ein Enzym namens METTL3 fügt diese m6A‑Marken an bestimmten Stellen in den RNA‑Vorlagen für INCENP und CDCA8 hinzu. Ein weiteres Protein, YTHDF3, erkennt diese Markierungen und hilft dabei, die zelluläre Proteinbiosynthese anzuwerben, wodurch die Produktion der beiden Proteine gesteigert wird. Wenn die Forschenden METTL3 oder YTHDF3 reduzierten oder YTHDF3 mit einem kleinen Molekül namens Ebselen blockierten, gingen die m6A‑Marken verloren bzw. wurden ignoriert, die Proteinspiegel von INCENP und CDCA8 fielen und die Krebszellen wurden empfindlicher gegenüber Chemotherapie.
Zellteilung stören, um die Chemotherapie zu verstärken
INCENP und CDCA8 sind Bestandteile eines größeren Komplexes, des Chromosomal Passenger Complex, der dafür sorgt, dass Chromosomen gleichmäßig auf die Tochterzellen verteilt werden. In resistenten Zellen helfen hohe Spiegel dieser Proteine, während der Zellteilung saubere, bipolare Spindeln aufrechtzuerhalten, wodurch der Tumor den Schaden durch Paclitaxel und Cisplatin überlebt. Werden INCENP und CDCA8 unterdrückt, bilden die Zellen häufig fehlerhafte, multipolare Spindeln. Dieses Chaos bei der Chromosomenaufteilung treibt Krebszellen in den Zelltod und verstärkt die tödliche Wirkung der Chemotherapie. Entscheidend war, dass die Schutzwirkung von INCENP und CDCA8 von den spezifischen m6A‑Stellen in ihren RNAs abhängt: Mutationen an diesen Stellen beseitigten die Resistenz.
Über eine Krebsart hinaus
Da Paclitaxel plus Cisplatin auch bei Lungen‑ und Brustkrebs eingesetzt wird, untersuchte das Team auch Biopsien von Patientinnen und Patienten mit diesen Tumoren. In allen drei Krebsarten sprachen Personen, deren Tumoren vor der Therapie niedrige Spiegel von INCENP, CDCA8 und YTHDF3 zeigten, deutlich häufiger gut auf die Behandlung an. Statistische Analysen ergaben, dass die Kombination dieser drei Marker besonders gut dabei hilft, wahrscheinliche Responder von Non‑Respondern zu unterscheiden, was auf ein praxisnahes Testpanel hindeutet, das in mehreren Krebsarten eingesetzt werden könnte.
Was das für Patienten und Ärztinnen und Ärzte bedeutet
Vereinfacht gesagt identifiziert diese Arbeit einen molekularen „Fingerabdruck“, der erklärt, warum manche Tumoren gegenüber starker Chemotherapie unempfindlich sind. Hohe Spiegel von INCENP und CDCA8, angetrieben durch ein m6A‑basiertes Kontrollsystem mit METTL3 und YTHDF3, halten Krebszellen auch unter Wirkstoffangriff in einem ordentlichen Teilungsmodus. Die Messung dieser Proteine in einer Biopsie könnte Ärzten helfen vorherzusagen, ob Paclitaxel plus Cisplatin einem bestimmten Patienten vermutlich nützt, und so anderen eine unwirksame Behandlung ersparen. Gleichzeitig könnten Medikamente, die diesen Signalweg blockieren, mit Standardchemotherapien kombiniert werden, um resistente Tumoren in tödliche Teilungsfehler zu treiben und möglicherweise das Überleben bei mehreren wichtigen Krebsarten zu verbessern.
Zitation: Wang, X., Wang, T., Wang, K. et al. INCENP and CDCA8 predict neoadjuvant chemotherapy response and outcomes in esophageal squamous cell carcinoma. Nat Commun 17, 1672 (2026). https://doi.org/10.1038/s41467-026-68371-x
Schlüsselwörter: neoadjuvante Chemotherapie, Plattenepithelkarzinom der Speiseröhre, Chemotherapie-Resistenz, Biomarker INCENP und CDCA8, RNA-m6A-Methylierung