Clear Sky Science · de
K48‑ubiquitin‑abhängige Proteasen zerschneiden post‑ER‑Proteine
Wie Zellen entscheiden, welche Proteine zu vernichten sind
Unsere Zellen entfernen ständig verschlissene oder beschädigte Proteine, insbesondere jene, die in Membranen eingebettet sind und als Tore oder Sensoren dienen. Diese Arbeit zeigt, dass Zellen Ubiquitin, ein winziges Anhängsel, nicht nur als generelles „Müll“-Etikett verwenden, sondern als einen Code, der Membranproteinen genau vorgibt, wie sie abgebaut werden. Das Verständnis dieses Codes erklärt, wie Zellen gesund bleiben, und kann künftige Therapien informieren, die gezielt krankheitsauslösende Proteine entfernen sollen.
Ein zellulärer Barcode für die Entsorgung von Proteinen
Zellen versehen unerwünschte Proteine mit Ketten eines kleinen Proteins namens Ubiquitin. Diese Ketten können auf verschiedene Weisen verknüpft sein, ähnlich wie Perlen, die durch unterschiedliche Löcher gefädelt werden, und jedes Muster kann ein anderes Schicksal signalisieren. Die Autoren konzentrierten sich auf Membranproteine, die bereits das endoplasmatische Retikulum (ER) verlassen haben und durch Kompartimente wie Golgi und Endosomen reisen. Sie fragten, ob zwei gebräuchliche Kettentypen, sogenannte K48‑verknüpfte und K63‑verknüpfte Ubiquitinketten, wirklich austauschbare Markierungen sind oder ob sie die Fracht in unterschiedliche Abbauwege lenken.
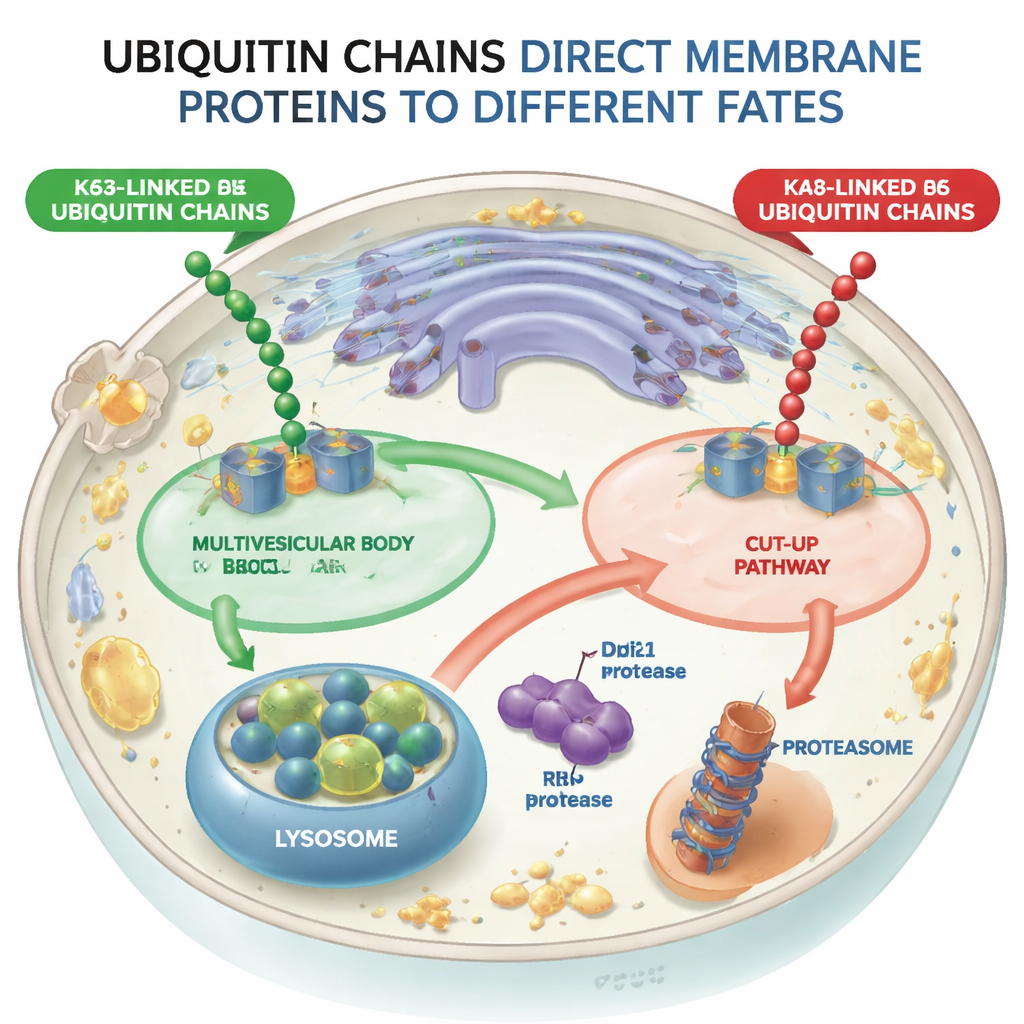
Zwei sich gabelnde Wege für markierte Proteine
Mithilfe von Hefezellen als Modell bauten die Forschenden molekulare Maschinen (Ubiquitin‑Ligasen), die entweder K48‑verknüpfte oder K63‑verknüpfte Ketten an dasselbe Test‑Membranprotein, einen Sortierrezeptor namens Vps10, anhängen konnten. Trug Vps10 K63‑verknüpfte Ketten, wurde es in innere Vesikel innerhalb der Endosomen geleitet—Strukturen, die als multivesikuläre Körper bekannt sind—und gelangen schließlich in Lysosomen, die Verdauungskompartimente der Zelle. Im Gegensatz dazu folgte Vps10 mit K48‑verknüpften Ketten nicht diesem multivesikulären Weg. Stattdessen wurde es auf eine völlig andere Weise zerteilt, was zeigt, dass die Zelle zwischen diesen beiden Kettentypen unterscheidet und dass der multivesikuläre Weg K48‑markierte Fracht effektiv ausschließt.
Ein „Cut‑Up“-Pfad, der Proteine in zwei Teile schneidet
Das Team entdeckte, dass K48‑verknüpfte Ketten einen Protein‑Schneid‑Weg auslösen, den sie CUT‑UP nannten, kurz für Cleavage of Ubiquitinated Targets by Ubiquitin‑dependent Proteases. Anstatt das gesamte Protein auf einmal aus der Membran zu ziehen, zerschneidet CUT‑UP es in Stücke, die dann von bestehenden zellulären Entsorgungssystemen fertig abgebaut werden. Ein zentrales Enzym, Ddi1, schwimmt im Zytosol und schneidet den Abschnitt des Membranproteins ab, der zum Zytoplasma zeigt. Dieses Fragment wird dann vom Proteasom, dem Hauptprotein‑Schredder der Zelle, verdaut. Gleichzeitig sitzt ein anderes Enzym, Rbd2, in der Membran selbst und schneidet den Teil des Proteins, der in das Lumen des Kompartiments zeigt, wodurch dieser in den Raum freigesetzt wird, der schließlich mit dem Lysosom verbunden ist. Um K48‑markiertes Vps10 vollständig vor dem Abbau zu schützen, musste Ddi1, Rbd2, das Proteasom und die lysosomalen Enzyme gemeinsam blockiert werden, was bestätigt, dass all diese Komponenten im CUT‑UP‑Pfad zusammenarbeiten.
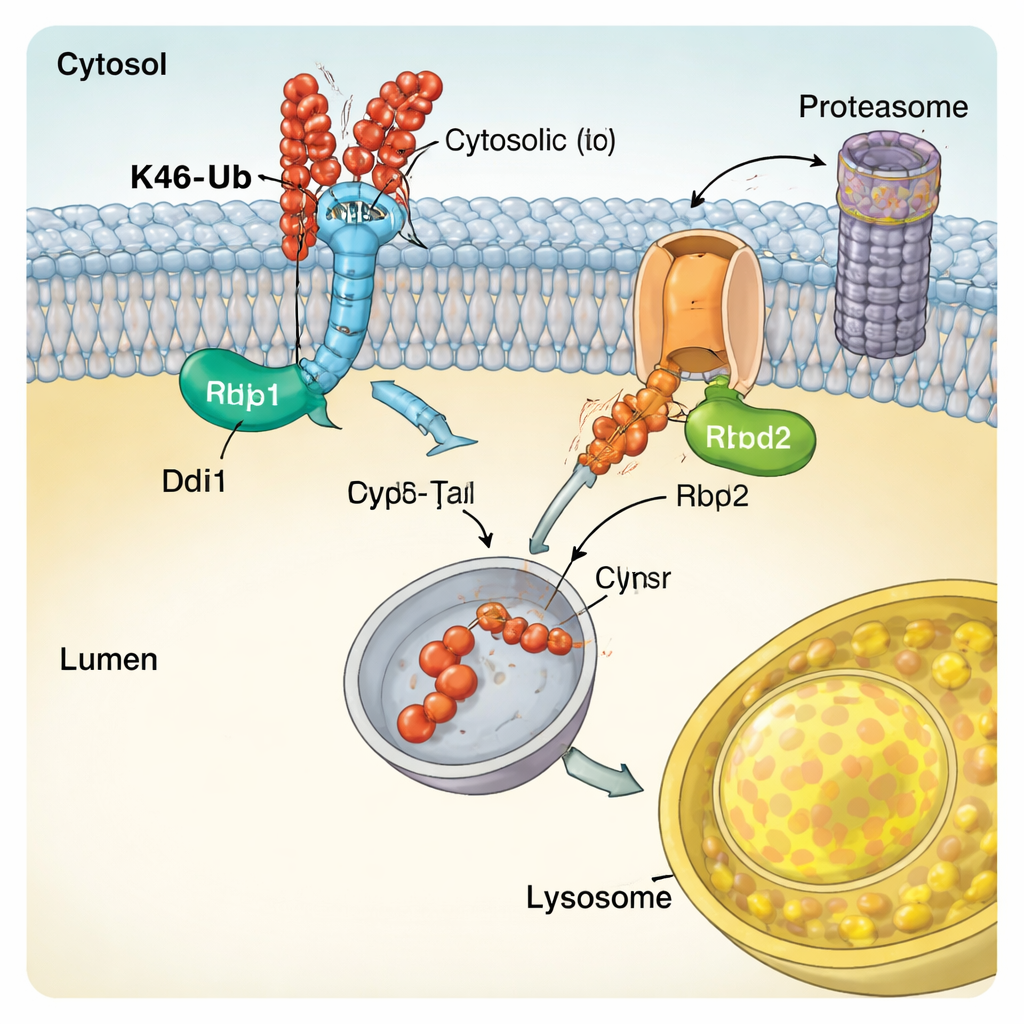
Spezialisierte Enzyme, die den Ubiquitin‑Code lesen
Um zu verstehen, wie CUT‑UP seine Ziele erkennt, untersuchten die Autoren die molekularen Eigenschaften von Ddi1. Sie zeigten, dass der zentrale katalytische Kern von Ddi1 nicht nur Proteine schneidet, sondern Ubiquitin auch direkt binden kann und dass seine Aktivität durch zusätzliche Regionen moduliert wird, die an Ubiquitinketten andocken. Ddi1 zeigte eine besondere Abhängigkeit von K48‑verknüpften Ketten, was zu seiner Rolle in CUT‑UP passt. Rbd2 hingegen ist eine Rhomboid‑Protease, die die Membran durchspannt. Die Studie fand heraus, dass Rbd2s aktives Zentrum für das Schneiden der lumen‑zugewandten Abschnitte von Vps10 essentiell ist und dass das Enzym durch mehrere sekretorische Kompartimente wandert, wodurch es an mehreren zellulären Orten wirken kann. Ähnliche Enzyme existieren in menschlichen Zellen und wurden mit Erkrankungen von Neurodegeneration bis Krebs in Verbindung gebracht, was nahelegt, dass CUT‑UP ähnliche Mechanismen von breiter Bedeutung sein könnten.
Warum das für Gesundheit und Therapie wichtig ist
Indem gezeigt wird, dass unterschiedliche Ubiquitin‑Kettentypen dasselbe Membranprotein in deutlich verschiedene Schicksale schicken—entweder in die Sortierung über multivesikuläre Körper oder in die CUT‑UP‑vermittelte Zerschneidung—liefert diese Arbeit starke Belege dafür, dass Zellen einen echten „Ubiquitin‑Code“ nutzen, um den Proteinabbau fein abzustimmen. Die Entdeckung von CUT‑UP erklärt, wie hartnäckige Membranproteine Stück für Stück demontiert werden können, und hebt Ddi1 und Rbd2 als Schlüsselakteure hervor, die diesen Code lesen und durchsetzen. Für Nicht‑Spezialisten lautet die Schlussfolgerung: Zellen markieren Proteine nicht einfach als Müll; sie legen fest, wie dieser Müll entfernt wird. Wenn Arzneimittelentwickler Werkzeuge entwerfen, die schädliche Proteine mit Ubiquitin markieren, um sie zu entfernen, wird das Verständnis von Wegen wie CUT‑UP entscheidend sein, um vorherzusagen, welche Fragmente entstehen und wie sich das auf das Zellverhalten auswirken könnte.
Zitation: Minard, A.Y., Winistorfer, S., Yu, L. et al. K48-ubiquitin-dependent proteases cut-up post-ER proteins. Nat Commun 17, 1669 (2026). https://doi.org/10.1038/s41467-026-68367-7
Schlüsselwörter: Ubiquitin‑Code, Proteinabbau, Membranproteine, Proteasom, Lysosom