Clear Sky Science · de
Verlust der Fsr-Quorum-Sensing-Funktion fördert Biofilm‑Bildung und verschlechtert den Verlauf der enterokokkenbedingten infektiösen Endokarditis
Stille Saboteure an den Herzklappen
Die infektiöse Endokarditis ist eine lebensbedrohliche Infektion der Herzklappen und weltweit im Zunehmen. Diese Studie konzentriert sich auf einen Hauptverursacher, das Darmbakterium Enterococcus faecalis, und fragt, warum manche Infektionen besonders schwer zu behandeln sind. Indem die Forschenden aufdecken, wie diese Bakterien miteinander kommunizieren und schützende Biofilme auf Herzklappen aufbauen, erklären sie, warum bestimmte Stämme schwerere Erkrankungen auslösen und gegenüber Antibiotika resistenter sind — und warum ein bakterielles Kommunikationssystem namens Fsr überraschenderweise als Bremse und nicht als Beschleuniger des Schadens wirkt.
Wie Bakterien Festungen im Herzen errichten
Herzklappen sind normalerweise dem schnellen Blutfluss ausgesetzt, aber wenn die Klappenoberfläche beschädigt ist, können Thrombozyten und Gerinnungsproteine ein winziges Gerinnsel oder eine Vegetation bilden. Dieses Gerinnsel wird zur Anlegestelle für Bakterien im Blutkreislauf. Nach dem Anhaften vermehren sich die Bakterien und verweben sich zu einem Biofilm — einer schleimigen, strukturierten Gemeinschaft, die sie vor Immunzellen und Medikamenten schützt. Das Team verwendete mikrofluidische Vorrichtungen, um den Blutfluss im Labor nachzubilden, und ein Rattenmodell, um Endokarditis in lebenden Tieren zu rekonstruieren; so konnten sie beobachten, wie sich E. faecalis anpasst, wenn die Infektion von wenigen verstreuten Zellen zu dicken, reifen Biofilmen fortschreitet. 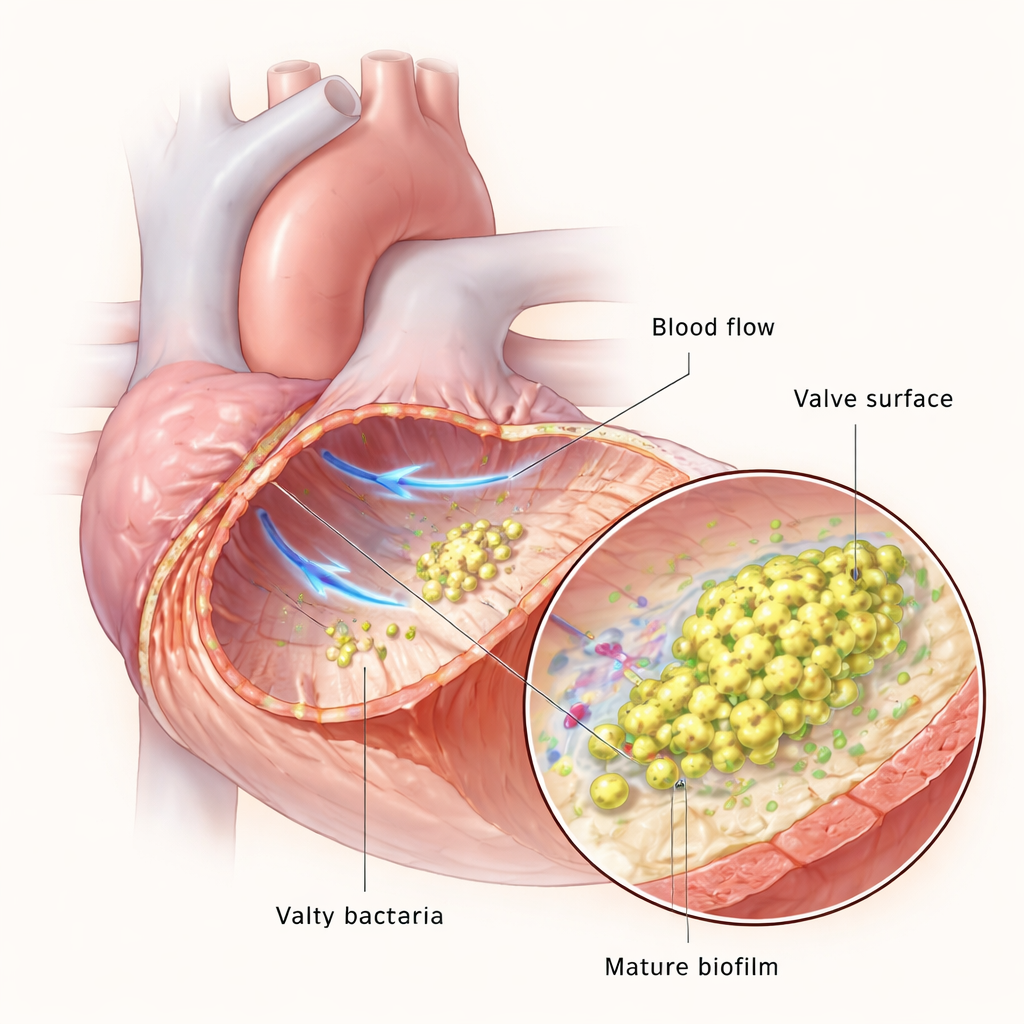
Wenn starker Blutfluss das bakterielle „Geplauder“ ausschaltet
Bakterien koordinieren ihr Verhalten häufig über Quorum Sensing, ein chemisches „Abstimmungssystem“, das Gene ein- oder ausschaltet, sobald genügend Zellen vorhanden sind. Fsr ist das Quorum-Sensing-System von E. faecalis. Überraschenderweise fanden die Forschenden heraus, dass starker, bewegter Flüssigkeitsstrom die Signalstoffe, die für die Aktivierung von Fsr nötig sind, tatsächlich wegspült. In frühen Stadien der Infektion, wenn Bakterien auf der freiliegenden Oberfläche der Vegetation sitzen und den vollen Blutfluss spüren, bleibt Fsr weitgehend stumm. Erst später, wenn Mikrokolonien größer werden und tiefer in der Vegetation eingelagert sind — vom Fluss abgeschirmt —, wird Fsr aktiviert. Das bedeutet, dass im echten Herzen Quorum Sensing nicht nur von der Zahl der Bakterien abhängt, sondern auch davon, wo sie innerhalb der dreidimensionalen Struktur sitzen.
Das Abschalten von Fsr lässt Biofilme überwuchern
Um zu testen, welche Rolle Fsr in der Infektion spielt, verglich das Team normale Bakterien mit Mutanten, denen das gesamte Fsr-System fehlte. Zu Beginn kolonisierten beide Formen die Klappen gleichermaßen gut. Nach drei Tagen hatten Tiere, die mit Fsr-defizienten Stämmen infiziert waren, jedoch größere Vegetationen und deutlich mehr Bakterien darin. Detaillierte Bildgebung zeigte, dass ihre Biofilme mehr von der Gerinnseloberfläche bedeckten und ihre Mikrokolonien größer waren. Der Verlust von Fsr schaltete außerdem zwei wichtige sezernierte Enzyme, GelE und SprE, ab, die normalerweise den Biofilm mitgestalten und ein Überwachsen begrenzen können. Tiere, die nur mit Mutanten infiziert waren, denen diese Enzyme fehlten, entwickelten ebenfalls voluminösere Biofilme, wenn auch nicht so extrem wie die Fsr-null-Stämme, was darauf hindeutet, dass weitere Fsr-regulierte Faktoren eine Rolle spielen. 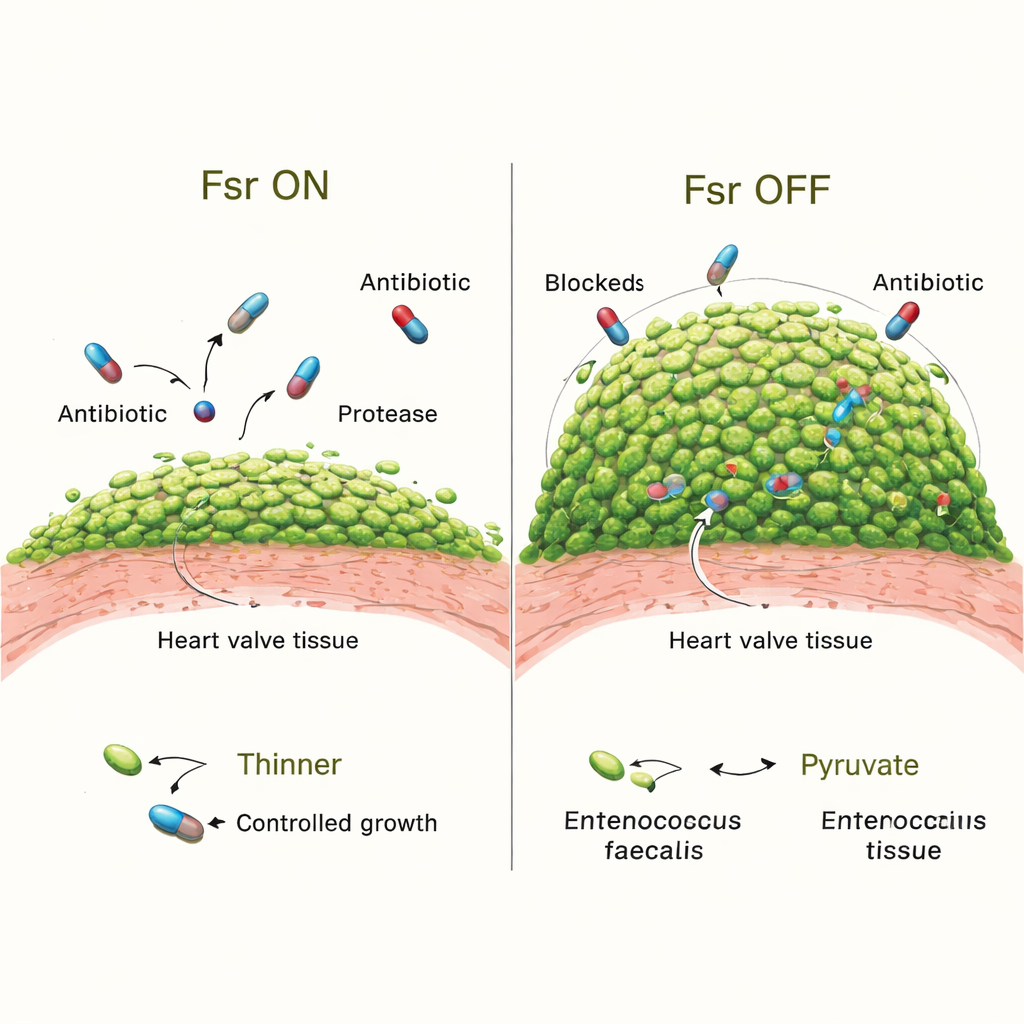
Metabolische Umprogrammierung und stärkerer Schutz vor Antibiotika
Die Genexpressionsprofile von Bakterien in infizierten Klappen zeigten, dass Fsr mehr reguliert als nur ein paar Enzyme. Ohne Fsr veränderte sich die Aktivität hunderter Gene, besonders solcher, die an Zuckeraufnahme und Energieproduktion beteiligt sind. Ein Genpaar, lrgA und lrgB, stach dabei hervor: Diese Gene wurden in Fsr-defizienten Bakterien stark hochreguliert und halfen den Zellen, Pyruvat — ein kleines, energiereiches Molekül im Blut — besser zu nutzen. Als die Forschenden lrgAB zusammen mit Fsr löschten, verschwand das übermäßige Biofilmwachstum, was auf eine Schlüsselrolle dieses Stoffwechselwegs für die überwagente Infektion hinweist. Auffällig war auch, dass Fsr-defiziente Biofilme schwerer zu behandeln waren. In mit Gentamicin behandelten Ratten schrumpften Infektionen mit normalen Bakterien und die Thrombozytenzahlen — ein Marker für Schwere der Erkrankung — verbesserten sich. Im Gegensatz dazu sprachen Fsr-defiziente Infektionen kaum an, obwohl die Bakterien in standardisierten Labortests nicht resistenter gegen das Medikament waren.
Ein human-spezifischer Dreh in der Entzündung
Die Studie förderte zudem einen möglichen Mechanismus zutage, wie diese Bakterien beim Menschen Entzündungen anfachen könnten. Das Enzym GelE kann das humane Vorläuferprotein des Immunsignals IL-1β so schneiden, dass die aktive Form entsteht und Entzündungsreaktionen auslöst. Auffällig war, dass GelE das Ratten-IL-1β anders schnitt — es wurde dabei eher abgebaut als aktiviert — und die genaue „aktivierende“ Schnittstelle in Ratten- und Mausproteinen fehlte. Dieser artspezifische Effekt deutet darauf hin, dass GelE beim Menschen Entzündung gezielt an der Biofilmgrenze fokussieren und so das Gewebeschädigungsgeschehen bei Endokarditis verschärfen könnte.
Vom Labor zum Patienten: Warum der Verlust von Fsr für Patienten relevant ist
Um zu prüfen, ob diese experimentellen Befunde klinische Relevanz haben, analysierten die Forschenden E. faecalis-Isolate von 81 Patienten mit infektiöser Endokarditis in der Schweiz und den USA. Fast die Hälfte der Stämme fehlte von Natur aus das Fsr-System. Patienten, die mit diesen Fsr-negativen Stämmen infiziert waren, hatten länger anhaltende Bakteriämien — also mehr Tage mit nachweisbaren Bakterien im Blut — und wurden häufiger in eine Hochschwere-Kategorie eingeordnet, die Intensivpflege, verlängerte Krankenhausaufenthalte, größere Herzoperationen oder Tod einschloss. Andere Virulenzgene konnten dieses Muster nicht erklären, was den Verlust von Fsr direkt als wichtigen Marker für aggressivere Erkrankungsverläufe hervorhebt.
Warum das für künftige Therapien wichtig ist
Zusammen kehren diese Befunde die einfache Vorstellung um, dass das Blockieren bakterieller Kommunikation stets Infektionen schwächt. Bei E. faecalis-Endokarditis bremst das Fsr-System tatsächlich die Biofilmerweiterung und macht Bakterien anfälliger für Antibiotika. Fehlt Fsr, bilden die Bakterien dichtere Biofilme, nutzen Blutnährstoffe effizienter und treiben hartnäckige, langwierige Infektionen voran. Für Patienten bedeutet dies, dass Stämme ohne Fsr schwerer zu behandeln sein können, und dass Therapien, die Quorum Sensing pauschal abschalten, in diesem Fall nach hinten losgehen könnten. Stattdessen könnten gezielte Ansätze, etwa die Beeinflussung metabolischer Wege wie der Pyruvatnutzung oder das Monitoring von Fsr- und GelE-Status als prognostische Marker, bessere Strategien zur Behandlung dieser gefährlichen Herzinfektionen bieten.
Zitation: Antypas, H., Schmidtchen, V., Staiger, W.I. et al. Loss of Fsr quorum sensing promotes biofilm formation and worsens outcomes in enterococcal infective endocarditis. Nat Commun 17, 1668 (2026). https://doi.org/10.1038/s41467-026-68366-8
Schlüsselwörter: infektiöse Endokarditis, bakterielle Biofilme, Quorum Sensing, Enterococcus faecalis, Antibiotikatoleranz