Clear Sky Science · de
Ingenieurmäßiges VPg-saRNA ermöglicht kap-unabhängige, niedrig-immunogene und präzise Kodierung therapeutischer Proteine in vivo
Die Regeln für RNA-Medikamente neu schreiben
Auf Boten-RNA (mRNA) basierende Impfstoffe haben die Wende gegen COVID-19 mitermöglicht. Doch ähnliche Moleküle einzusetzen, um in chronischen Krankheiten fehlende Proteine zu ersetzen oder zu ergänzen, ist deutlich schwieriger. Der Körper baut fremde RNA rasch ab und löst starke Immunreaktionen aus, und viele bestehende Entwürfe selbstverstärkender RNA machen beim Kopieren Fehler. Diese Studie beschreibt eine neue Art selbstverstärkender RNA – zusammengesetzt aus Teilen des humanen Norovirus – die so konstruiert ist, dass sie langlebiger, weniger entzündlich und ungewöhnlich genau ist. Das öffnet Wege für präzisere und dauerhaftere RNA-Medikamente.
Eine schlauere sich selbst kopierende RNA
Konventionelle mRNA-Medikamente enthalten eine einzelne „Anleitung“ für ein Protein und werden von der Zelle einmal gelesen, bevor sie abgebaut werden. Selbstverstärkende RNA (saRNA) trägt zusätzliche virale Komponenten, die der RNA erlauben, sich innerhalb der Zellen zu vervielfältigen und so aus einer kleinen Dosis viel mehr Protein zu produzieren. Am besten untersucht sind saRNA-Systeme aus Alphaviren, doch sie sind groß, aktivieren starke antivirale Abwehrmechanismen und kopieren mit relativ geringer Genauigkeit. Die Autoren griffen stattdessen auf humanen Norovirus zurück, einen häufigen Erreger von Magen-Darm-Erkrankungen. Sie isolierten einen kompakten Abschnitt des Norovirus-Genoms und bauten ihn als Träger für therapeutische Gene um. Im Zentrum steht VPg, ein kleines virales Protein, das chemisch an das 5'-Ende der RNA gebunden ist. VPg ersetzt die übliche „Cap“-Struktur menschlicher mRNA und ermöglicht der RNA, von einem anderen Satz zellulärer Faktoren übersetzt zu werden, die weniger empfindlich auf bestimmte Stresssignale reagieren. 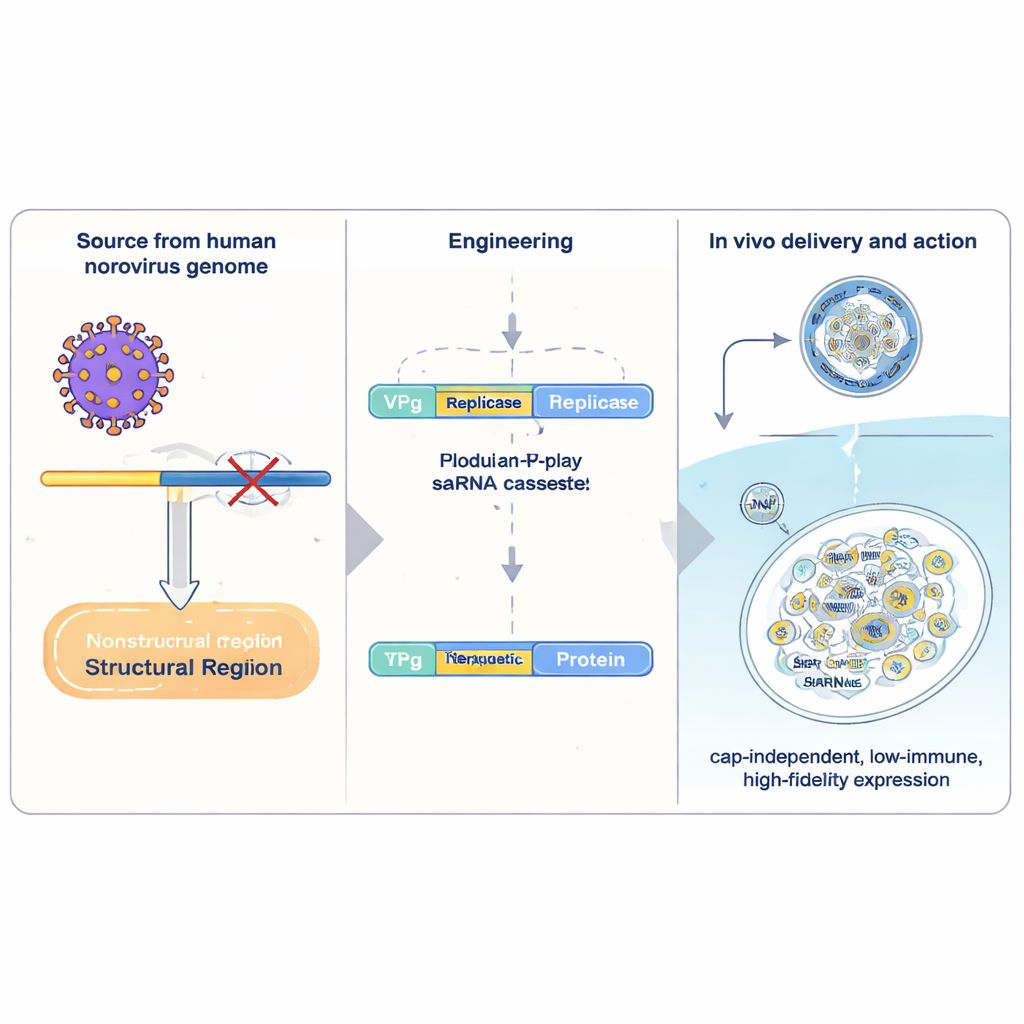
Hohe Genauigkeit ohne Immunsturm
Für Proteintherapien ist Genauigkeit wichtig: Schon kleine Kopierfehler können das Verhalten eines Wirkstoffs verändern oder toxische Nebenprodukte erzeugen. Das Team zeigte, dass, wenn VPg des Norovirus an das RNA-Polymerase-Enzym bindet, die Rate, mit der falsche Bausteine eingebaut werden, verlangsamt wird, wodurch die Fehlerrate stark sinkt. Sie identifizierten bestimmte Aminosäuren in VPg, die eine Schlüsselregion der Polymerase berühren, und zeigten, dass die Störung dieser Schnittstelle die Kopiergenauigkeit verschlechtert. Gleichzeitig erzeugen klassische saRNA-Designs große Mengen doppelsträngiger RNA, eine molekulare Alarmglocke, die antivirale Abwehrmechanismen aktiviert und die Proteinsynthese herunterfährt. Durch das Redesign der Polymerase zugunsten einer bestimmten VPg-gebundenen Startform und durch die Umordnung des Genoms, sodass nur der therapeutische Strang effizient produziert wird, verringerten die Autoren die Bildung doppelsträngiger RNA deutlich. Sie passten zudem eine Schwanzregion der RNA so an, dass VPg an der korrekten Stelle anbindet und kurzlebige, unbeabsichtigte Fragmente verhindert, die in streunende Peptide übersetzt werden könnten.
Wirksam dort, wo Standard-mRNA versagt
Die neue VPg-basierte saRNA wurde in anspruchsvollen Krankheitsszenarien getestet, in denen gewöhnliche cap-tragende mRNA versagt. Bei krebsbedingter Kachexie – einem Auszehrungssyndrom, bei dem Muskeln und Fettgewebe schwinden – sind wichtige Translationsfaktoren, die die Standard-mRNA-Cap erkennen, abgeschaltet, wodurch cap-abhängige mRNAs ineffizient werden. Weil VPg einen alternativen Zugang zur zellulären Translationsmaschinerie nutzt, trieb es weiterhin die Produktion des Appetit- und Stoffwechselhormons Ghrelin in einem Mausmodell für Bauchspeicheldrüsenkrebs an. Monatliche Niedrigdosis-Injektionen halfen, Muskel- und Fettmasse zu erhalten, verbesserten Nahrungsaufnahme und Stoffwechsel und verlängerten das Überleben moderat, ohne offensichtliche Toxizität oder Anzeichen chronischer Immunaktivierung.
Präziser Krebsangriff und gedämpfte Autoimmunreaktionen
Um zu prüfen, ob hohe Kopiergenauigkeit tatsächlich einen Unterschied macht, beluden die Forschenden den VPg-Vektor mit einem komplexen onkolytischen Konstrukt, GSDMDENG, das dazu entworfen ist, Löcher in Mitochondrien von Krebszellen zu schlagen und tumorspezifische Immunantworten zu stimulieren. Wurde dasselbe Konstrukt in einer konventionellen Alphavirus-saRNA platziert, akkumulierten Mutationen über wiederholte Kopierrunden und schwächten seine selektive krebsabtötende und immunstimulierende Wirkung. Im Gegensatz dazu erhielt das VPg-System die beabsichtigte Sequenz, erzeugte starke Tumorzelllyse und löste langlebige T-Zell-Antworten aus, die das Fortschreiten von Bauchspeicheldrüsenkrebs in Mausmodellen verlangsamten oder verhinderten. Schließlich wandten sie VPg-saRNA auf eine andere Herausforderung an: chronische Graft-versus-Host-Erkrankung, bei der Immunzellen nach Knochenmarkstransplantation die Lunge angreifen. Eine VPg-saRNA, die aktiviertes Protein C codiert, verringerte die schädliche Antikörperbildung, verhinderte Lungennarbung und verbesserte die Atmung bei Mäusen, während ein vergleichbares Alphavirus-basiertes Konstrukt stärkere angeborene Immunreaktionen auslöste und die Ergebnisse verschlechterte.
Warum das für künftige RNA-Arzneien wichtig ist
Insgesamt skizziert die Arbeit eine kompakte, „Plug-and-Play“-RNA-Plattform, die drei erwünschte Eigenschaften kombiniert: sie vervielfältigt sich mit hoher Genauigkeit, ist darauf ausgelegt, Immunalarme zu minimieren, und umgeht einige der Engpässe, die die Standard-mRNA-Translation beschränken. Da das therapeutische Gen einfach in ein festes, norovirus-basiertes Rückgrat eingesetzt wird, können viele verschiedene Proteine – von Hormonen über Gerinnungsregulatoren bis hin zu onkolytischen Wirkstoffen – auf derselben Plattform getestet werden. Obwohl vor einer Anwendung am Menschen noch viel Arbeit nötig ist, deutet dieser VPg-saRNA-Ansatz auf einen Weg zu RNA-Medikamenten hin, die eher wie stabile Proteininfusionen wirken: niedrig dosiert, länger anhaltend und darauf ausgelegt, selbst in erkranktem Gewebe zu funktionieren, wo gewöhnliche mRNA-Botschaften nicht zuverlässig gelesen werden können. 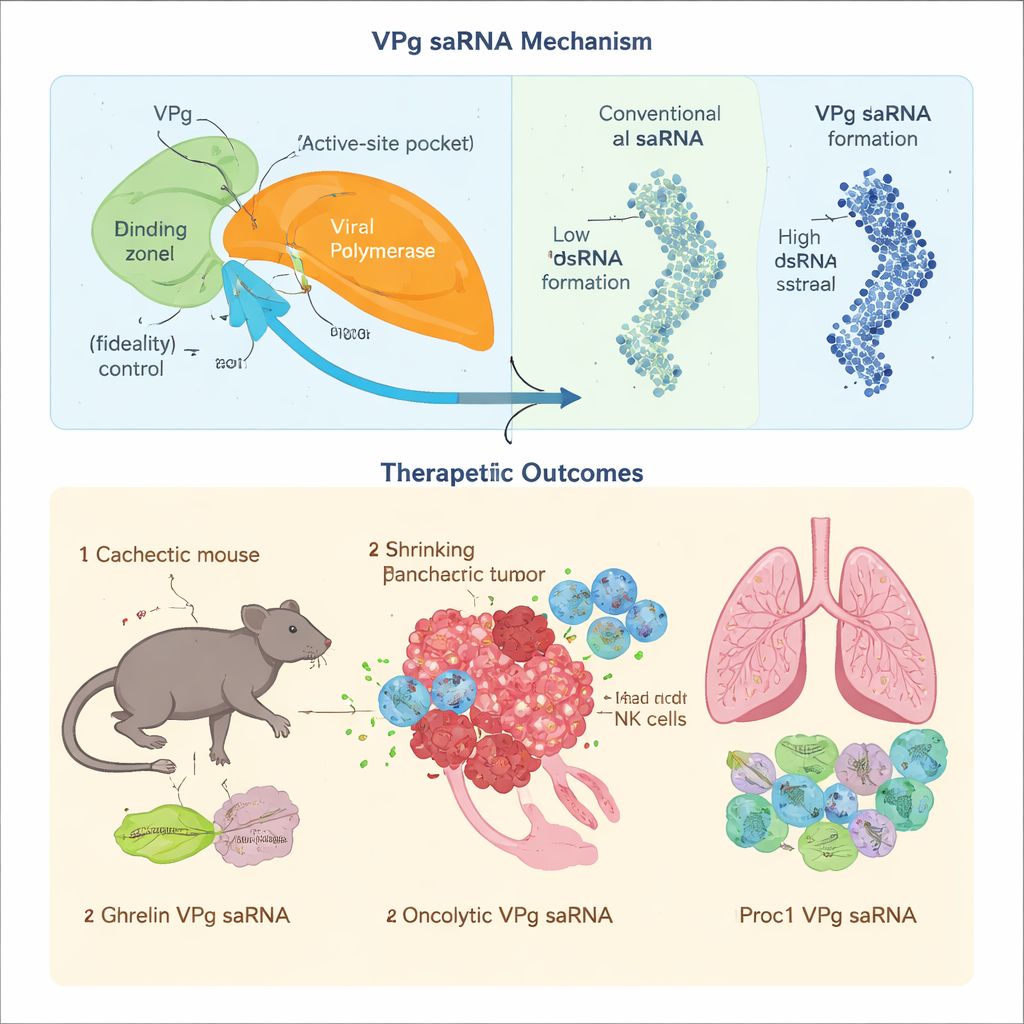
Zitation: Feng, Z., Chu, L., Li, Q. et al. Engineered VPg saRNA achieves cap-independent, low-immunogenic and precise encoding of therapeutic proteins in vivo. Nat Commun 17, 1666 (2026). https://doi.org/10.1038/s41467-026-68364-w
Schlüsselwörter: selbstverstärkende RNA, mRNA-Therapeutika, Norovirus-VPg, Krebs-Kachexie, Graft-versus-Host-Krankheit